网址:http://m.1010jiajiao.com/timu3_id_412627[举报]
用化学方法测定微量碘化物时,必须利用“化学放大”反应将碘的量“放大”,然后再进行测定。下面是“化学放大”反应的实验步骤:
①向含微量I-并且呈中性或弱酸性溶液里加入溴水,将I-完全氧化成![]() ,煮沸去掉过量的Br2;
,煮沸去掉过量的Br2;
②向由①制得的水溶液中加入过量的酸性KI溶液,振荡使反应进行完全;
③在②得到的水溶液中加入足量的CCl4,振荡,把生成的I2从水溶液里全部转移到CCl4 中,用分液漏斗分液去掉水层;
④向③得到的CCl4层加入肼(即联氨H2N—NH2)的水溶液,振荡,使I2完全以I-形式从CCl4层进入水层,用分液漏斗分液去掉CCl4层。
经过以上四步得到的水溶液里,含有通过反应而“放大”了的碘,请回答下列问题:
(1)写出步骤②的离子方程式,并标出下列反应的电子转移的方向和数目:_______________________。
![]()
(2)将右图所示的分液漏斗中的下层液体放出的操作步骤为:
①___________________________________________。
②旋开活塞,使下层液体流出到一个烧杯里,当下层液体全部流出活塞的细孔时,__________________。
③从漏斗上口倒出上层液体。
④旋开活塞,将留在颈部的下层液体放出到盛接下层液体的烧杯里。
(3)若忽略实验过程中出现的损失,经过一次“化学放大”的溶液里,I-的量是原溶液里I-的量的____________倍。经过n次“化学放大”的溶液里,I-的量是原溶液里的量的________倍。
查看习题详情和答案>>氯、溴、碘的化学性质非常相似.在上个世纪,人们很早就得到了高氯酸和高碘酸及其盐,但无论用什么方法都得不到+7价溴的化合物.因此在很长的一个历史时期,人们认为溴不会表现+7价,1968年有个名叫Appclman的化学家用发现不久的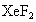 和
和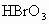 反应,首次检验出
反应,首次检验出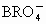 .随后在1971年用
.随后在1971年用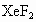 和含KOH、
和含KOH、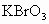 的水溶液反应,得到了很纯的
的水溶液反应,得到了很纯的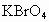 晶体.
晶体.
(1)已知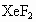 跟水反应放出氧气和氙气,氟则以化合态留在水溶液里,试写出配乎的化学方程式:_________________________________;
跟水反应放出氧气和氙气,氟则以化合态留在水溶液里,试写出配乎的化学方程式:_________________________________;
(2)写出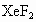 和含KOH、
和含KOH、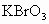 的水溶液反应得到
的水溶液反应得到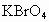 晶体的化学方程式:____________________________________________;
晶体的化学方程式:____________________________________________;
(3)试根据上面的信息指出高溴酸根的稳定性和溶液pH的关系:________________.
查看习题详情和答案>>钠是碱金属元素中最常见的一种,它不仅在日常生活中有重要作用,而且在尖端技术方面也发挥着重要的作用.当前,人们已能利用原子能发电,其中最重要的装置即是原子反应堆.在原子的裂变过程中,由于释放出巨大的能量,会使反应堆内的温度升得很高,因此,就需要把热量导出,使反应堆冷却.钠钾合金以其独特的优点,成为原子反应堆理想的导热传热剂.
在工业上也利用钠制取钛、锆、钽等稀有金属,这些金属在航天工业上有广泛的应用.
在日常生活中钠也有广泛用途,如用于制作单色光源的钠光灯,射程远,透雾能力强,广泛地用于制作指示灯、路灯等.
(1)查表:钠的熔点是97.81℃,钾的熔点是63.55℃,而钠钾合金的熔点是-10℃,这说明________.
(2)写出钠从四氯化钛(TiCl4)中置换出钛的化学方程式,并思考该反应是否可以在水溶液里进行?为什么?________.
(3)雾天行车时,司机不开大灯而开小灯照明,其道理是什么?________.
氯、溴、碘的化学性质非常相似.在上个世纪,人们很早就得到了高氯酸和高碘酸及其盐,但无论用什么方法都得不到+7价溴的化合物.因此在很长的一个历史时期,人们认为溴不会表现+7价,1968年有个名叫Appclman的化学家用发现不久的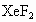 和
和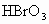 反应,首次检验出
反应,首次检验出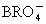 .随后在1971年用
.随后在1971年用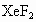 和含KOH、
和含KOH、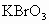 的水溶液反应,得到了很纯的
的水溶液反应,得到了很纯的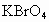 晶体.
晶体.
(1)已知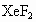 跟水反应放出氧气和氙气,氟则以化合态留在水溶液里,试写出配乎的化学方程式:_________________________________;
跟水反应放出氧气和氙气,氟则以化合态留在水溶液里,试写出配乎的化学方程式:_________________________________;
(2)写出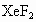 和含KOH、
和含KOH、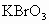 的水溶液反应得到
的水溶液反应得到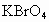 晶体的化学方程式:____________________________________________;
晶体的化学方程式:____________________________________________;
(3)试根据上面的信息指出高溴酸根的稳定性和溶液pH的关系:________________.
查看习题详情和答案>>
请回答下列问题:
(1)A和I的结构简式为A


(2)F中官能团的名称为
(3)反应②、⑥和⑦的反应类型为②
(4)M是一种普遍使用的抗生素类药物,它是由2个F分子在一定条件下脱去2个水分子形成的环状酯,写出该反应的化学方程式


(5)D有两种能发生银镜反应且属链状化合物的稳定同分异构体,请写出它们的结构简式