网址:http://m.1010jiajiao.com/timu3_id_412218[举报]
(05年江苏卷)(10分)右图中,A、C是工业上用途很广的两种重要化工原料,B为日常生活中常见的金属,H、G是正四面体结构的非极性分子,H是一种重要的能源,J是一种耐高温材料,K是由两种常见元素组成的化合物(图中部分反应物或生成物没有列出)
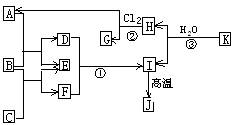 请按要求回答:
请按要求回答:
(1)写出B的化学式_____________________,G的电子式______________________。
(2)反应①的离子方程式为___________________________________。
(3)反应②进行的条件是______________、____________。
(4)反应③的化学方程式为____________________________________。
查看习题详情和答案>>
根据上述流程回答下列问题:
(1)混合①中发生反应的化学方程式为
(2)混合①中使用冰水的目的是
(3)操作Ⅱ和操作Ⅲ的名称分别是
(4)操作Ⅲ一般适用于分离
a.固体和液体 b.固体和固体 c.互不相溶的液体 d.互溶的液体
(5)混合②中加入Na2SO3的目的是
(6)纯净的氢溴酸应为无色液体,但实际工业生产中制得的氢溴酸(工业氢溴酸)带有淡淡的黄色.于是甲乙两同学设计了简单实验加以探究:
甲同学假设工业氢溴酸呈淡黄色是因为含Fe3+,则用于证明该假设所用的试剂为
乙同学假设工业氢溴酸呈淡黄色是因为
(7)检验氢溴酸右美沙芬片含有溴元素的方法是
元素周期表中第ⅦA族元素的单质及其化合物的用途广泛。
(1)能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是 (填序号)。
a.Cl2、Br2、I2的熔点 b. Cl2、Br2、I2的氧化性
c.HCl、HBr、HI的热稳定性 d. HCl、HBr、HI的酸性
(2)工业上,通过如下转化可制得KClO3晶体:
NaCl溶液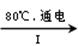 NaClO3溶液
NaClO3溶液 KClO3晶体
KClO3晶体
①完成I中反应的总化学方程式:□NaCl+□H2O=□NaClO3+□ 。
②Ⅱ中转化的基本反应类型是 ,该反应过程能析出KClO3晶体而无其它晶体析出的原因是 。
(3)一定条件,在水溶液中1 mol Cl-、ClOX-(x=1,2,3,4)的能量(KJ)相对大小如右图所示。
①D是 (填离子符号)。
②B→A+C反应的离子方程式为 ;生成1molC时, KJ的热(填吸收或放出以及具体数值)
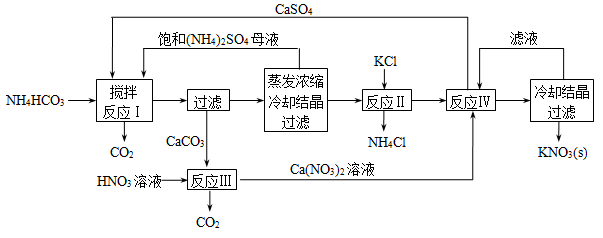
(1)反应Ⅰ中,CaSO4与NH4HCO3的物质的量之比为1︰2,该反应的化学方程式为 。
(2)反应Ⅱ需在干态、加热的条件下进行,加热的目的是 ;从反应Ⅳ所得混合物中分离出CaSO4的方法是 (填“趁热过滤”、“冷却过滤”)。
(3)检验反应Ⅱ所得K2SO4中是否混有KCl的方法是:取少量K2SO4样品溶解于水, 。
(4)整个流程中,可循环利用的物质除(NH4)2SO4外,还有 (填化学式)。
(5)将硝酸与浓KCl溶液混合,也可得到KNO3,同时生成等体积的气体A和气体B。B是三原子分子,B与O2反应生成1体积黄绿色气体A和2体积红棕色气体C。B的分子式为 。
II.(1)工业上可采用电化学的方法获得N2H4,装置如右图所示,则通入氧气的 一极为 (填“正极”、“负极”),NH3反应的电极反应式为 。
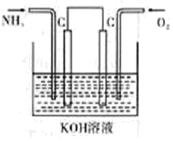
(2)肼(N2H4)可以在纯氧中燃烧生成氮气和水,为了充分利用其能量, 有人设计了原电池装置,电极材料是多孔石墨电极,电解质为能够传导H+的固体电解质,请写出负极反应式 。
(15分)元素周期表中第ⅦA族元素的单质及其化合物的用途广泛。
(1)与氯元素同族的短周期元素的原子结构示意图为 。
(2)能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是 (填序号)。
a.Cl2、Br2、I2的熔点 b. Cl2、Br2、I2的氧化性
c.HCl、HBr、HI的热稳定性 d. HCl、HBr、HI的酸性
(3)工业上,通过如下转化可制得KClO3晶体:
NaCl溶液 NaClO3溶液
NaClO3溶液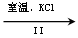 KClO3晶体
KClO3晶体
①完成I中反应的总化学方程式:□NaCl+□H2O=□NaClO3+□ 。
②Ⅱ中转化的基本反应类型是 ,该反应过程能析出KClO3晶体而无其它晶体析出的原因是 。
(4)一定条件,在水溶液中1 mol Cl-、ClO-(x=1,2,3,4)的能量(KJ)相对大小如右图所示。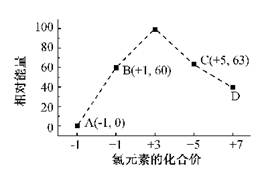
①D是 (填离子符号)。
②B→A+C反应的热化学方程式为 (用离子符号表示)。