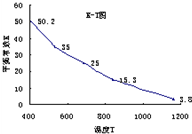
摘要:15.碘在水中溶解度很小.但易溶于KI溶液.因为发生反应:I2(aq)+I-(aq)=I3-.已知在不同温度下该反应的平衡常数如右图.则下列说法正确的是( ) A.上述反应正反应为吸热反应 B.实验室配制碘水.为增大碘的溶解度可加入少量的KI C.降低上述体系的温度.C(I2)增大 D.上述体系中加入CCl4.水溶液中C(I2)增大
网址:http://m.1010jiajiao.com/timu3_id_412097[举报]
碘在水中溶解度很小,但易溶于KI溶液,因为发生反应:I2(aq)+I-(aq)=I3-。已知在不同温度下该反应的平衡常数如右图,下列说法不正确的是( )

A.上述反应正反应为放热反应
B.实验室配制碘水,为增大碘的溶解度可加入少量的KI
C.用该反应原理可除去硫粉中少量的碘单质
D.上述体系中加入苯,平衡不移动
查看习题详情和答案>>碘在水中溶解度很小,但易溶于KI溶液,因为发生反应:I2(aq)+I-(aq)=I3-。已知在不同温度下该反应的平衡常数如右图,下列说法不正确的是( )
A.上述反应正反应为放热反应
B.实验室配制碘水,为增大碘的溶解度可加入少量的KI
C.用该反应原理可除去硫粉中少量的碘单质
D.上述体系中加入苯,平衡不移动
查看习题详情和答案>>
碘在水中溶解度很小,但易溶于KI溶液,因为发生反应:I2(aq)+I-(aq)===I3- (aq)。已知在不同温度下该反应的平衡常数如图:
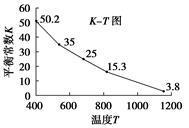
下列说法不正确的是( )
A.上述反应正反应为放热反应
B.实验室配制碘水,为增大碘的溶解度可加入KI
C.用该反应原理可除去硫粉中少量的碘单质
D.上述体系中加入苯,平衡不移动
查看习题详情和答案>>