网址:http://m.1010jiajiao.com/timu3_id_409402[举报]
(7分).化学反应中的能量变化,是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同所致。下图为N2(g)和O2(g)生成NO(g)过程中的能量变化。

(1)人们通常把拆开1mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,则N≡N的键能为________kJ·mol-1,由上图写出N2(g)和O2(g)生成NO(g)的热化学反应方程式________。
(2)1840年,俄国化学家盖斯在分析了许多化学反应热效应的基础上,总结出一条规律:“一个化学反应,不论是一步完成,还是分几步完成,其总的热效应是完全相同的。”这个规律被称为盖斯定律。有些反应的反应热虽然无法直接测得,但可以利用盖斯定律间接计算求得。
①根据下列反应的热化学反应式,计算由C(石墨)和H2(g)反应生成1molC2H2(g)的ΔH。
C(石墨)+O2(g)===CO2(g)ΔH1=-393.5kJ·mol-1
2H2(g)+O2(g)===2H2O(l)ΔH2=-571.6kJ·mol-1
2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l)ΔH3=-2599.2kJ·mol-1,
则由C(石墨)和H2(g)反应生成1molC2H2(g)的ΔH=________kJ·mol-1。
②已知3.6g碳在6.4g的氧气中燃烧,至反应物耗尽,并放出XkJ热量。已知单质碳的燃烧热为YkJ·mol-1,则1molC与O2反应生成CO的反应热ΔH为________。
查看习题详情和答案>>
I.取5ml 0.1mol/L的KI溶液,滴加5-6滴FeCl3稀溶液;
Ⅱ.继续加入2mlCCl4振荡
Ⅲ.取萃取后的上层清液,滴加KSCN溶液.
(1)探究活动I的实验现象为
探究活动Ⅱ的实验现象为
(2)探究活动Ⅲ的意图是通过生成血红色的Fe(SCN)3溶液,验证有Fe3+残留,从而证明化学反应有一定的限度,但在实验中却未见溶液呈血红色.对此同学们提出了下列两种猜想:
猜想一:Fe3+全部转化为Fe2+
猜想二:生成的Fe(SCN)3浓度极小,其颜色肉眼无法观察.
为了验证猜想,查阅资料获得下列信息:
信息一:乙醚微溶于水,Fe(SCN)3在乙醚中的溶解度比在水中大;
信息二:Fe3+可与[Fe(CN)6]4-反应生成蓝色沉淀,用K4[Fe(CN)6]溶液检验Fe3+的灵敏度比用KSCN更高.
结合新信息,现设计以下实验方案验证猜想:
①请完成下表
| 实验操作 | 现象和结论 |
| 步骤一: | 若产生蓝色沉淀,则 |
| 步骤二: | 若乙醚层呈血红色,则 |
Ⅳ.为了测定探究活动I中的FeCl3稀溶液的浓度,现进行以下操作:
①移取25.00mLFeCl3稀溶液至锥形瓶中,加入
②重复滴定三次,平均耗用c mol/LKI标准溶液VmL,则FeCl3稀溶液物质的量浓度为
③若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果
㈠2SO2(g)+O2(g) ![]() 2SO3(g)反应过程的能量变化如图
2SO3(g)反应过程的能量变化如图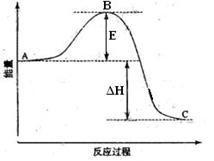 所示。已知1mol SO2(g)氧化为1mol SO3的ΔH=-99kJ·mol-1.
所示。已知1mol SO2(g)氧化为1mol SO3的ΔH=-99kJ·mol-1.
请回答下列问题:
⑴图中A、C分别表示 、 ,E的大小对该反应的反应热有无影响? 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低? ,理由是 ;
⑵图中△H= KJ·mol-1;
⑶已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H(要求写出计算过程)。
 ㈡进一步研究表明,化学反应的能量变化(ΔH)与反应物和生成物的键能有关。键能可以简单地理解为断开1 mol化学键所需吸收的能量,表中是部分化学键的键能数据:
㈡进一步研究表明,化学反应的能量变化(ΔH)与反应物和生成物的键能有关。键能可以简单地理解为断开1 mol化学键所需吸收的能量,表中是部分化学键的键能数据:
| 化学键 | P—P | P—O | O==O | P==O |
| 键能/kJ·mol-1 | 197 | 360 | 499 | x |
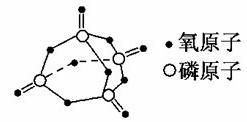
已知白磷的燃烧热为2378.0 kJ/mol,白磷完全燃烧的产物结构如图Ⅲ所示,则上表中x=________。
查看习题详情和答案>>已知:

以乙炔为原料,通过下图所示步骤能合成有机物中间体E(转化过程中的反应条件及部分产物已略去)。

其中,A、B、C、D分别代表一种有机物;B的分子式为C4H10O2,分子中无甲基。[来源:]
请回答下列问题:
(1)A→B的化学反应类型是 。
写出B→C化学方程式: 。
(2)E和H2完全加成得到的物质的结构简式是 。
(3)写出符合下列条件的E的两种同分异构体 。
A.含有苯环 B.属于酯类 C.可发生银镜反应
(4)下列说法正确的是
A.上述流程中,乙炔、有机物B、有机物E都可发生聚合反应
B.有机物E能使酸性KMnO4溶液褪色,可说明E含碳碳双键
C.有机物C的名称为丁二醛,C具有还原性
D.甲醛(HCHO)溶液俗称福尔马林溶液,能使蛋白质变性
(5)C到D的变化可表示为2C→D,D的结构简式是 。
查看习题详情和答案>>
(14分)由乙酰水杨酸(ASS)制成的阿司匹林是德国一家制药公司于1899年合成出的止痛剂(Pain Reliefers)。长时间以来一直被广泛的使用,现在每年的需求量仍是很高。ASS可由下列反应序列合成制得:
![]()

(1)写出A与B的结构简式及B与乙酸酐反应的化学方程式
(2)B物质与乙酸酐反应时,还会生成一些副产品,其中有一种是高分子,其结构简式为__________。为了除去此物质,可在产物中加入_______溶液,再经过滤、酸化等步骤可得较纯净的ASS。
(3)为了测定自制乙酰水杨酸的纯度,一般可采用以下步骤:准确称取自制的乙酰水杨酸三份,每份约0.25g,分别置于250mL锥形瓶中,加入25 mL 95%乙醇(已调至对酚酞指示剂显中性),摇动使其溶解,再向其中加入适量酚酞指示剂,用准确浓度的NaOH溶液滴定至出现微红色,30秒钟不变色为终点,分别记录所消耗NaOH溶液的体积,根据所消耗NaOH溶液的体积,分别计算乙酰水杨酸的质量分数。在上述测定过程中,为防止乙酰水杨酸在滴定过程中水解,应如何正确操作?并说明理由。
(4)为了测定阿司匹林片剂中乙酰水杨酸的含量,通常采用返滴定法。步骤为:称取10片药物(设总质量为w总/g),研细混匀后,准确称取一定量(G/g)药粉于锥形瓶中,加入V1/mL(过量)的NaOH标准溶液[浓度c(NaOH)/mol?L-1],于水浴上加热使乙酰基水解完全后,再用HCl标准溶液[浓度c(HCl)/mol?L-1]回滴,以酚酞为指示剂,耗去HCl溶液V2/mL。请列出求算每片药中含有乙酰水杨酸的质量(g/片)的计算式。
![]() 已知乙酰水杨酸可溶于NaOH溶液中,并生成水杨酸盐和乙酸盐。其溶解反应式可表示为:
已知乙酰水杨酸可溶于NaOH溶液中,并生成水杨酸盐和乙酸盐。其溶解反应式可表示为:
![]()

![]() 乙酰水杨酸的摩尔质量为180.2g?mol-1,水杨酸的pKal=3.0,pKa2=13.1,乙酸的pKa=4.75
乙酰水杨酸的摩尔质量为180.2g?mol-1,水杨酸的pKal=3.0,pKa2=13.1,乙酸的pKa=4.75