网址:http://m.1010jiajiao.com/timu3_id_408555[举报]
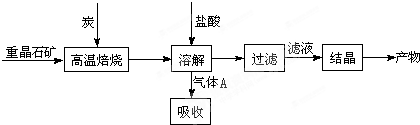
某研究小组在实验室用重晶石(主要成分BaSO4)对工业过程进行模拟实验.
查表得:BaSO4(s)+4C(s)
| 高温 |
BaSO4(s)+2C(s)
| 高温 |
(1)①制备BaCl2的工艺流程图中气体A用过量NaOH溶液吸收,得到硫化钠.Na2S水解的离子方程式为:
②常温下,相同浓度的Na2S和NaHS溶液中,下列说法正确的是:
A.Na2S溶液的pH比NaHS溶液pH大
B.两溶液中含有的离子种类不同
C.两溶液中滴入同体积同浓度的盐酸,产生气体速率相等
D.两溶液中加入NaOH固体,c(S2-)都增大
E.NaHS溶液中:c(Na+)>c(HS-)>c(OH-)>c (H+)>c(S2-)
(2)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,
| c(Br-) |
| c(Cr-) |
[已知:Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10]
(3)反应C(s)+CO2(g)
| 高温 |
(4)实际生产中必须加入过量的炭,同时还要通入空气,其目的是:①
工业上制备 BaC12 的工艺流程图如图所示: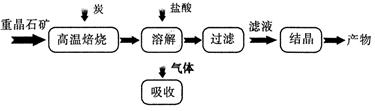
某研究小组在实验室用重晶石(主要成分BaSO4)对工业过程进行模拟实验。查表得: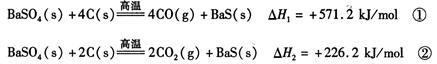
(1)反应C(s) + CO2(g) 2CO(g)的△H = kJ/mol
2CO(g)的△H = kJ/mol
(2)过滤过程中需要使用玻璃棒,玻璃棒的作用是 。
(3)盐酸溶解焙烧的固体后,产生的气体用过量 NaOH 溶液吸收,得到硫化钠溶液。 Na2S 水解的离子方程式为 。
(4)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,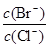 = 。[已知:
= 。[已知:
Ksp(AgBr) = 5.4×10─13 , Ksp(AgCl) = 2.0×10─10]
工业上制备 BaC12 的工艺流程图如图所示:

某研究小组在实验室用重晶石(主要成分BaSO4)对工业过程进行模拟实验。查表得:

(1)反应C(s) + CO2(g) 2CO(g)的△H = kJ/mol
2CO(g)的△H = kJ/mol
(2)过滤过程中需要使用玻璃棒,玻璃棒的作用是 。
(3)盐酸溶解焙烧的固体后,产生的气体用过量 NaOH 溶液吸收,得到硫化钠溶液。 Na2S 水解的离子方程式为 。
(4)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,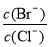 = 。[已知:
= 。[已知:
Ksp(AgBr) = 5.4×10─13 , Ksp(AgCl) = 2.0×10─10]
查看习题详情和答案>>
(10分)工业上制备BaCl2的工艺流程图如下:

某研究小组在实验室用重晶石(主要成分BaSO4)对工业过程进行模拟实验。查表得
BaSO4(s) + 4C(s)![]() 4CO(g) + BaS(s) △H1 = 571.2 kJ·mol-1 ①
4CO(g) + BaS(s) △H1 = 571.2 kJ·mol-1 ①
BaSO4(s) + 2C(s)![]() 2CO2(g) + BaS(s) △H2= 226.2 kJ·mol-1 ②
2CO2(g) + BaS(s) △H2= 226.2 kJ·mol-1 ②
⑴气体用过量NaOH溶液吸收,得到硫化钠。Na2S水解的离子方程式为 。 (2)反应C(s) + CO2(g)![]() 2CO(g)的△H2= kJ·mol-1。
2CO(g)的△H2= kJ·mol-1。
(3)“温室效应”是全球关注的环境问题之一。CO2是目前大气中含量最高的一种温室气体。因此,控制和治理CO2是解决温室效应的有效途径。
①下列措施中,有利于降低大气中CO2浓度的有: 。(填字母)
a.减少化石燃料的使用 b.植树造林,增大植被面积
c.采用节能技术 d.利用太阳能、风能
②将CO2转化成有机物可有效实现碳循环。CO2转化成有机物的例子很多,如:
a.6CO2 + 6H2O![]() C6H12O6 b.CO2 + 3H2
C6H12O6 b.CO2 + 3H2![]() CH3OH +H2O
CH3OH +H2O
c.CO2 + CH4![]() CH3COOH d.2CO2 + 6H2
CH3COOH d.2CO2 + 6H2![]() CH2==CH2 + 4H2O
CH2==CH2 + 4H2O
以上反应中,最节能的是 ,原子利用率最高的是 。
查看习题详情和答案>>
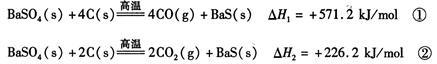
 2CO(g)的△H = kJ/mol
2CO(g)的△H = kJ/mol = 。[已知:
= 。[已知: