网址:http://m.1010jiajiao.com/timu3_id_406020[举报]
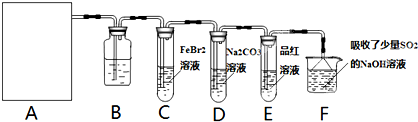
(1)若A是用二氧化锰和浓盐酸反应制取氯气的发生装置,除圆底烧瓶和导管外还用到的玻璃仪器有
(2)①装置B中盛有的试剂是
②若E中品红溶液褪色,则C装置中发生反应的离子方程式是
③已知碳酸的酸性强于次氯酸,则装置D中反应的化学方程式为
(3)某研究性学习小组用刚吸收过少量SO2的NaOH溶液吸收处理上述实验后的尾气.吸收尾气一段时间后,吸收液(呈强碱性)中肯定存在Cl-、OH-、CO32-和SO42-.请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑盐类的水解;在碱性条件下ClO-也有强氧化性.).
①提出合理假设:
假设1:只存在SO32-;
假设2:只存在ClO-;
假设3:既存在SO32-,也存在ClO-;
假设4:既不存在SO32-,也不存在ClO-.
指导老师经分析认为,其中一个假设并不合理,它是
②设计实验方案,进行实验,请写出实验步骤以及预期现象和结论.限选实验试剂.
a.3mol/L H2SO4 b.0.01mol/L KMnO4 c.1mol/L BaCl2溶液
d.淀粉一KI溶液 e.酚酞试液 f.品红溶液
步骤一;取少量吸收液于试管中,滴加3mol/L H2SO4至溶液呈酸性,然后将所得溶液分装于A、B两试管中.
步骤二:向A试管中滴加1~2滴
步骤三:向B试管中滴加1~2滴
③若假设2成立;写出步骤三中的离子方程式:
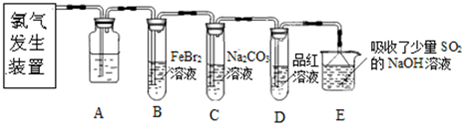
(1)实验室用二氧化锰和浓盐酸加热制取氯气,发生装置中除圆底烧瓶和导管外还需用到的玻璃仪器有
(2)装置A中盛有的试剂是
(3)若D中品红溶液褪色,则B装置中发生反应的离子方程式是
(4)证明FeBr2与Cl2发生了氧化还原反应的实验方法是
某研究性学习小组用刚吸收过少量SO2的NaOH溶液吸收处理上述实验后的尾气.经分析吸收尾气一段时间后,吸收液(呈强碱性)中肯定存在Cl-、OH-、CO32-和SO42-,对于可能存在的其他阴离子,研究小组提出以下3种假设.假设1:只存在SO32-;假设2:只存在ClO-;假设3:既不存在SO32-,也不存在ClO-.
(5)学习小组判断同时存在SO32-和ClO-是不可能的理由是
(6)现限选以下试剂,设计实验方案,进行实验,请写出实验步骤以及预期现象和结论.
a.3mol/L H2SO4 b.0.01mol/L KMnO4c.1mol/L BaCl2溶液
d.淀粉碘化钾溶液 e.酚酞试液
步骤一;取少量吸收液于试管中,滴加3mol/L H2SO4至溶液呈酸性,然后将所得溶液分装于A、B两试管中.
步骤二:向A试管中滴加少量
步骤三:向B试管中滴加少量
(1)分析某地几年内的降雨成分发现,前些年雨水中阴离子主要以SO2-4离子为主,近几年雨水中
| NO | - 4 |
A.煤烟型
B.机动车尾气型
C.由煤烟型向煤烟型与机动车尾气混合型转化
D.由机动车尾气型向煤烟型与机动车尾气混合型转化
(2)某校研究性学习小组收集到一酸雨样本,他们将样本置于敞口容器中并对样本进行一段时间的pH值测定,其测定结果见下表:
| 测试时间/h | 0 | 1 | 2 | 3 | 4 | 6 | 6 |
| 样本的Ph | 4.93 | 4.72 | 4.63 | 4.58 | 4.56 | 4.55 | 4.55 |
(3)在工业上采用氨法烟气脱硫技术.其做法是用氨吸收烟气中的SO2生成亚硫酸铵和亚硫酸氢铵,再用一定量的磷酸进行反应,在反应回收SO2后的混合手中通入适量的氨气得到一种复合肥.氨水吸收SO2生成亚硫酸铵的化学方程式
(4)为将SO2的污染变废为宝,人们正在探索用CO还原SO2得到单质硫的方法来除去SO2和得到单质硫.该方法涉及到的化学反应有:
A.XSO2+2XCO═2xCO2+Sx
B.xCO+Sx═xCOS
C.2XCOS+xSO2═2xCO2+3Sx
其中属于氧化还原反应的是
(5)含氮氧化物的气体可以用NH3在一定条件下进行处理,变成两种无毒的物质后排放.下列流程是探究不同催化剂对NH3还原NO反应的催化性能.

若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,将经催化反应后的混合气体通过滴有酚酞的稀硫酸溶液(溶液的体积、浓度均相同).为比较不同催化剂的催化性能,需要测量并记录的数据是
①反应开始时两者生成H2的速率 。?
②等物质的量浓度的NaX和NaY溶液的碱性,NaX NaY(填“>”“<”或“=”);理由是:? ?。?
(2)某研究性学习小组的同学,取一定质量纯净的Na2SO3固体,隔绝空气600 ℃以上强热,得固体A,经测定强热前后固体质量保持不变。为进一步证明Na2SO3固体在强热条件下是否分解以及该条件下分解是否完全,他们对A进行如下实验:?

依据实验现象以及质量守恒定律和氧化还原反应的有关规律,他们推测固体A的成分可能是Na2SO4、Na2SO3、Na2S2O3、Na2S和Na2O中的数种,并且提出以下两种假设。?
试回答下列问题:?
假设1:①A溶液碱性比Na2SO3溶液碱性强,是由于生成的Na2S水解所致,则Na2SO3固体分解的化学反应方程式为: 。?
②若气体C是H2S,判断Na2SO3固体分解是否完全 (填“是”或“否”),你判断的理由是: 。?
假设2:③A溶液碱性比Na2SO3溶液碱性强,是由于生成的Na2O溶于水所致,则Na2SO3固体分解的化学反应方程式为:(未平配)?
□Na2SO3——□ Na2S2O3+□ Na2SO4+□ Na2O,请配平该化学反应方程式。?
④为进一步确定何种假设正确,该小组同学查阅有关资料得知,Na2S2O3不稳定,受热易分解,请你帮助判断上述何种假设正确 。?
查看习题详情和答案>>氯气是一种重要的化工原料。某学习小组在实验室中利用下图所示装置制取氯气并探究其性质。
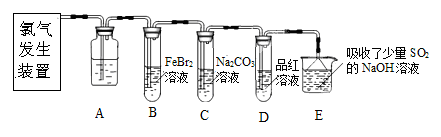
(1)实验室用二氧化锰和浓盐酸加热制取氯气,发生装置中除圆底烧瓶和导管外还需用到的玻璃仪器有
;
(2)装置A中盛有的试剂是 ,作用是 。
(3)若D中品红溶液褪色,则B装置中发生反应的离子方程式是
(4)证明FeBr2与Cl2发生了氧化还原反应的实验方法是 (填操作方法)。
某研究性学习小组用刚吸收过少量SO2的NaOH溶液吸收处理上述实验后的尾气。经分析吸收尾气一段时间后,吸收液(呈强碱性)中肯定存在Cl-、OH-、CO32- 和SO42-,对于可能存在的其他阴离子,研究小组提出以下3种假设。假设1:只存在SO32-;假设2:只存在ClO-;假设3:既不存在SO32-,也不存在ClO-。
(5)学习小组判断同时存在SO32-和ClO-是不可能的理由是 。
38.现限选以下试剂,设计实验方案,进行实验,请写出实验步骤以及预期现象和结论。
a.3 mol/L H2SO4
b.0.01 mol/L KMnO4
c.1 mol/L BaCl2溶液
d.淀粉碘化钾溶液
e.酚酞试液
步骤一;取少量吸收液于试管中,滴加3 mol/L H2SO4至溶液呈酸性,然后将所得溶液分装于A、B
两试管中。
步骤二:向A试管中滴加少量___________ (填序号),若溶液_________________(填现象),则假设
1成立。
步骤三:向B试管中滴加少量___________(填序号),若溶液_________________(填现象),则假设2
成立。
查看习题详情和答案>>