摘要:17.(1)2NH3+H2SO4=(NH4)2SO4 (2)N≡N , (NH4)2SO3或NH4HSO3 (3)ClO-+SO2+2OH-=Cl-++H2O (4)N2H4
网址:http://m.1010jiajiao.com/timu3_id_404469[举报]
A、B、C为短周期元素,在周期表中所处位置如图所示.A、C两元素的原子核外电子数之和等于B原子的质子数.
(1)B位于元素周期表第
(2)A元素形成的单质的电子式为:
 .
.
(3)在A B、C的气态氢化物中最稳定的是
(4)C的离子结构示意图为
 .
.
(5)写出A的气态氢化物与B的最高价氧化物对应水化物反应的化学方程式
查看习题详情和答案>>
| A | C | |
| B |
三
三
周期,第ⅥA
ⅥA
族.(2)A元素形成的单质的电子式为:


(3)在A B、C的气态氢化物中最稳定的是
HF
HF
.(4)C的离子结构示意图为


(5)写出A的气态氢化物与B的最高价氧化物对应水化物反应的化学方程式
2NH3+H2SO4=( NH4)2SO4
2NH3+H2SO4=( NH4)2SO4
.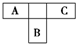 A、B、C为短周期元素,在周期表中所处的位置如图所示.A、C两元素的原子核外电子数之和等于B原子的质子数.B原子核内质子数和中子数相等.
A、B、C为短周期元素,在周期表中所处的位置如图所示.A、C两元素的原子核外电子数之和等于B原子的质子数.B原子核内质子数和中子数相等.(1)写出A、B、C三种元素的名称分别为
氮
氮
、硫
硫
、氟
氟
;(2)B位于元素周期表中第
三
三
周期,第ⅥA
ⅥA
族;(3)C的原子结构示意图为
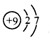
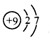
2F2+2H2O═4HF+O2
2F2+2H2O═4HF+O2
;(4)比较B、C的原子半径;B
>
>
C,写出A的气态氢化物与B的最高价氧化物对应水化物反应的化学方程式2NH3+H2SO4═(NH4)2SO4
2NH3+H2SO4═(NH4)2SO4
.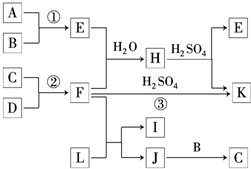 如图是部分短周期元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去).已知:
如图是部分短周期元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去).已知:(a)A、B、C、D都是非金属单质,其中B、C、D在常温常压下是气体.
(b)反应①、②是化工生产中的重要反应.
(c)化合物E是形成酸雨的污染物之一,化合物K是常用的氮肥.
(d)化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得.
(e)化合物J由两种元素组成,它是火箭推进剂的成分之一,其相对分子质量为32.
请按要求填空:
(1)反应③的化学方程式
2NH3+H2SO4═(NH4)2SO4
2NH3+H2SO4═(NH4)2SO4
.(2)C的结构式
N≡N
N≡N
;H的化学式(NH4)2SO3或NH4HSO3
(NH4)2SO3或NH4HSO3
.(3)L的溶液与化合物E反应的离子方程式:
ClO-+SO2+2OH-═Cl-+SO42-+H2O或ClO-+SO2+H2O═Cl-+SO42-+2H+
ClO-+SO2+2OH-═Cl-+SO42-+H2O或ClO-+SO2+H2O═Cl-+SO42-+2H+
.(4)化合物J的化学式
N2H4
N2H4
.某化学课外活动小组设计实验探究氮的化合物的性质,装置如下图所示(A装置未画出),其中A为气体发生装置.A中所用试剂,从下列固体物质中选取:①NH4HCO3、②NH4Cl、③Ca(OH)2、④NaOH.

检查装置气密性后,先将C处铂丝网加热至红热,再将A处产生的气体通过B装置片刻后,撤去C处酒精灯,铂丝继续保持红热,F处铜片逐渐溶解.
(1)实验室制取A中气体时若只用一种试剂,该试剂是
(2)下面关于A中所用试剂的说法正确的是
A.施用该物质会大大提高粮食产量而对环境无影响
B.向该物质的溶液中加入足量氢氧化钡溶液发生反应的离子方程式为:NH4++OH-=NH3?H2O
C.可通过加热方法区别该试剂和(NH4)2SO4
D.工业上用NH3等合成该物质的过程可称为氮的固定
(3)装置C中发生催化氧化反应的化学方程式为
(4)假设A、B中的药品充足,则装置F中可以观察到的现象有
(5)指导老师从安全与环保角度考虑,指出该装置有两处明显的缺陷,请你提出修改建议:
查看习题详情和答案>>

检查装置气密性后,先将C处铂丝网加热至红热,再将A处产生的气体通过B装置片刻后,撤去C处酒精灯,铂丝继续保持红热,F处铜片逐渐溶解.
(1)实验室制取A中气体时若只用一种试剂,该试剂是
NH4HCO3
NH4HCO3
(填代表备选试剂的序号);此时A中主要的玻璃仪器有试管、酒精灯
试管、酒精灯
(填名称).(2)下面关于A中所用试剂的说法正确的是
C
C
.A.施用该物质会大大提高粮食产量而对环境无影响
B.向该物质的溶液中加入足量氢氧化钡溶液发生反应的离子方程式为:NH4++OH-=NH3?H2O
C.可通过加热方法区别该试剂和(NH4)2SO4
D.工业上用NH3等合成该物质的过程可称为氮的固定
(3)装置C中发生催化氧化反应的化学方程式为
4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
,装置E发生反应的化学方程式为
| ||
| △ |
2NH3+H2SO4=(NH4)2SO4
2NH3+H2SO4=(NH4)2SO4
.(4)假设A、B中的药品充足,则装置F中可以观察到的现象有
水中产生气泡
水中产生气泡
溶液逐渐变为蓝色,气体在广口瓶上方变为红棕色
溶液逐渐变为蓝色,气体在广口瓶上方变为红棕色
.(5)指导老师从安全与环保角度考虑,指出该装置有两处明显的缺陷,请你提出修改建议:
在装置E、F之间增加一个防倒吸装置,在装置F后面增加一个尾气吸收装置
在装置E、F之间增加一个防倒吸装置,在装置F后面增加一个尾气吸收装置
.甲、乙、丙三位同学分别用如图所示三套实验装置及化学药品(其中碱石灰为固体氢氧化钠和生石灰的混合物)制取氨气.请你参与探究,并回答下列问题:

(1)三位同学制取氨气的化学方程式为:
(2)三位同学用上述装置制取氨气时,其中有一位同学没有收集到氨气(如果他们的实验操作都正确),你认为没有收集到氨气的同学是
(3)检验氨气是否收集满的方法是
A、闻到有氨气逸出
B、棉花被气体冲出
C、用湿润的红色石蕊试纸在试管口检验,发现试纸变蓝
D、用湿润的蓝色石蕊试纸在试管口检验,发现试纸变红
(4)三位同学都认为他们的实验装置也可用于加热碳酸氢铵固体制取纯净的氨气,你判断能够达到实验目的是
查看习题详情和答案>>

(1)三位同学制取氨气的化学方程式为:
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
| ||
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
.
| ||
(2)三位同学用上述装置制取氨气时,其中有一位同学没有收集到氨气(如果他们的实验操作都正确),你认为没有收集到氨气的同学是
乙
乙
(填“甲”、“乙”或“丙”),收集不到氨气的主要原因是2NH3+H2SO4═(NH4)2SO4
2NH3+H2SO4═(NH4)2SO4
(用化学方程式表示).(3)检验氨气是否收集满的方法是
C
C
A、闻到有氨气逸出
B、棉花被气体冲出
C、用湿润的红色石蕊试纸在试管口检验,发现试纸变蓝
D、用湿润的蓝色石蕊试纸在试管口检验,发现试纸变红
(4)三位同学都认为他们的实验装置也可用于加热碳酸氢铵固体制取纯净的氨气,你判断能够达到实验目的是
丙
丙
(填“甲”、“乙”或“丙”).