摘要:20.在一定密闭容器中加入一定量的X.发生可逆反应: 2X △H=QkJ·mol-1在t1时刻达到平衡.然后在t2时刻开始加热到一定温度后停止加热并保温.到t3时刻又建立平衡.下图能表示这一变化的是 ( )
网址:http://m.1010jiajiao.com/timu3_id_402064[举报]
 向一容积为1L 的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s)?bZ(g);△H<0.如图是容器中X、Z的物质的量浓度随时间变化的曲线.根据以上信息,下列说法正确的是( )
向一容积为1L 的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s)?bZ(g);△H<0.如图是容器中X、Z的物质的量浓度随时间变化的曲线.根据以上信息,下列说法正确的是( )
查看习题详情和答案>>
向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s)  bZ(g);△H<0。右图是容器中X、Z的物质的量浓度随时间变化的曲线。
bZ(g);△H<0。右图是容器中X、Z的物质的量浓度随时间变化的曲线。
根据以上信息,下列说法正确的是
| A.用X表示0~10min内该反应的平均速率为v(X)=0.045mol/L·min |
| B.根据上图可求得方程式中a:b= 1:3, |
| C.推测在第7min时曲线变化的原因可能是升温 |
| D.推测在第13min时曲线变化的原因可能是降温 |
向一容积为1L 的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s)  bZ(g);△H<0。右图是容器中X、Z的物质的量浓度随时间变化的曲线。
bZ(g);△H<0。右图是容器中X、Z的物质的量浓度随时间变化的曲线。
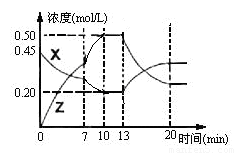
根据以上信息,下列说法正确的是
A.用X表示0~10min内该反应的平均速率为v(X)=0.045mol/L·min
B.根据上图可求得方程式中a:b= 1:3,
C.推测在第7min时曲线变化的原因可能是升温
D.推测在第13min时曲线变化的原因可能是降温
查看习题详情和答案>>
向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s) bZ(g)
bZ(g)
 。下图是容器中X、Z的物质的量浓度随时间变化的曲线。
。下图是容器中X、Z的物质的量浓度随时间变化的曲线。
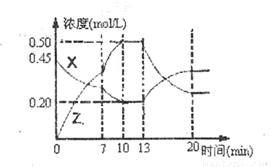
根据以上信息判断,下列说法中正确的是 ( )
A.用X表示0~10 min内该反应的平均速率为v(x)=0.045mol/(L·min)
B.化学方程式中a:b=1:3
C.推测在第7min时曲线变化的原因可能是升温
D.推测在第13min时该反应刚好达到化学平衡
查看习题详情和答案>>
向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s)  bZ(g) △H<0。下图是容器中X、Z的物质的量浓度随时间变化的曲线。
bZ(g) △H<0。下图是容器中X、Z的物质的量浓度随时间变化的曲线。
根据以上信息判断,下列说法中正确的是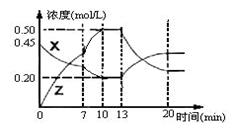
| A.用X表示0~10min内该反应的平均速率为v(X)=0.045mol/(L·min) |
| B.化学方程式中a:b= 1:3, |
| C.推测在第7min时曲线变化的原因可能是增加X的浓度 |
| D.推测该反应处于化学平衡状态的时间是10min--13min及第20min 后 |