网址:http://m.1010jiajiao.com/timu3_id_399971[举报]
 氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点.
氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点.(1)直接热分解法制氢.某温度下,H2O(g)?H2(g)+
| 1 |
| 2 |
c(H2)c
| ||
| c(H2O) |
c(H2)c
| ||
| c(H2O) |
(2)热化学循环制氢.制备H2的反应步骤如下:
①Br2(g)+CaO(s)═CaBr2(s)+
| 1 |
| 2 |
②3FeBr2(s)+4H2O(g)═Fe3O4(s)+6HBr(g)+H2(g)△H=+384kJ?mol-1
③CaBr2(s)+H2O (g)═CaO(s)+2HBr(g)△H=+212kJ?mol-1
④Fe3O4(s)+8HBr(g)═Br2(g)+3FeBr2(s)+4H2O(g)△H=-274kJ?mol-1
则 H2O(g)?H2(g)+
| 1 |
| 2 |
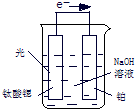
(3)光电化学分解制氢,其原理如图.钛酸锶光电极的电极反应为4OH--4e-═O2+2H2O,则铂电极的电极反应为
(4)水煤气法制氢.
CO(g)+H2O(g)?CO2(g)+H2(g)△H<0,在850℃时,K=1.
①若升高温度到950℃时,达到平衡时K
②850℃时,若向一容积可变的密闭容器中同时充入1.0mol CO、3.0mol H2O、1.0mol CO2 和x mol H2,若要使上述反应开始时向正反应方向进行,则x应满足的条件是
(5)甲烷制氢.将1.0mol CH4和2.0mol H2O (g)通入容积为100L的反应室,在一定条件下发生反应:CH4(g)+H2O(g)═CO(g)+3H2(g).测得达到平衡所需的时间为5min,CH4的平衡转化率为50%,则用H2表示该反应的平均反应速率为
(6)LiBH4具有非常高的储氢能力,分解时生成氢化锂和两种非金属单质.该反应的化学方程式为
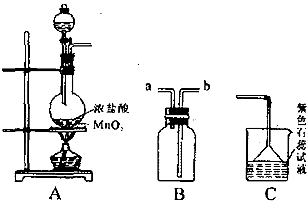
(1)装置A发生反应的离子方程式为
| ||
| ||
(2)装置 B 如图所示放置,则连接 A 的导管口是(填管口字母)
(3)实验中可观察到C 处石蕊试液的现象是
(4)取出 B 中的集气瓶进行氯气与铜的燃烧实验:首先进行的操作是
(5〕Cl2可与甲苯在光照条件下反应生成一氯甲苯,一氯甲苯进一步水解,可得某种香精的原料苯甲醇.为了获得较纯的一氯甲苯,同时回收未反应的甲苯应采用
A.分液漏斗 B.酒精灯 C.铁架台 D.蒸馏烧瓶 E.短颈漏斗 F.水冷凝管
G.玻璃捧 H.温度计 I.尾接管 J.烧杯 K.锥形瓶.
原电池、电解(电镀)池是化学反应利用方面的典型事例,体现出能量之间的转换,受到越来越多的关注。按要求回答下列各个问题。
(1)南昌大学最近研发出一种新型纳米锂电池,已跻身国内领先地位。锂离子电池的正极材料是锂过渡金属氧化物(例如LiCoO2)混以一定量的导电添加物(例如C)构成的混合导体,负极材料是可插入锂的碳负极。两极的电极反应式:
负极:![]() 正极:
正极:![]() 。
。
充、放电时电池中的变化简单表示为:![]() (a、b、c、d表示充放电过程)。其中表示充电时阴极发生变化的过程是 (填a、b、c、d),判断理由是 。
(a、b、c、d表示充放电过程)。其中表示充电时阴极发生变化的过程是 (填a、b、c、d),判断理由是 。
(2)在正负极之间是固体电解质。固体电解质又称离子导体,在一定温度范围内具有很强的导电性。固体电解质虽然是固体,但却像电解质溶液一样为离子的导电载体。下列物质能作为固体电解质的是 (填编号)。
①特种钢;②硝酸钾晶体;③银;④高纯度硅。
(3)实验室中用该类电池在铁棒上镀铜,当有lmol电子发生转移时,则正极产生物质的质量为 g。
(4)为了使产品更耐腐蚀和美观,通常采用电镀的方式,但随之而来的是污染问题。某电镀厂处理有氰电镀的废水时,用Ti02作催化剂,用NaCl0将CN-离子氧化成CNO-,CNO-在酸性条件下继续被NaClO氧化成N2和C02;用如图装置实验,通过测定二氧化碳的量确定CN-的含量。将浓缩后含CN-离子200mL的污水与过量NaClO溶液的混合液,倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶液全部放入乙中,关闭活塞。
①甲中反应的离子方程式为_____________

②乙中除生成N2和C02外,还有HCl及副产物Cl2等。在上述装置中HCl和C12是如何被除掉的?______。
③实验后得到0.4吧沉淀,则浓缩后的污水中CN-的含量为 g/L。
查看习题详情和答案>>