摘要:19.现取下列混合物各12.0g.不管混合物中各成分的含量比例如何变化.完全燃烧 后均得到17.6g CO2的可能是 ( ) A.苯.1-己块 B.乙醇.乙醚 C.葡萄糖.甲酸甲酯 D.乙酸.甲醛 20?下列各组中的两种物质相互反应时.不论哪种物质过量.都可用同一个离子方 程式表示的是 ( ) A.偏铝酸钠溶液与盐酸 B.苯酚钠溶液与二氧化碳 C.氯化铝溶液与氨水 D.烧碱溶液与二氧化硫
网址:http://m.1010jiajiao.com/timu3_id_399918[举报]
今有一混合物的水溶液,可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份各200mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液无沉淀产生,加热后,收集到气体0.06mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量变为4.66g.
根据上述实验,下列推测正确的是( )
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液无沉淀产生,加热后,收集到气体0.06mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量变为4.66g.
根据上述实验,下列推测正确的是( )
| A、依据电荷守恒,推测一定存在K+和NH4+ | B、200mL溶液中含0.02mol CO32- | C、Ba2+一定不存在,Mg2+可能存在 | D、4.66g沉淀中含BaCO3和BaSO4 |
某固体混合物中,可能含有下列离子中的几种:K+、NH4+、Mg2+、Ba2+、Cl-、SO42-、CO32-,将该混合物溶于水后得澄清溶液,现取三份各100 mL该溶液分别进行如下实验:
(1)在一份溶液中加入AgNO3溶液,有白色沉淀生成;
(2)在另一份溶液中加入足量的NaOH溶液并加热,收集到1.12 L气体(标准状 况下);
(3)在第三份溶液中加入足量的BaCl2溶液有沉淀生成,经称量其质量为6.27 g,在该沉淀中加入足量的盐酸,沉淀部分溶解,剩余固体质量为2. 33 g。
根据上述实验回答下列问题:
①溶液中一定不存在的离子是_____________;
②溶液中一定存在的阴离子有___________,其物质的量浓度分别为___________,
③推断K+是否存在并说理由:_____________。
查看习题详情和答案>>
(1)在一份溶液中加入AgNO3溶液,有白色沉淀生成;
(2)在另一份溶液中加入足量的NaOH溶液并加热,收集到1.12 L气体(标准状 况下);
(3)在第三份溶液中加入足量的BaCl2溶液有沉淀生成,经称量其质量为6.27 g,在该沉淀中加入足量的盐酸,沉淀部分溶解,剩余固体质量为2. 33 g。
根据上述实验回答下列问题:
①溶液中一定不存在的离子是_____________;
②溶液中一定存在的阴离子有___________,其物质的量浓度分别为___________,
③推断K+是否存在并说理由:_____________。
(1)某同学为探究蔗糖的水解反应,进行如下实验,填写实验步骤III的实验现象:
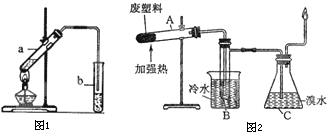
(2)“酒是陈的香”的原因之一是储存过程中生成了有香味的酯.实验室用下图所示装置制取乙酸乙酯.
①试管a中生成乙酸乙酯的化学反应方程式是 .
②试管b中盛放的试剂是 溶液
③若要把b中制得的乙酸乙酯从混合物中分离出来,应采用的实验操作是 .
④生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,也即达到化学平衡状态.下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号) .
a单位时间里,生成1mol乙酸乙酯,同时生成1mol水
b单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
c单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
d正反应的速率与逆反应的速率相等
e混合物中各物质的浓度不再变化
(3)加热聚丙烯塑料得到的产物如表:
实验装置如图所示.
①试管A中的最终残余物为 ;
②试管B收集到的产品中,有能使酸性高锰酸钾溶液褪色的物质,该物质的一氯代物有 种.
③锥形瓶C中观察到的现象是 ;经溴水充分吸收再干燥后,剩余两种气体的平均相对分子质量为 .
查看习题详情和答案>>

| 实验步骤 | 实验现象 |
| I.向编号为①②③的3支试管中,分别加入1mL 20%的蔗糖溶液,向试管②和③中加入0.5mL稀硫酸,并将这3支试管同时水浴加热约5min | 均无明显现象 |
| II.取试管①和②,加入新制氢氧化铜悬浊液,加热至沸腾 | 均无明显现象 |
| III.取试管③,先加入NaOH溶液调溶液pH至碱性,再加入新制氢氧化铜悬浊液,加热至沸腾 | |
| 结论:证明蔗糖在稀硫酸作用下发生了水解反应 | |
①试管a中生成乙酸乙酯的化学反应方程式是
②试管b中盛放的试剂是
③若要把b中制得的乙酸乙酯从混合物中分离出来,应采用的实验操作是
④生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,也即达到化学平衡状态.下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号)
a单位时间里,生成1mol乙酸乙酯,同时生成1mol水
b单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
c单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
d正反应的速率与逆反应的速率相等
e混合物中各物质的浓度不再变化
(3)加热聚丙烯塑料得到的产物如表:
| 产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
| 质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |
①试管A中的最终残余物为
②试管B收集到的产品中,有能使酸性高锰酸钾溶液褪色的物质,该物质的一氯代物有
③锥形瓶C中观察到的现象是
(10分)由几种化合物组成的混合物,含有以下离子中的若干种:K+、Cl-、NH4+、Mg2+、CO32-、Ba2+、SO42-。将该混合物溶于水后得澄清溶液,现各取三份100 mL该溶液分别进行如下实验:
| 实验序号 | 实验内容 | 实验结果 |
| 1 | 加入AgNO3溶液 | 有白色沉淀生成 |
| 2 | 加足量NaOH溶液并加热 | 收集到气体1.12 L (标准状况下) |
| 3 | 加足量BaCl2溶液时,对所得沉淀进行洗涤、干燥、称量,再向沉淀中加入足量稀盐酸,然后干燥、称量 | 第一次称量读数为6.27 g, 第二次称量读数为2.33 g |
(1)根据实验1对Cl-是否存在的判断是 (填“一定存在”、“一定不存在”或“不能确定”),根据实验1~3判断混合物中一定不存在的离子是 。
(2)试确定溶液中一定存在的阴离子及其物质的量浓度(可不填满)。
| 阴离子符号 | 物质的量浓度(mol·L-1) |
| | |
| | |
| | |
。 查看习题详情和答案>>
(10分)由几种化合物组成的混合物,含有以下离子中的若干种:K+、Cl-、NH4+、Mg2+、CO32-、Ba2+、SO42-。将该混合物溶于水后得澄清溶液,现各取三份100 mL该溶液分别进行如下实验:
|
实验序号 |
实验内容 |
实验结果 |
|
1 |
加入AgNO3溶液 |
有白色沉淀生成 |
|
2 |
加足量NaOH溶液并加热 |
收集到气体1.12 L (标准状况下) |
|
3 |
加足量BaCl2溶液时,对所得沉淀进行洗涤、干燥、称量,再向沉淀中加入足量稀盐酸,然后干燥、称量 |
第一次称量读数为6.27 g, 第二次称量读数为2.33 g |
试回答下列问题:
(1)根据实验1对Cl-是否存在的判断是 (填“一定存在”、“一定不存在”或“不能确定”),根据实验1~3判断混合物中一定不存在的离子是 。
(2)试确定溶液中一定存在的阴离子及其物质的量浓度(可不填满)。
|
阴离子符号 |
物质的量浓度(mol·L-1) |
|
|
|
|
|
|
|
|
|
(3)试确定K+是否存在 (填“存在” 或“不存在”),判断的理由是
。
查看习题详情和答案>>