摘要:3.某含硫元素的氧化物中.硫元素与氧元素的质量比1:1.该氧化物中硫元素的化合价为: ( ) A.+2 B.+3 C.+4 D.+1
网址:http://m.1010jiajiao.com/timu3_id_3961712[举报]
氢氧化铜固体受热分解能得到两种氧化物,一种为固体,另一种是无色液体.某化学活动小组为确定这种固体产物是什么,进行了如下探究活动.
【假设】:
生成的固体产物:①可能是氧化亚铜(Cu2O)(红色);②可能是 .
【设计实验】:
小明用氢氧化钠溶液与硫酸铜溶液反应制得氢氧化铜,放入试管中,使其在加热条件下分解(如图),观察到蓝色粉末逐渐变成黑色.
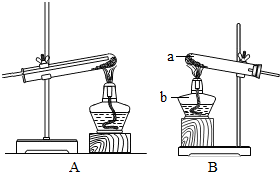
请指出仪器名称:a ,b .【推测结论】:猜想 成立.
【形成结论】:
写出氢氧化铜受热分解的化学方程式: .
【查阅资料】
已知:(1)此黑色固体可用氢气还原,则小明选择下列 装置进行实验;
(2)已知Cu2O有如下性质:Cu2O+H2SO4═Cu+CuSO4+H2O,在用氢气还原黑色固体后得到的铜中常混有少量Cu2O,取此Cu和Cu2O的混合物共10g放入足量的稀硫酸中充分反应,过滤得9.5g固体,则此混合物中Cu2O的质量分数为 .
【拓展与思考】:小华也用氢氧化钠溶液与硫酸铜溶液反应,但得到的沉淀不呈蓝色,而是浅绿色的;他又将此浊液加热直至沸腾,观察不到有分解变黑的迹象.为什么?小华查找资料得知,该浅绿色沉淀物是溶解度极小的碱式硫酸铜,其化学式为Cu4(OH)6SO4,同时还生成硫酸钠;此浅绿色沉淀能与酸反应,形成蓝色溶液.则碱式硫酸铜中铜元素的化合价为 ,请帮小华写出生成浅绿色沉淀的有关反应的化学方程式: .
小华想设计一个实验,证明该浅绿色沉淀中含有硫酸根,于是将沉淀过滤、洗涤,把沉淀再溶解在足量的无色溶液A中,取所得溶液滴加无色溶液B,若有大量白色沉淀生成,则表示原浅绿色沉淀中有SO42-,试推测:(1)无色溶液A的化学式是 ,无色溶液B的化学式是 ;
(3)写出产生白色溶液的化学方程式 .
查看习题详情和答案>>
【假设】:
生成的固体产物:①可能是氧化亚铜(Cu2O)(红色);②可能是
【设计实验】:
小明用氢氧化钠溶液与硫酸铜溶液反应制得氢氧化铜,放入试管中,使其在加热条件下分解(如图),观察到蓝色粉末逐渐变成黑色.

请指出仪器名称:a
【形成结论】:
写出氢氧化铜受热分解的化学方程式:
【查阅资料】
已知:(1)此黑色固体可用氢气还原,则小明选择下列
(2)已知Cu2O有如下性质:Cu2O+H2SO4═Cu+CuSO4+H2O,在用氢气还原黑色固体后得到的铜中常混有少量Cu2O,取此Cu和Cu2O的混合物共10g放入足量的稀硫酸中充分反应,过滤得9.5g固体,则此混合物中Cu2O的质量分数为
【拓展与思考】:小华也用氢氧化钠溶液与硫酸铜溶液反应,但得到的沉淀不呈蓝色,而是浅绿色的;他又将此浊液加热直至沸腾,观察不到有分解变黑的迹象.为什么?小华查找资料得知,该浅绿色沉淀物是溶解度极小的碱式硫酸铜,其化学式为Cu4(OH)6SO4,同时还生成硫酸钠;此浅绿色沉淀能与酸反应,形成蓝色溶液.则碱式硫酸铜中铜元素的化合价为
小华想设计一个实验,证明该浅绿色沉淀中含有硫酸根,于是将沉淀过滤、洗涤,把沉淀再溶解在足量的无色溶液A中,取所得溶液滴加无色溶液B,若有大量白色沉淀生成,则表示原浅绿色沉淀中有SO42-,试推测:(1)无色溶液A的化学式是
(3)写出产生白色溶液的化学方程式
下图中,A是含淀粉类粮食经过发酵、蒸馏而得到的一种可再生能源,反应③常用于实验室检验二氧化碳.
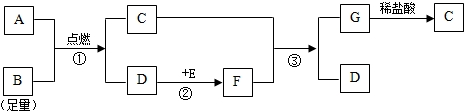
(1)反应①的化学方程式为 ,A物质中碳元素的化合价为 .
(2)反应③的化学方程式为 .
(3)D物质发生分解反应的化学方程式为 .
(4)A也是一种常见溶剂,密度比水小,A和浓硫酸相互混合时表现出的现象与用水稀释浓硫酸相似,A与浓硫酸的混合物可用来制取多种有机物.某同学需要用两只量筒分别量取50mL的A和150mL的浓硫酸,他应该选用的两只量筒依次为 (选填序号).
A.10mL量筒 B.50mL量筒 C. 100mL量筒 D.250mL量筒
为了混合A和浓硫酸,他应该先在500mL的烧杯中倒入 (选填“A”或“浓硫酸”),然后 .
查看习题详情和答案>>

(1)反应①的化学方程式为
(2)反应③的化学方程式为
(3)D物质发生分解反应的化学方程式为
(4)A也是一种常见溶剂,密度比水小,A和浓硫酸相互混合时表现出的现象与用水稀释浓硫酸相似,A与浓硫酸的混合物可用来制取多种有机物.某同学需要用两只量筒分别量取50mL的A和150mL的浓硫酸,他应该选用的两只量筒依次为
A.10mL量筒 B.50mL量筒 C. 100mL量筒 D.250mL量筒
为了混合A和浓硫酸,他应该先在500mL的烧杯中倒入
单质和氧化物化学式的书写:
查看习题详情和答案>>
| 物质类别 | 物质名称 | 化学式 | 我的发现(书写规则与读法) | |
| 单质 | 金属单质 | 钠、钾、铝、铜 | Na、K、Al、Cu Na、K、Al、Cu |
习惯上用元素符号表示,读元素符号的名称 习惯上用元素符号表示,读元素符号的名称 |
| 非金属单质 | 碳、硫、磷、硅 | C、S、P、Si C、S、P、Si |
习惯上用元素符号表示,读元素符号的名称 习惯上用元素符号表示,读元素符号的名称 | |
| 氧气、氮气、氯气 | O2、N2、Cl2 O2、N2、Cl2 |
在元素符号右下角写上表示分子中所含原子数的数字,读作“某气” 在元素符号右下角写上表示分子中所含原子数的数字,读作“某气” | ||
| 稀有气体单质 | 氦气、氖气、氩气 | He、Ne、Ar He、Ne、Ar |
用元素符号表示,读作“某气”. 用元素符号表示,读作“某气”. | |
| 氧化物 | 二氧化碳、二氧化锰、四氧化三铁 | CO2、MnO2、Fe3O4 CO2、MnO2、Fe3O4 |
一般把氧的元素符号写在右方,另一种元素符号写在左方.一般是从右到左读,读作“某化某”,有时还要读出各种元素的原子个数. 一般把氧的元素符号写在右方,另一种元素符号写在左方.一般是从右到左读,读作“某化某”,有时还要读出各种元素的原子个数. | |
下图中,A是含淀粉类粮食经过发酵、蒸馏而得到的一种可再生能源,反应③常用于实验室检验二氧化碳.

(1)反应①的化学方程式为______,A物质中碳元素的化合价为______.
(2)反应③的化学方程式为______.
(3)D物质发生分解反应的化学方程式为______.
(4)A也是一种常见溶剂,密度比水小,A和浓硫酸相互混合时表现出的现象与用水稀释浓硫酸相似,A与浓硫酸的混合物可用来制取多种有机物.某同学需要用两只量筒分别量取50mL的A和150mL的浓硫酸,他应该选用的两只量筒依次为______(选填序号).
A.10mL量筒 B.50mL量筒 C. 100mL量筒 D.250mL量筒
为了混合A和浓硫酸,他应该先在500mL的烧杯中倒入______(选填“A”或“浓硫酸”),然后______.
查看习题详情和答案>>
 下表是元素周期表的部分信息,请回答下列问题:
下表是元素周期表的部分信息,请回答下列问题:| 1H 氢 |
2He 氦 | |||||||
| 3Li 锂 |
4Be 铍 |
5B 硼 |
6C 碳 |
7N 氮 |
8O 氧 |
9F 氟 |
10Ne 氖 | |
| llNa 钠 |
12Mg 镁 |
13A1 铝 |
14Si 硅 |
15P 磷 |
16S 硫 |
17C1 氯 |
18Ar 氩 | |
| 19K 钾 |
xCa 钙 |
… | ||||||
8
8
(2)分析上表可发现:每一横行元素从左向右排列所遵循的一条规律是
质子数递增
质子数递增
每一列从上到下所遵循的一条规律是电子层数递增
电子层数递增
(最后一列除外)(3)图甲是某元素在元素周期表中的部分信息,图乙是该元素的一种粒子结构示意图.
①该元素的原子的核电荷数为
16
16
,相对原子质量是32.06
32.06
,该元素的化学性质与表中氧
氧
元素的化学性质最相似.②图乙所示粒子的符号为
S2-
S2-
,该元素与钠元素形成的物质化学式为Na2S
Na2S
.