摘要:19.某化肥厂以氨和空气(其中氧气的体积分数为0.2)为原料生产硝酸铵过程如下: 其中反应①为4NH3+5O24NO+6H2O ⑴步骤②中发生了两个反应.将这两个化学方程式合并为一个化学方程式.可表示为 . ⑵若不考虑副反应且各步反应均完全.为使生产过程中不再补充空气.则原料气中氨(包括第③步被硝酸吸收的氨)的体积分数最大值为 . ⑶假设实际生产中.反应①.②中含氮物质的利用率分别为a.b.反应③中氨的利用率为c.硝酸的利用率为100%.则合成硝酸铵的整个流程中.氨的总利用率是多少?
网址:http://m.1010jiajiao.com/timu3_id_394098[举报]
你留意过标签上的化学吗?
(1)这是某品牌休闲西服标签上的部分内容:
回答 ①其中属于合成纤维的是
②从此标签中可感觉羊毛、绦纶两种纤维的共同点有
③将面料、里料中各抽出一根来点燃,可观察到的现象是
(2)某化肥厂生产的一种化肥,其包装袋上标有:
①该厂生产的每一袋这种化肥中NH4NO3的质量应不少于
②某些汽车的安全气囊中也装有NH4NO3,它在高温或猛烈撞击时,会迅速反应,产生大量气体,从而避免驾驶员受伤.其原理是:2NH4NO3=2N2↑+O2↑+4H2O↑,在使用此化肥时,你最想关照农民大哥的事情是
查看习题详情和答案>>
(1)这是某品牌休闲西服标签上的部分内容:
| 等级:特级 成份:面料 羊毛80% 绦纶20% 里料 绦纶100% |
 |
| 熨烫标准:中温,不超过150℃ |
绦纶
绦纶
②从此标签中可感觉羊毛、绦纶两种纤维的共同点有
不耐高温,有可燃性
不耐高温,有可燃性
.③将面料、里料中各抽出一根来点燃,可观察到的现象是
羊毛灼烧时有烧焦羽毛的气味,而绦纶无此现象
羊毛灼烧时有烧焦羽毛的气味,而绦纶无此现象
.(2)某化肥厂生产的一种化肥,其包装袋上标有:
| 硝酸铵(NH4NO3) 净重 50kg 含氮量≥31.5% |
 |
45
45
kg.②某些汽车的安全气囊中也装有NH4NO3,它在高温或猛烈撞击时,会迅速反应,产生大量气体,从而避免驾驶员受伤.其原理是:2NH4NO3=2N2↑+O2↑+4H2O↑,在使用此化肥时,你最想关照农民大哥的事情是
若化肥结块,不能用硬器敲击
若化肥结块,不能用硬器敲击
、不要与草木灰等碱性物质共施
不要与草木灰等碱性物质共施
(至少说出两点).(2011?宁波模拟)一种“人工固氮”的新方法是在光照条件下,N2在催化剂表面与水蒸气发生反应生成NH3和氧气. 已知:
(1)请根据以上信息,写出“人工固氮”新方法的热化学方程式:
(2)进一步研究NH3生成量与温度的关系,部分实验数据见下表(反应时间3h):
①50℃时从开始到3h内以O2物质的量浓度变化表示的平均反应速率为
②与目前广泛应用的工业合成氨方法相比,该方法中固氮反应速率慢.请提出可提高其反应速率且增大NH3生成量的建议(请写出两条)
(3)氨是氮肥工业的重要原料.某化肥厂生产铵态氮肥(NH4)2SO4的工业流程如下:
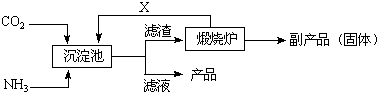
①往沉淀池中装入CaSO4悬浊液后,需先通入足量NH3,再通入CO2的原因是
②煅烧炉中产生的固态副产品为
查看习题详情和答案>>
| 化学键 | N≡N | H-O | N-H | O=O |
| 键能/kJ?mol-1 | 945 | 463 | 391 | 498 |
N2(g)+3H2O(g) 2NH3(g)+
2NH3(g)+
O2(g);△H=+630kJ?mol-1
 2NH3(g)+
2NH3(g)+| 3 |
| 2 |
N2(g)+3H2O(g) 2NH3(g)+
2NH3(g)+
O2(g);△H=+630kJ?mol-1
; 2NH3(g)+
2NH3(g)+| 3 |
| 2 |
(2)进一步研究NH3生成量与温度的关系,部分实验数据见下表(反应时间3h):
| T/℃ | 30 | 40 | 50 |
| 生成NH3量/(10-6mol/L) | 4.8 | 5.9 | 6.0 |
1.5×l0-6mol/(L?h)(或2.5×l0-8mol/(L?min)
1.5×l0-6mol/(L?h)(或2.5×l0-8mol/(L?min)
;②与目前广泛应用的工业合成氨方法相比,该方法中固氮反应速率慢.请提出可提高其反应速率且增大NH3生成量的建议(请写出两条)
升高温度
升高温度
、增大压强
增大压强
;(3)氨是氮肥工业的重要原料.某化肥厂生产铵态氮肥(NH4)2SO4的工业流程如下:

①往沉淀池中装入CaSO4悬浊液后,需先通入足量NH3,再通入CO2的原因是
氨在水中溶解度大,使溶液呈碱性,有利于吸收CO2,增大c(CO32-),促使CaSO4转化为CaCO3,同时生成(NH4)2SO4
氨在水中溶解度大,使溶液呈碱性,有利于吸收CO2,增大c(CO32-),促使CaSO4转化为CaCO3,同时生成(NH4)2SO4
.②煅烧炉中产生的固态副产品为
CaO(或生石灰)
CaO(或生石灰)
,生产流程中能被循环利用的物质X为CO2(或二氧化碳)
CO2(或二氧化碳)
.
某化肥厂以氨和空气(其中氧气的体积分数为0.2)为原料生产硝酸铵过程如下:
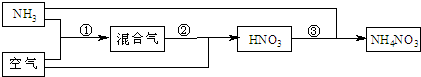
其中反应①为4NH3+5O2
4NO+6H2O
(1)步骤②中发生了两个反应,将这两个化学方程式合并为一个化学方程式,可表示为 .
(2)若不考虑副反应且各步反应均完全,为使生产过程中不再补充空气,则原料气中氨(包括第③步被硝酸吸收的氨)的体积分数最大值为 .
(3)假设实际生产中,反应①、②中含氮物质的利用率分别为a、b,反应③中氨的利用率为c、硝酸的利用率为100%,则合成硝酸铵的整个流程中,氨的总利用率是多少? .
查看习题详情和答案>>

其中反应①为4NH3+5O2
| ||
(1)步骤②中发生了两个反应,将这两个化学方程式合并为一个化学方程式,可表示为
(2)若不考虑副反应且各步反应均完全,为使生产过程中不再补充空气,则原料气中氨(包括第③步被硝酸吸收的氨)的体积分数最大值为
(3)假设实际生产中,反应①、②中含氮物质的利用率分别为a、b,反应③中氨的利用率为c、硝酸的利用率为100%,则合成硝酸铵的整个流程中,氨的总利用率是多少?
【化学-化学与技术】
化学肥料在农业生产中有重要作用.农业生产中,大量施用的化肥主要是氮肥、磷肥、钾肥.
(1)普钙是磷肥,它的有效成分是 (写化学式).
(2)尿素是一种含氮量较高的氮肥,工业生产尿素是将氨气与二氧化碳在加压、加热的条件下反应生成氨基甲酸铵(H2NCOONH4),再使氨基甲酸铵脱水得到尿素.反应的化学方程式为 、 .
(3)某化肥厂用NH3制备NH4NO3,已知由NH3制NO的产率是96%、NO制HNO3的产率是92%,则制HNO3所用云NH3的质量占耗用全部NH3质量的 %.
(4)合成氨气是生产氮肥的重要环节.合成氨生产简易流程示意图如下:

从示意图可知其存在循环操作.简要说明为什么在化工生产中经常采用循环操作 .合成氨的反应需在500℃进行,其主要原因是 .
查看习题详情和答案>>
化学肥料在农业生产中有重要作用.农业生产中,大量施用的化肥主要是氮肥、磷肥、钾肥.
(1)普钙是磷肥,它的有效成分是
(2)尿素是一种含氮量较高的氮肥,工业生产尿素是将氨气与二氧化碳在加压、加热的条件下反应生成氨基甲酸铵(H2NCOONH4),再使氨基甲酸铵脱水得到尿素.反应的化学方程式为
(3)某化肥厂用NH3制备NH4NO3,已知由NH3制NO的产率是96%、NO制HNO3的产率是92%,则制HNO3所用云NH3的质量占耗用全部NH3质量的
(4)合成氨气是生产氮肥的重要环节.合成氨生产简易流程示意图如下:

从示意图可知其存在循环操作.简要说明为什么在化工生产中经常采用循环操作