摘要:4.⑴ 漏斗.玻璃棒.烧杯 低温蒸发结晶 ⑵ (如图或其 他能防止氨气倒吸的装置) ⑶ 冷凝管 ⑷ ① 吸水 ② 2CaSO4 2CaO+2SO2↑+O2↑ ③ 75.6% (第⑴小题每空1分.其余每空2分.本题共12分)
网址:http://m.1010jiajiao.com/timu3_id_393719[举报]
物质分离的三类操作
(1)过滤和蒸发(分别如图1、图2所示)

过滤是将
________分离的一种方法.如粗盐提纯、氯化钾和二氧化锰的分离.过滤时应注意:①一贴:将滤纸折叠好放入漏斗,加少量蒸馏水润湿,使滤纸紧贴漏斗内壁;②二低:滤纸边缘应略低于漏斗边缘,加入漏斗中液体的液面应略低于滤纸的边缘;③三靠:向漏斗中倾倒液体时,烧杯的夹嘴应与玻璃棒接触,玻璃棒的底端应和三层滤纸处轻轻接触,漏斗颈的末端应与接受器的内壁相接触.蒸发是将
________的方法,结晶是溶质从溶液中析出晶体的过程.该方法可以用来分离和提纯几种可溶性的固体混合物.结晶的原理是________,从而使晶体析出.加热蒸发皿使溶液蒸发时,要用玻璃棒不断搅动溶液,原因是________.当蒸发皿中出现较多的固体时要停止加热.(2)蒸馏和萃取(分别如图3、图4所示)

这两种方法主要用于液体间的分离.
蒸馏和分馏用于分离
________.如蒸馏水的制备、酒精和水的分离、从普通白酒中提取无水酒精等.在蒸馏时,要用石棉网,目的是________;使用碎瓷片是要________;温度计的水银球不能插入液体中,而要与支管口持平,以测量________的温度;冷凝器中水的流向是________,防止因水流不匀(或水流中出现气泡)而使冷凝管炸裂,且冷凝充分.萃取的原理是
________.萃取剂的选择原则是:①与原溶液中的溶剂互不相溶、互不反应,且密度相差较大;②溶质在萃取剂中的溶解度大于在原溶剂中的溶解度;③溶质与萃取剂易于分离.如用CCl4从碘水中提取碘.萃取后的溶液,我们一般要结合分液操作.分液是将________液体混合物进行分离的方法.如汽油和水的分离.(3)洗气(如图5所示)
洗气常用于气体混合物的分离、除杂.根据气体性质的不同,我们可以将气体通过盛有一定除杂试剂的洗气瓶或干燥管,如实验室制备氯气时一般利用盛有饱和食盐水、浓硫酸的洗气瓶分别除去氯化氢、水蒸气.

(2008?揭阳一模)最近,我国利用生产磷铵排放的废渣磷石膏制取硫酸并联产水泥的技术研究获得成功.具体生产流程如下: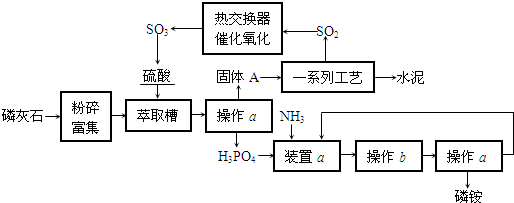
回答下列问题:
(1)若操作a、操作b均在实验室进行,则操作a时用到的玻璃仪器有
(2)装置a用磷酸吸收NH3.若该过程在实验室中进行,请画出装置a的示意图.
(3)热交换器是实现冷热交换的装置.化学实验中也经常利用热交换来实现某种实验目的,如气、液热交换时通常使用的仪器是
(4)固体A为生石膏(CaSO4?2H2O)和不含结晶水且高温时也不分解的杂质.生石膏在120℃时失水生成熟石膏(2CaSO4?H2O),熟石膏在200℃时失水生成硫酸钙.为测定固体A中生石膏的含量,某科研小组进行了如下实验:称取固体A 180g置于坩埚中加热,加热过程中固体质量随温度变化记录如图:实验中每次对固体称量时须在冷却后进行.为保证实验结果的精确性,固体冷却时必须防止
查看习题详情和答案>>

回答下列问题:
(1)若操作a、操作b均在实验室进行,则操作a时用到的玻璃仪器有
漏斗、玻璃棒、烧杯
漏斗、玻璃棒、烧杯
;进行操作b时需注意低温蒸发结晶
低温蒸发结晶
.(2)装置a用磷酸吸收NH3.若该过程在实验室中进行,请画出装置a的示意图.
(3)热交换器是实现冷热交换的装置.化学实验中也经常利用热交换来实现某种实验目的,如气、液热交换时通常使用的仪器是
冷凝管
冷凝管
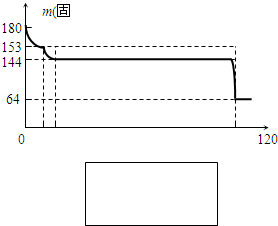
.(4)固体A为生石膏(CaSO4?2H2O)和不含结晶水且高温时也不分解的杂质.生石膏在120℃时失水生成熟石膏(2CaSO4?H2O),熟石膏在200℃时失水生成硫酸钙.为测定固体A中生石膏的含量,某科研小组进行了如下实验:称取固体A 180g置于坩埚中加热,加热过程中固体质量随温度变化记录如图:实验中每次对固体称量时须在冷却后进行.为保证实验结果的精确性,固体冷却时必须防止
吸水
吸水
.将加热到1400℃时生成的气体通入品红溶液中,品红褪色.写出1400℃时的化学反应方程式2CaSO4
2CaO+2SO2↑+O2↑
| ||
2CaSO4
2CaO+2SO2↑+O2↑
.③固体A中生石膏的质量分数=
| ||
95.6%
95.6%
.
 在中学化学实验中,通常用无水硫酸铜检验少量水的存在.由于无水硫酸铜吸湿性很强,需要现制现用.
在中学化学实验中,通常用无水硫酸铜检验少量水的存在.由于无水硫酸铜吸湿性很强,需要现制现用.方法甲:取2药匙细小的硫酸铜晶体置于
研钵
研钵
中研碎后放入坩埚,将坩埚放在泥三角
泥三角
上用小火慢慢加热并用玻璃棒不停搅拌,最后将坩埚移入干燥器
干燥器
中进行冷却(请选用合适仪器或设备填空:表面皿、研钵、烧杯、通风橱、试管夹、干燥器、泥三角).方法乙:取2药匙研碎的硫酸铜晶体于小烧杯中,加入20ml浓硫酸(质量分数不低于98%),并用玻璃棒搅拌,静置5min后倾去浓硫酸,用无水乙醇洗涤数次,倒在滤纸上晾干.
交流与讨论:
(1)方法甲中,加热温度稍高时会出现变黑现象,原因是
CuSO4?5H2O
CuO+SO3+5H2O或CuSO4?5H2O
CuO+H2SO4+4H2O
| ||
| ||
CuSO4?5H2O
CuO+SO3+5H2O或CuSO4?5H2O
CuO+H2SO4+4H2O
(用化学方程式表示);
| ||
| ||
(2)方法乙中,浓硫酸的作用是
吸水剂
吸水剂
,为了不浪费药品,对无水乙醇洗涤液进行再生的方法是加CaO后蒸馏
加CaO后蒸馏
,所用的主要玻璃仪器有蒸馏烧瓶、温度计、承接管(牛角管)、锥形瓶酒精灯、冷凝管
酒精灯、冷凝管
等;(3)用制得的无水硫酸铜检验某双氧水中是否含水时,除了发现固体变蓝外,还发现该双氧水中有气泡产生,对此你有何猜想
铜离子(或硫酸铜)对双氧水分解有催化作用
铜离子(或硫酸铜)对双氧水分解有催化作用
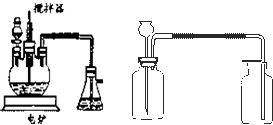
;(4)目前工业上正积极探索用浓HNO3作氧化剂,用Cu与浓H2SO4、浓HNO3反应,采取间歇加热、逐渐加入浓HNO3的方法来制备CuSO4?5H2O 的新工艺.模拟制备装置如图所示.
问题一如图装置中,分液漏斗内装的液体是
浓硝酸
浓硝酸
;反应结束时,获取CuSO4?5H2O的操作过程是先先撤去导管
先撤去导管
,后停止加热
停止加热
;趁热将三颈瓶中的液体倒入烧杯中冷却,析出晶体CuSO4?5H2O,过滤、晾干;问题二工业上用石灰乳吸收尾气,除了防止环境污染外,还能得到了有经济实用价值的副产品----亚硝酸钙.尾气吸收生成亚硝酸钙的化学方程式是:
NO2+NO+Ca(OH)2=Ca(NO2)2+H2O 或4NO2+2Ca(OH)2=Ca(NO3)2+Ca(NO2)2+2H2O
NO2+NO+Ca(OH)2=Ca(NO2)2+H2O 或4NO2+2Ca(OH)2=Ca(NO3)2+Ca(NO2)2+2H2O
;问题三将石灰乳稀释,可得到澄清石灰水. 澄清石灰水与CO2相遇能够产生白色沉淀.某同学想用如图所示装置以大理石和稀盐酸反应制取CO2.教师指出制取等量的气体,该装置需要太多的盐酸,造成浪费.该同学对该装置某部位加了一个小试管,解决了这个问题.请你把改进画在图中合适的位置.


海洋是资源的宝库,海水中所含食盐高达4×1016t.用海水可生产食盐和金属镁或镁的化合物,其过程如下图所示.

请回答:
(1)贝壳主要成分的化学式
(2)步骤④反应的离子方程式
(3)实验室由粗盐结晶制精盐的操作包括溶解、过滤、蒸发等步骤.
A.粗盐提纯过程中过滤的目的是
①获得NaCl晶体 ②除去难溶性物质 ③除去易挥发物质 ④除去可溶性物质
B.过滤需要用到的玻璃仪器有玻璃棒
(4)Mg(OH)2加热分解生成MgO和H2O,MgO是高熔点的化合物.某些材料因含有Mg(OH)2而具有阻燃性.简析Mg(OH)2能够阻燃的原因.
①
(5)电解MgCl2制金属Mg的反应方程式为:MgCl2
Mg+Cl2↑.电解0.2molMgCl2可生成金属Mg
查看习题详情和答案>>

请回答:
(1)贝壳主要成分的化学式
CaCO3
CaCO3
.(2)步骤④反应的离子方程式
Mg(OH)2+2H+=Mg2++2H2O
Mg(OH)2+2H+=Mg2++2H2O
.(3)实验室由粗盐结晶制精盐的操作包括溶解、过滤、蒸发等步骤.
A.粗盐提纯过程中过滤的目的是
②
②
(填序号)①获得NaCl晶体 ②除去难溶性物质 ③除去易挥发物质 ④除去可溶性物质
B.过滤需要用到的玻璃仪器有玻璃棒
漏斗
漏斗
、烧杯
烧杯
.(4)Mg(OH)2加热分解生成MgO和H2O,MgO是高熔点的化合物.某些材料因含有Mg(OH)2而具有阻燃性.简析Mg(OH)2能够阻燃的原因.
①
Mg(OH)2受热分解生成MgO难熔物覆盖在可燃物表面阻止了可燃物的燃烧
Mg(OH)2受热分解生成MgO难熔物覆盖在可燃物表面阻止了可燃物的燃烧
; ②分解生成的水会降低环境的温度
分解生成的水会降低环境的温度
.(5)电解MgCl2制金属Mg的反应方程式为:MgCl2
| ||
4.8
4.8
g,同时可得到氯气4.48
4.48
L(标准状况).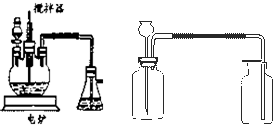 在中学化学实验中,通常用无水硫酸铜检验少量水的存在.由于无水硫酸铜吸湿性很强,需要现制现用.
在中学化学实验中,通常用无水硫酸铜检验少量水的存在.由于无水硫酸铜吸湿性很强,需要现制现用.