摘要:4.实验室中根据2SO2+O22SO3,ΔH=-393.2 kJ·mol-1设计如下图所示实验装置来制备SO3固体.请回答下列问题. (1)实验前.必须进行的操作是(填操作名称.不必写具体过程) ▲ (2)在A装置中加入Na2SO3固体的同时.还需加几滴水.然后再滴加浓硫酸.加几滴水的作用是 ▲ (3)小试管C的作用是 ▲ (4)广口瓶D内盛的试剂是 ▲ .装置D的三个作用是 ① ▲ ② ▲ ③ ▲ (5)实验中当Cr2O3表面红热时.应将酒精灯移开一会儿再加热.以防温度过高.这样做的原因是 ▲ (6)装置F中U型管内收集到的物质的颜色.状态是 ▲ (7)装置G的作用是 ▲ (8)从G装置导出的尾气处理方法是 ▲ (1)检查装置的气密性 (2)水与浓硫酸作用放热.有利于SO2的放出 (3)缓冲.防止倒吸 (4)浓硫酸.①干燥SO2和O2 ②使SO2和O2混合均匀 ③通过观察控制气体比例和气流速度 (5)温度过高不利于SO3的生成.且影响催化剂的活性 防止水蒸气与SO3接触(8)用NaOH溶液吸收
网址:http://m.1010jiajiao.com/timu3_id_393700[举报]
A、B、C、D、E五种短周期元素,原子序数依次增大,A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y,A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物.回答下列问题:
(1)常温下,X、Y的水溶液的pH均为5.则两种水溶液中由水电离出的H+浓度之比是
(2)A、B、D、E四种元素组成的某无机化合物,受热易分解.写出少量该化合物溶液与足量的Ba(OH)2溶液反应的离子方程式
(3)A、B、D、E四种元素组成的某无机化合物浓度为0.1mol/L时,pH最接近
A.5.6B.7.0 C.8.4D.13.0
(4)在一个装有可移动活塞的容器中进行如下反应:C2(g)+3A2(g) 2CA3(g)
2CA3(g)
△H=-92.4kJ?mol-1.反应达到平衡后,测得容器中含有C2 0.5mol,A2 0.2mol,CA3 0.2mol,总容积为1.0L.
①如果达成此平衡前各物质起始的量有以下几种可能,其中不合理的是
A.C2 0.6mol,A2 0.5mol,CA3 0mol
B.C2 0mol,A2 0mol,CA3 1.2mol
C.C2 0.6mol/L,A2 0.5mol/L,CA3 0.2mol/L
②求算此平衡体系的平衡常数K=
③如果保持温度和压强不变,向上述平衡体系中加入0.18molC2,平衡将
④已知0.4mol 液态C2 A4与足量的液态双氧水反应,生成C2和水蒸气,放出256.65kJ的热量.写出该反应的热化学方程式
查看习题详情和答案>>
(1)常温下,X、Y的水溶液的pH均为5.则两种水溶液中由水电离出的H+浓度之比是
10-4:1
10-4:1
.(2)A、B、D、E四种元素组成的某无机化合物,受热易分解.写出少量该化合物溶液与足量的Ba(OH)2溶液反应的离子方程式
Ba2++HCO3-+OH-═BaCO3↓+H2O
Ba2++HCO3-+OH-═BaCO3↓+H2O
.(3)A、B、D、E四种元素组成的某无机化合物浓度为0.1mol/L时,pH最接近
C
C
.A.5.6B.7.0 C.8.4D.13.0
(4)在一个装有可移动活塞的容器中进行如下反应:C2(g)+3A2(g)
 2CA3(g)
2CA3(g)△H=-92.4kJ?mol-1.反应达到平衡后,测得容器中含有C2 0.5mol,A2 0.2mol,CA3 0.2mol,总容积为1.0L.
①如果达成此平衡前各物质起始的量有以下几种可能,其中不合理的是
BC
BC
:A.C2 0.6mol,A2 0.5mol,CA3 0mol
B.C2 0mol,A2 0mol,CA3 1.2mol
C.C2 0.6mol/L,A2 0.5mol/L,CA3 0.2mol/L
②求算此平衡体系的平衡常数K=
10
10
;③如果保持温度和压强不变,向上述平衡体系中加入0.18molC2,平衡将
逆向
逆向
(填“正向”、“逆向”或“不”)移动.理由是原平衡体系中,1.0L容器中含有分子0.5mol+0.2mol+0.2mol=0.9mol,当加入N2,体系瞬间有分子0.9mol+0.18ml=1.08mol,瞬间总体积为1.08×
=1.2L,所以:Q=
=
=10.59>10,平衡逆向移动
| 1.00 |
| 0.9 |
| c2(NH3) |
| c(N2)×c3(H2) |
(
| ||||
(
|
原平衡体系中,1.0L容器中含有分子0.5mol+0.2mol+0.2mol=0.9mol,当加入N2,体系瞬间有分子0.9mol+0.18ml=1.08mol,瞬间总体积为1.08×
=1.2L,所以:Q=
=
=10.59>10,平衡逆向移动
.| 1.00 |
| 0.9 |
| c2(NH3) |
| c(N2)×c3(H2) |
(
| ||||
(
|
④已知0.4mol 液态C2 A4与足量的液态双氧水反应,生成C2和水蒸气,放出256.65kJ的热量.写出该反应的热化学方程式
N2H4(l)+2H2O2(l)=N2(g)+4H2O(g)△H=-641.63kJ?mol-1
N2H4(l)+2H2O2(l)=N2(g)+4H2O(g)△H=-641.63kJ?mol-1
.目前,我们食用的食品、饮料等带外包装的越来越多,购买前须认真阅读食品包装说明,严禁食用超期的、对人体有害的食品,以确保人体健康.
(1)下表是某饮料包装袋上的说明,从表中的配料中分别选出一种填在相应的横线上.
其中①属于着色剂的有
(2)下表是某食品包装袋上的说明,从表中的配料中分别选出一种填在相应的横线上.
①富含蛋白质的是
③富含油脂的是
查看习题详情和答案>>
(1)下表是某饮料包装袋上的说明,从表中的配料中分别选出一种填在相应的横线上.
| 品 名 | 浓缩菠萝汁 |
| 配 料 | 水.浓缩菠萝汁.蔗糖.柠檬酸.黄原胶.甜蜜素.维生素C,菠萝香精.柠檬黄.日落黄.山梨酸钾等 |
| 果汁含量 | ≥80% |
| 生产日期 | 标于包装袋封口上 |
柠檬黄、日落黄
柠檬黄、日落黄
②属于调味剂的有蔗糖、柠檬酸、甜蜜素、菠萝香精
蔗糖、柠檬酸、甜蜜素、菠萝香精
③属于防腐剂的有山梨酸钾
山梨酸钾
④富含维生素的有维生素C
维生素C
(2)下表是某食品包装袋上的说明,从表中的配料中分别选出一种填在相应的横线上.
| 品 名 | ××× |
| 配 料 | 鲜鸡蛋、精面粉、白砂糖、精炼植物油、奶油、奶粉、食盐、柠檬汁等 |
| 保质期 | 240天 |
| 生产日期 | 标于包装袋封口上 |
鲜鸡蛋、奶粉
鲜鸡蛋、奶粉
②富含糖类的是精面粉、白砂糖
精面粉、白砂糖
.③富含油脂的是
精炼植物油、奶油
精炼植物油、奶油
④富含维生素的是柠檬汁
柠檬汁
.某校化学兴趣小组的同学用滴定法对一含有少量Na2SO4的NaOH样品中NaOH的含量进行测定.实验步骤如下,回答下列问题:
(1)用分析天平准确称取该样品5.000g,全部溶于水配制成1000.0mL的溶液.用
(2)用浓度为0.1000mol/L的盐酸标准溶液进行滴定.滴定管在使用前应先检漏、洗涤、
(3)若用测定溶液pH的方法来确定滴定的终点,则应用
(4)滴定过程中,锥形瓶中溶液的pH变化如下
请绘制出上述中和滴定的曲线.
(5)下表是几种酸碱指示剂的变色范围,根据你作出的中和滴定曲线分析,上述中和滴定中可选用的指示剂是
(6)样品中,NaOH的质量百分含量为
查看习题详情和答案>>
(1)用分析天平准确称取该样品5.000g,全部溶于水配制成1000.0mL的溶液.用
碱式滴定管
碱式滴定管
量取其中20.00mL放在锥形瓶中,滴加几滴指示剂,待测.(2)用浓度为0.1000mol/L的盐酸标准溶液进行滴定.滴定管在使用前应先检漏、洗涤、
用待装液润洗
用待装液润洗
、正式装液,排除气泡并调节液面.(3)若用测定溶液pH的方法来确定滴定的终点,则应用
pH计
pH计
测定锥形瓶中溶液的pH,临近滴定终点时应注意每滴一滴测一次
每滴一滴测一次
.(4)滴定过程中,锥形瓶中溶液的pH变化如下
| V(HCl)/mL | 0.00 | 12.00 | 18.00 | 22.00 | 23.00 | 23.96 | 24.00 | 24.04 | 25.00 | 26.00 | 30.00 |
| pH | 13.1 | 12.6 | 12.2 | 11.7 | 11.4 | 9.9 | 7.0 | 4.0 | 2.7 | 2.4 | 1.9 |
(5)下表是几种酸碱指示剂的变色范围,根据你作出的中和滴定曲线分析,上述中和滴定中可选用的指示剂是
甲基橙或酚酞
甲基橙或酚酞
,滴定终点的现象是溶液由黄色变成橙色其半分钟不褪色(或溶液由粉红色变为无色且半分钟不褪色)
溶液由黄色变成橙色其半分钟不褪色(或溶液由粉红色变为无色且半分钟不褪色)
.(如有几种,可任填一种)| 指示剂 | 变色范围 (pH) |
各范围内颜色 | ||
| 前 | 中间 | 后 | ||
| 甲基橙 | 3.1~4.4 | 红 | 橙色 | 黄 |
| 石蕊 | 5.0~8.0 | 红 | 紫色 | 蓝 |
| 酚酞 | 8.2~10.0 | 无 | 粉红 | 红 |
96%
96%
.若滴定前滴定管尖嘴部分有气泡,滴定终了没有气泡,则会造成计算值偏大
偏大
(填“偏大”、“偏小”或“无法确定”).实验室有一瓶混有少量NaCl杂质的NaOH固体试剂,为准确测其纯度,采用盐酸滴定法进行测定.
①称取Wg NaOH固体试剂配制成100.00mL水溶液备用;
②将浓度为 c mol/L的标准盐酸装在用标准盐酸润洗过的25.00mL酸式滴定管中,调节液面位置在零刻度以下,并记下刻度;
③取V1mL NaOH待测溶液置于洁净的锥形瓶中,加入2~3滴甲基橙指示剂充分振荡,然后用浓度为c mol/L的标准盐酸滴定,重复测定3次,平均用去盐酸V2mL.
试回答:
(1)配制标准盐酸溶液时,必须使用的最主要玻璃仪器是
(2)滴定时,滴定过程中两眼应该注视
(3)下列操作会使实验测得结果偏大的是(填选项的序号)
A.用湿润的pH试纸测定某NaOH溶液的pH
B.中和滴定实验中用蒸馏水洗净的锥形瓶直接装待测液
C.若滴定前酸式滴定管尖嘴气泡未排出,滴定结束后气泡消失
D.装标准盐酸的酸式滴定管没有进行润洗
E.读数时,若滴定前仰视,滴定后俯视
(4)固体试剂NaOH的质量分数的表达式为
×100%
×100%.
查看习题详情和答案>>
①称取Wg NaOH固体试剂配制成100.00mL水溶液备用;
②将浓度为 c mol/L的标准盐酸装在用标准盐酸润洗过的25.00mL酸式滴定管中,调节液面位置在零刻度以下,并记下刻度;
③取V1mL NaOH待测溶液置于洁净的锥形瓶中,加入2~3滴甲基橙指示剂充分振荡,然后用浓度为c mol/L的标准盐酸滴定,重复测定3次,平均用去盐酸V2mL.
试回答:
(1)配制标准盐酸溶液时,必须使用的最主要玻璃仪器是
容量瓶
容量瓶
.(2)滴定时,滴定过程中两眼应该注视
锥形瓶内溶液的颜色变化
锥形瓶内溶液的颜色变化
.滴定终点时溶液颜色由黄
黄
色突变为橙
橙
色.在盛放待测溶液的锥形瓶下方放一张白纸的作用是观察锥形瓶中溶液颜色的变化明显,减少实验误差
观察锥形瓶中溶液颜色的变化明显,减少实验误差
.(3)下列操作会使实验测得结果偏大的是(填选项的序号)
CD
CD
;A.用湿润的pH试纸测定某NaOH溶液的pH
B.中和滴定实验中用蒸馏水洗净的锥形瓶直接装待测液
C.若滴定前酸式滴定管尖嘴气泡未排出,滴定结束后气泡消失
D.装标准盐酸的酸式滴定管没有进行润洗
E.读数时,若滴定前仰视,滴定后俯视
(4)固体试剂NaOH的质量分数的表达式为
| 4CV2 |
| WV1 |
| 4CV2 |
| WV1 |
黄铁矿(主要成分为FeS2)是我国大多数硫酸厂制取硫酸的主要原料.某化学学习小组对某黄铁矿石进行如下实验探究.[实验一]测定硫元素的含量.
Ⅰ、将m1g该黄铁矿样品放入如图1所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全.石英管中发生反应的化学方程式为:4FeS2+11O2
2Fe2O3+8SO2.
Ⅱ、反应结束后,将乙瓶中的溶液进行如图2所示处理.
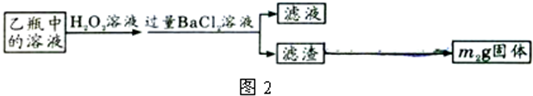
[实验二]测定铁元素的含量.
Ⅲ、测定铁元素含量的实验步骤如图3所示.

问题讨论:
(1)Ⅰ中,甲瓶内所盛试剂是
(2)Ⅱ中的滤渣在称量前还应进行的操作是
(3)Ⅱ中,所加H2O2溶液(氧化剂)需足量的理由是
(4)④中取稀释液25.00ml需用的仪器是
(5)该黄铁矿中硫元素的质量分数为
×100%
×100%.
查看习题详情和答案>>
Ⅰ、将m1g该黄铁矿样品放入如图1所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全.石英管中发生反应的化学方程式为:4FeS2+11O2
| ||

Ⅱ、反应结束后,将乙瓶中的溶液进行如图2所示处理.

[实验二]测定铁元素的含量.
Ⅲ、测定铁元素含量的实验步骤如图3所示.

问题讨论:
(1)Ⅰ中,甲瓶内所盛试剂是
NaOH
NaOH
溶液.乙瓶内发生反应的离子方程式有:SO2+2OH-=SO32-+H2O
SO2+2OH-=SO32-+H2O
、2SO32-+O2=2SO42-
2SO32-+O2=2SO42-
.(2)Ⅱ中的滤渣在称量前还应进行的操作是
洗涤、干燥
洗涤、干燥
.(3)Ⅱ中,所加H2O2溶液(氧化剂)需足量的理由是
使SO32-完全氧化为SO42-
使SO32-完全氧化为SO42-
.(4)④中取稀释液25.00ml需用的仪器是
酸式滴定管
酸式滴定管
.Ⅲ的步骤③中,需要用到的仪器除烧杯、玻璃棒、胶头滴管外,还有250ml 容量瓶
250ml 容量瓶
(画出其简易装置图).(5)该黄铁矿中硫元素的质量分数为
| 32m2 |
| 233m1 |
| 32m2 |
| 233m1 |