摘要:22. ⑴ 以前实验室制备纯碱(Na2CO3)的主要步骤为:将饱和NaCl溶液倒入烧杯加热.控制30-35℃.搅拌下分批加入研细的NH4HCO3固体.加料完毕.保温30分钟.静置.过滤得NaHCO3晶体.用少量蒸馏水洗涤除去杂质.抽干.转入蒸发皿中灼烧得Na2CO3固体. 四种盐在不同温度下的溶解度表 温度 溶解度 0℃ 10℃ 20℃ 30℃ 40℃ 50℃ 60℃ 100℃ NaCl 35.7 35.8 36.0 36.3 36.6 37.0 37.3 39.8 NH4HCO3 11.9 15.8 21.0 27.0 - - - - NaHCO3 6.9 8.1 9.6 11.1 12.7 14.5 16.4 - NH4Cl 29.4 33.3 37.2 41.4 45.8 50.4 55.3 77.3 ①.反应控制在30-35℃.是因为高于35℃NH4HCO3会分解.低于30℃则反应速率降低 .为控制此温度范围.通常采取的加热方法为 , ②.加料完毕.保温30分钟.目的 , ③.静置后只析出NaHCO3晶体的原因 , ④过滤所得母液中含有NaHCO3.NaCl .NH4Cl.NH4HCO3.加入适当试剂并作进一步处理.使 循环使用.回收得到NH4Cl晶体. ⑵我国科学家侯德榜改革国外的纯碱生产工艺.使其更加先进.被称为侯德榜制碱法.生产流程为: ⑤ 沉淀池中反应的化学方程式: - , ⑥ 检验产品碳酸钠中是否含有氯化钠的操作方法为: . ⑦循环(I)中应该加入或通入物质的化学式为 .
网址:http://m.1010jiajiao.com/timu3_id_393514[举报]
海洋中有丰富的食品、矿产、能源、药物和水产资源,如图为海水利用的部分过程.
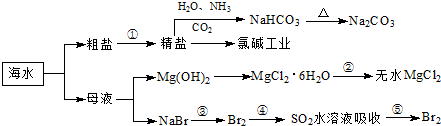
回答下列有关问题.
(1)下列有关说法正确的是 .
A.目前国际上主要使用蒸馏法的“海水淡化”技术,得高纯度淡水
B.用澄清的石灰水可鉴别NaHCO3和Na2CO3
C.在第③、④、⑤步骤中,溴元素均被氧化
D.工业上通过电解饱和NaCl溶液制取金属钠
(2)写出第③步骤的化学反应方程式 .
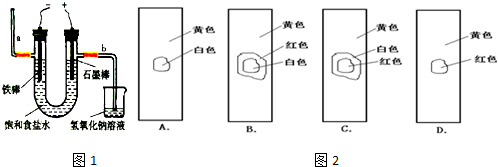
(3)工业上利用电解饱和食盐水可制得重要化工产品,又称为“氯碱工业”. 氯气的工业制取装置如图1,回答:
①若饱和食盐水中含有酚酞,通电后 (填a或b)侧先变红.
②电解反应的化学方程式为 .
③氯气制成氯水,用玻璃棒蘸取新制氯水滴在pH试纸中部,观察到的现象是 .
(4)工业上以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱.有关反应的化学方程式为:
NH3+CO2+H2O═NH4HCO3;
NH4HCO3+NaCl═NaHCO3↓+NH4Cl;
2NaHCO3
Na2CO3+CO2↑+H2O
某活动小组根据上述制碱原理,进行碳酸氢钠的制备实验.
①一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如图3所示(图中夹持、固定用的仪器未画出).试回答下列有关问题:
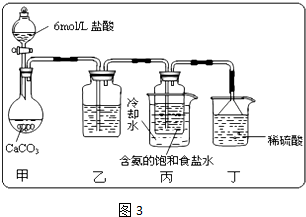
Ⅰ、乙装置中的试剂是 ,其作用是 .
Ⅱ、丁装置中稀硫酸的作用是 .
Ⅲ、实验结束后,分离出NaHCO3 晶体的操作是 (填分离操作的名称),该操作所需要的玻璃仪器有 .
②碳酸氢钠受热所得固体12.28g与足量的石灰水充分反应,所得沉淀经洗涤、干燥质量为12.00g,则所得固体中碳酸钠的质量分数为 .
③请你再设计出一种实验室制取少量碳酸氢钠的方法: .
查看习题详情和答案>>

回答下列有关问题.
(1)下列有关说法正确的是
A.目前国际上主要使用蒸馏法的“海水淡化”技术,得高纯度淡水
B.用澄清的石灰水可鉴别NaHCO3和Na2CO3
C.在第③、④、⑤步骤中,溴元素均被氧化
D.工业上通过电解饱和NaCl溶液制取金属钠
(2)写出第③步骤的化学反应方程式
(3)工业上利用电解饱和食盐水可制得重要化工产品,又称为“氯碱工业”. 氯气的工业制取装置如图1,回答:
①若饱和食盐水中含有酚酞,通电后
②电解反应的化学方程式为
③氯气制成氯水,用玻璃棒蘸取新制氯水滴在pH试纸中部,观察到的现象是

(4)工业上以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱.有关反应的化学方程式为:
NH3+CO2+H2O═NH4HCO3;
NH4HCO3+NaCl═NaHCO3↓+NH4Cl;
2NaHCO3
| ||
某活动小组根据上述制碱原理,进行碳酸氢钠的制备实验.
①一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如图3所示(图中夹持、固定用的仪器未画出).试回答下列有关问题:

Ⅰ、乙装置中的试剂是
Ⅱ、丁装置中稀硫酸的作用是
Ⅲ、实验结束后,分离出NaHCO3 晶体的操作是
②碳酸氢钠受热所得固体12.28g与足量的石灰水充分反应,所得沉淀经洗涤、干燥质量为12.00g,则所得固体中碳酸钠的质量分数为
③请你再设计出一种实验室制取少量碳酸氢钠的方法: