网址:http://m.1010jiajiao.com/timu3_id_390213[举报]
(2001·理综)已知天然气的主要成分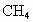 是一种会产生温室效应的气体.等物质的量的
是一种会产生温室效应的气体.等物质的量的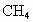 和
和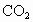 产生的温室效应前者大.下面是有关天然气的几种叙述:①天然气与煤、柴油相比是比较清洁的能源;②等质量的
产生的温室效应前者大.下面是有关天然气的几种叙述:①天然气与煤、柴油相比是比较清洁的能源;②等质量的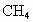 和
和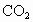 产生的温室效应也是前者大;③燃烧天然气,也是酸雨的成因之一.其中正确的是
产生的温室效应也是前者大;③燃烧天然气,也是酸雨的成因之一.其中正确的是
[ ]
(09年天津理综·10)(14分)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
![]() (1)氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为 (用a、b表示)。
(1)氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为 (用a、b表示)。
![]() (2)负极反应式为 。
(2)负极反应式为 。
![]() (3)电极表面镀铂粉的原因为 。
(3)电极表面镀铂粉的原因为 。
![]() (4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
(4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:![]() Ⅰ.2Li+H2
Ⅰ.2Li+H2![]()
![]() 2LIH
2LIH
![]() Ⅱ.LiH+H2O==LiOH+H2↑
Ⅱ.LiH+H2O==LiOH+H2↑
![]() ①反应Ⅰ中的还原剂是 ,反应Ⅱ中的氧化剂是 。
①反应Ⅰ中的还原剂是 ,反应Ⅱ中的氧化剂是 。
![]() ②已知LiH固体密度为0.82g/cm3。用锂吸收224L(标准状况)H2,生成的LiH体积与被吸收的H2体积比为 。
②已知LiH固体密度为0.82g/cm3。用锂吸收224L(标准状况)H2,生成的LiH体积与被吸收的H2体积比为 。
![]() ③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为 mol。
③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为 mol。
(06年天津卷)已知反应:①101kPa时,2C(s)+O2(g)=2CO(g);△H=-221kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(1);△H=-57.3kJ/mol
下列结论正确的是()
A 碳的燃烧热大于110.5kJ/mol
B ①的反应热为221kJ/mol
C 稀硫酸与稀NaOH溶液反应的中和热为-57.3kJ/mol
D 稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量
查看习题详情和答案>>
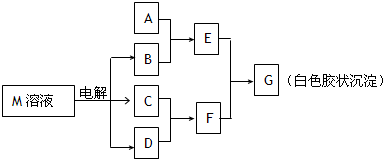
(1)若A是与X、Y同周期的一种常见金属,则A元素在周期表中的位置是
(2)若A是某元素的一种常见酸性氧化物,可用于制造光导纤维,则该元素原子结构示意图为


(3)B的电子式为
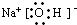
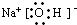


(4)工业上用电解物质M的产物之一氧化有毒含氰(CN-)碱性废水,得到无毒的N2、CO2等.写出此反应的离子反应方程式
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为
(2)W与Y可形成化合物W2Y,该化合物的电子式为


(3)X的硝酸盐水溶液显
(4)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为
(5)比较Y、Z气态氢化物的稳定性:
(6)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是
(7)Z的最高价氧化物为无色液体,0.25mol该物质与一定量水混合得到一种稀溶液,并放出Q kJ的热量.写出该反应的热化学方程式: