网址:http://m.1010jiajiao.com/timu3_id_389326[举报]

A.NaOH溶液 B.浓H2SO4 C.Ba(OH)2溶液 D.食盐水
查看习题详情和答案>>
A.浓H2SO4 B.NaOH溶液?
C.水 D.饱和食盐水?
查看习题详情和答案>>|
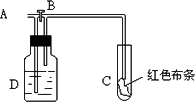
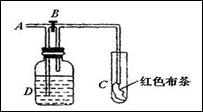
如下图:A处通入氯气,关闭B阀时,C处湿润红色布条无变化,打开B阀时,C处湿润的红色布条褪色.则D中可以盛放足量的
| |
| [ ] | |
A. |
浓硫酸 |
B. |
氢氧化钠溶液 |
C. |
水 |
D. |
饱和食盐水 |
|
如下图,A处通入氯气.关闭B阀时,C处红色布条褪色,打开B阀时,C处红色布条无变化.由此做的判断正确的是
| |
A. |
D中可能是浓硫酸 |
B. |
通入的氯气含有水分 |
C. |
D中可能是水 |
D. |
D中可能是饱和食盐水 |
Ⅰ.利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理.用乙烯作为还原剂将氮的氧化物还原为N2是燃煤烟气的一种脱硝(除NOx)技术.其脱硝机理如图甲,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图乙所示.
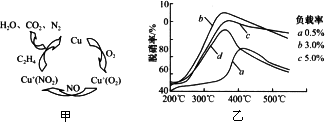
①写出该脱硝过程中乙烯和NO2反应的化学方程式________.
②为达到最佳脱硝效果,应采取的条件________.
Ⅱ.有学者设想以下图所示装置用电化学原理将燃煤烟气中的CO2、SO2转化为重要化工原料.
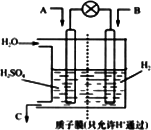
若A为SO2,B为O2,C为H2SO4.科研人员希望每分钟从C处获得50 mL 10 mol/L H2SO4,则A处通人烟气(SO2的体积分数为1%)的速率为________L/min(标准状况).
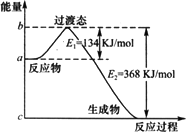
Ⅲ.(1)下图是1 mol NO2(g)和1 mol CO(g)反应生成CO2和NO过程中能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是________,ΔH的变化是________(填“增大”、“减小”、“不变”).
(2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)![]() CO2(g)+3H2(g) ΔH=+49.0 kJ·mol-1,
CO2(g)+3H2(g) ΔH=+49.0 kJ·mol-1,
②CH3OH(g)+![]() O2(g)
O2(g)![]() CO2(g)+2H2(g) ΔH=-192.9kJ·mol-1
CO2(g)+2H2(g) ΔH=-192.9kJ·mol-1
又知③H2O(g)=H2O(l) ΔH=-44 kJ·mol-1
则甲醇蒸气完全燃烧生成液态水的热化学方程式为________.
写出甲醇燃料电池在酸性条件下的负极电极反应式________.