网址:http://m.1010jiajiao.com/timu3_id_389222[举报]
| |||||||||||||||
| 改变的条件 | 新平衡与原平衡比较 | |
| A | 升高温度 | X的体积分数变大 |
| B | 增大压强 | Z的浓度不变 |
| C | 充入一定量Y | Y的转化率增大 |
| D | 充入一定量Z | X的体积分数变大 |
化学能与电能之间的相互转化与人的生活实际密切相关,在生产、生活中有重要的应用,同时也是学生形成化学学科素养的重要组成部分。
(1)熔融状态下,钠的单质和氯化亚铁能组成可充电电池(如图1),反应原理为:2Na+FeCl2  Fe+2NaCl,该电池放电时,正极反应式为 ________________ _____:
Fe+2NaCl,该电池放电时,正极反应式为 ________________ _____:
充电时,__________(写物质名称)电极接电源的负极;
该电池的电解质为________ _。
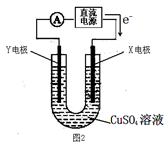
(2)某同学用铜片、石墨作电极电解一定浓度的硫酸铜溶液(如图2),一段时间停止通电取出电极。若在电解后的溶液中加入0.98g氢氧化铜粉末恰好完全溶解,经测定所得溶液与电解前完全相同。请回答下列问题:
①Y电极材料是 ,发生 (填“氧化或还原”)反应。
②电解过程中X电极上发生的电极反方应式是:
③如在电解后的溶液中加入足量的小苏打,充分反应后产生气体在标准状况下所占的体积是
(3)常温时,BaSO4的Ksp=1.08×10-10,现将等体积的BaCl2溶液与2.0×10-3mol/l的Na2SO4
溶液混合。若要生成BaSO4沉淀,BaCl2溶液的最小浓度为______________。
(1)熔融状态下,钠的单质和氯化亚铁能组成可充电电池(如图1),反应原理为:2Na+FeCl2
 Fe+2NaCl,该电池放电时,正极反应式为 ________________ _____:
Fe+2NaCl,该电池放电时,正极反应式为 ________________ _____: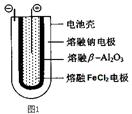
充电时,__________(写物质名称)电极接电源的负极;
该电池的电解质为________ _。
(2)某同学用铜片、石墨作电极电解一定浓度的硫酸铜溶液(如图2),一段时间停止通电取出电极。若在电解后的溶液中加入0.98g氢氧化铜粉末恰好完全溶解,经测定所得溶液与电解前完全相同。请回答下列问题:
①Y电极材料是 ,发生 (填“氧化或还原”)反应。
②电解过程中X电极上发生的电极反方应式是:
③如在电解后的溶液中加入足量的小苏打,充分反应后产生气体在标准状况下所占的体积是
(3)常温时,BaSO4的Ksp=1.08×10-10,现将等体积的BaCl2溶液与2.0×10-3mol/l的Na2SO4
溶液混合。若要生成BaSO4沉淀,BaCl2溶液的最小浓度为______________。
现有五种短周期元素A、B、C、D、E,其原子序数依次增大。A、E同主族,A元素原子半径最小,B元素原子的最外层电子数是内层电子数的2倍。C元素最高价氧化物的水化物X能与其氢化物Y反应生成盐。A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物。
(1) 写出Y和D2在催化剂作用下反应的化学方程式___________________________
(用化学式表示,以下同)
(2) 将X和Y的水溶液充分混合后,测得溶液的pH>7,则该溶液中离子浓度由大到小的顺序是____________________________________________。
(3) 将B的某种单质作电极,电解E元素的最高价氧化物对应水化物的水溶液时,阳极的电极反应式为_____________________________________。
(4) 在一定温度下,将3 mol A2和3mol C2两种气体通人容积为lL的恒容密闭容器中,发生反应3 A2 (g)+ C2 (g)![]() 2C A2 (g)△H=一92.4kJ/mol。当反应达到平衡时,测得容器内的压强为起始时的
2C A2 (g)△H=一92.4kJ/mol。当反应达到平衡时,测得容器内的压强为起始时的![]() 。则此时反应放出的热量为______________,该条件下
。则此时反应放出的热量为______________,该条件下
反应的平衡常数K=______________(小数点后保留2位)。
(5) 燃料电池具有能量利用率高,可连续使用和污染小等优点。右图为某燃料电池结构示意图,电解质溶液为KOH溶液,电极材料为石墨,BA4和氧气源源不 断地通到电极上。每消耗1molBA4时,外电路中通过电子的物质的量是_______。
断地通到电极上。每消耗1molBA4时,外电路中通过电子的物质的量是_______。