摘要:.常温下.体积相等.pH值都是3的盐酸和醋酸.分别加水稀释到pH等于4.然后用0.01mol/L的烧碱溶液将酸中和.下列说法中正确的是: ( ) A. 稀释前盐酸和醋酸的物质的量浓度相等 B.稀释后醋酸溶液的体积较大 C. 中和醋酸所用烧碱溶液的体积较大 D. 完全中和后两种溶液的pH值仍然相等
网址:http://m.1010jiajiao.com/timu3_id_388994[举报]
常温下,体积相等,pH值都是3的盐酸和醋酸,分别加水稀释到pH等于4,然后用0.01mol/L的烧碱溶液将酸中和,下列说法中正确的是( )
A.稀释前盐酸和醋酸的物质量浓度相等
B.稀释后醋酸溶液的体积与盐酸溶液的体积相等
C.中和醋酸所用烧碱溶液的体积较大
D.完全中和后两种溶液的pH值仍然相等
查看习题详情和答案>>常温下,体积相等,pH值都是3的盐酸和醋酸,分别加水稀释到pH等于4,然后用0.01mol/L的烧碱溶液将酸中和,下列说法中正确的是( )
A.稀释前盐酸和醋酸的物质量浓度相等
B.稀释后醋酸溶液的体积与盐酸溶液的体积相等
C.中和醋酸所用烧碱溶液的体积较大
D.完全中和后两种溶液的pH值仍然相等
查看习题详情和答案>>常温下,体积相等,pH值都是3的盐酸和醋酸,分别加水稀释到pH等于4,然后用0.01mol/L的烧碱溶液将酸中和,下列说法中正确的是( )
| A.稀释前盐酸和醋酸的物质量浓度相等 |
| B.稀释后醋酸溶液的体积与盐酸溶液的体积相等 |
| C.中和醋酸所用烧碱溶液的体积较大 |
| D.完全中和后两种溶液的pH值仍然相等 |
同学们为了探究镁条与盐酸、醋酸反应时,浓度或温度对反应速率(观察镁条消失的时间)的影响,他们准备了以下化学用品:0.20mol/L与0.40mol/L的HCl溶液、0.2mol/L与0.40mol/L的CH3COOH溶液、4条镁条(形状、大小、质量相同)、几支试管和胶头滴管,酸液温度控制为298K和308K.
(1)该实验缺少的仪器是______.
(2)酸液都取足量、相同体积,请你帮助完成以下面实验设计表:
(3)相同温度时,镁条与相同浓度的盐酸、醋酸反应,刚开始时两者产生气体的速率盐酸______醋酸(选填“=、>或<”),镁条最先消失的是______(选填“盐酸或醋酸”,下同);如果镁条足量,选pH相同、等体积的盐酸和醋酸与镁条反应,产生气体最多的是______.
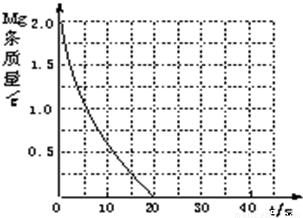
(4)若(2)中实验①镁条消失的时间是20s,则镁条剩余质量与时间关系图如右图.假设:该反应温度每升高10℃,反应速率是原来的2倍;温度相同、浓度相同时,醋酸的平均反应速度是盐酸的1/2.请你在此图中大致画出“实验②”(用实线)、“实验④中醋酸实验”(用虚线)的镁条质量与时间关系曲线.
(5)某温度下,醋酸的电离平衡常数K(CH3COOH)=1.0×10-5.若醋酸的起始浓度为0.l0mol/L,则平衡时溶液的pH值是多少?(写出计算过程)
查看习题详情和答案>>
(1)该实验缺少的仪器是______.
(2)酸液都取足量、相同体积,请你帮助完成以下面实验设计表:
| 实验编号 | 温度(K) | 盐酸浓度 | 醋酸浓度 | 实验目的 |
| ① | 298 | 0.20 | a.实验①和②是探究______对镁与盐酸反应速率的影响; b.实验①和③是探究______对镁与盐酸反应速率的影响; c.实验①和④是探究相同温度下,相同浓度的盐酸、醋酸与镁反应速率的区别. | |
| ② | 308 | 0.20 | ||
| ③ | 298 | 0.40 | ||
| ④ | ______ | ______ |

(4)若(2)中实验①镁条消失的时间是20s,则镁条剩余质量与时间关系图如右图.假设:该反应温度每升高10℃,反应速率是原来的2倍;温度相同、浓度相同时,醋酸的平均反应速度是盐酸的1/2.请你在此图中大致画出“实验②”(用实线)、“实验④中醋酸实验”(用虚线)的镁条质量与时间关系曲线.
(5)某温度下,醋酸的电离平衡常数K(CH3COOH)=1.0×10-5.若醋酸的起始浓度为0.l0mol/L,则平衡时溶液的pH值是多少?(写出计算过程)
查看习题详情和答案>>
下列一句话中叙述了两个值,前者记为M,后者记为N,M和N的关系从A、B、C、D 中选择:
A.M>N B.M<N C.M=N D.无法比较
(1)相同温度下,1L 1mol/L 的NH4Cl溶液中的NH4+个数和2L 0.5mol?L-1NH4Cl溶液中NH4+的个数:
(2)相同温度下,pH值为12的烧碱溶液中水的电离度和pH值为12的CH3COONa溶液中水的电离度:
(3)两份室温时的饱和石灰水,一份升温到50℃;另一份加入少量CaO,恢复至室温,两溶液中的c(Ca2+):
(4)常温下两份等浓度的纯碱溶液,将第二份升高温度,两溶液中c(HCO3-):
(5)将pH值为2的醋酸和盐酸都稀释相同倍数所得稀溶液的pH值:
(6)常温下0.1mol/L的CH3COOH与0.1mol/LCH3COONa等体积混合后溶液中c(Na+)和c(CH3COO-):
(7)同温度下,0.1mol/LFeCl3溶液中Fe3+水解百分率与0.01mol?L-1FeCl3溶液中Fe3+ 的水解百分率:
(8)室温下某强酸和某强碱溶液等体积混合后,溶液的pH值为7,原酸溶液和原碱溶液的物质的量浓度:
(9)pH值相同的醋酸和盐酸,分别用蒸馏水稀释至原来的M倍和N倍,稀释后两溶液的PH值仍然相同,则M和N的关系是:
查看习题详情和答案>>
A.M>N B.M<N C.M=N D.无法比较
(1)相同温度下,1L 1mol/L 的NH4Cl溶液中的NH4+个数和2L 0.5mol?L-1NH4Cl溶液中NH4+的个数:
A
A
;(2)相同温度下,pH值为12的烧碱溶液中水的电离度和pH值为12的CH3COONa溶液中水的电离度:
B
B
;(3)两份室温时的饱和石灰水,一份升温到50℃;另一份加入少量CaO,恢复至室温,两溶液中的c(Ca2+):
B
B
;(4)常温下两份等浓度的纯碱溶液,将第二份升高温度,两溶液中c(HCO3-):
B
B
;(5)将pH值为2的醋酸和盐酸都稀释相同倍数所得稀溶液的pH值:
B
B
;(6)常温下0.1mol/L的CH3COOH与0.1mol/LCH3COONa等体积混合后溶液中c(Na+)和c(CH3COO-):
B
B
;(7)同温度下,0.1mol/LFeCl3溶液中Fe3+水解百分率与0.01mol?L-1FeCl3溶液中Fe3+ 的水解百分率:
B
B
;(8)室温下某强酸和某强碱溶液等体积混合后,溶液的pH值为7,原酸溶液和原碱溶液的物质的量浓度:
D
D
;(9)pH值相同的醋酸和盐酸,分别用蒸馏水稀释至原来的M倍和N倍,稀释后两溶液的PH值仍然相同,则M和N的关系是:
A
A
.