摘要:根据①Fe3++I----Fe2++I2 ②Br2+Fe2+-----Br-+Fe3+,可判断离子还原性由强到弱的顺序是( ) A.Fe2+ . I- .Br- B. I-.Fe2+ .Br- C. Fe2+ .Br-. I- D.Br-. I-.Fe2+
网址:http://m.1010jiajiao.com/timu3_id_388803[举报]
有一瓶澄清溶液,含有
NH4+、Mg2+、Ba2+、Al3+、Fe3+、CO32-、NO3-、Cl-、I-中的三或四种离子.取3份等体积的上述溶液进行以下实验:
(1)第一份用pH试纸试验,表明溶液呈强酸性,加入少量CCl4及数滴新制的氯水,经摇荡后CCl4层呈紫红色.
(2)第二份逐滴加入足量稀硝酸和硝酸银溶液,得沉淀4.70g.
(3)第三份逐滴加入稀NaOH溶液,使溶液从酸性逐渐转变为碱性,在滴加过程中及滴加完毕后,溶液中均无沉淀生成.
①若取(3)得到的溶液,向其中加入Na2CO3溶液,有1.97g白色沉淀生成.
②若将(3)得到的碱性溶液加热,有0.005mol气体放出,该气体能使湿润的红色石蕊试纸变蓝.
根据上述实验事实确定( )
NH4+、Mg2+、Ba2+、Al3+、Fe3+、CO32-、NO3-、Cl-、I-中的三或四种离子.取3份等体积的上述溶液进行以下实验:
(1)第一份用pH试纸试验,表明溶液呈强酸性,加入少量CCl4及数滴新制的氯水,经摇荡后CCl4层呈紫红色.
(2)第二份逐滴加入足量稀硝酸和硝酸银溶液,得沉淀4.70g.
(3)第三份逐滴加入稀NaOH溶液,使溶液从酸性逐渐转变为碱性,在滴加过程中及滴加完毕后,溶液中均无沉淀生成.
①若取(3)得到的溶液,向其中加入Na2CO3溶液,有1.97g白色沉淀生成.
②若将(3)得到的碱性溶液加热,有0.005mol气体放出,该气体能使湿润的红色石蕊试纸变蓝.
根据上述实验事实确定( )
| A、Mg2+可能存在 | B、Fe3+肯定不存在 | C、Cl-肯定存在 | D、NO3-可能存在 |
根据下列三个反应的化学化学方程式,判断下列关系式不正确的是( )
(1)I2+SO2+2H2O═H2SO4+2HI
(2)2FeCl3+2HI═2FeCl2+2HCl+I2
(3)2FeCl2+Cl2═2FeCl3.
(1)I2+SO2+2H2O═H2SO4+2HI
(2)2FeCl3+2HI═2FeCl2+2HCl+I2
(3)2FeCl2+Cl2═2FeCl3.
查看习题详情和答案>>
(2009?广东模拟)七水硫酸镁(MgSO4?7H2O)在印染、造纸和医药等工业上都有广泛的应用,利用化工厂生产硼砂的废渣-硼镁泥可制取七水硫酸镁.硼镁泥的主要成分是MgCO3,还含有其他杂质(MgO、SiO2、Fe2O3、FeO、CaO、Al2O3、MnO等).
表1 部分阳离子以氢氧化物形式完全沉淀时溶液的pH
表2 两种盐的溶解度(单位为g/100g水)
硼镁泥制取七水硫酸镁的工艺流程如下:
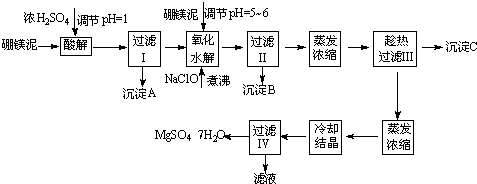
根据以上流程图并参考表格pH数据和溶解度数据,试回答下列问题:
(1)过滤I的滤液中加入硼镁泥,调节溶液的pH=5~6,再加入NaClO溶液加热煮沸,将溶液中的Mn2+氧化成MnO2,反应的离子反应方程式为
(2)沉淀B中除MnO2、SiO2外还含有
(3)检验过滤Ⅱ后的滤液中是否含有Fe3+的实验方法是
(4)沉淀C的化学式是
查看习题详情和答案>>
表1 部分阳离子以氢氧化物形式完全沉淀时溶液的pH
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Mg(OH)2 |
| pH值 | 5.2 | 3.2 | 9.7 | 10.4 | 11.2 |
| 温度/℃ | 10 | 30 | 40 | 50 | 60 |
| CaSO4 | 0.19 | 0.21 | 0.21 | 0.20 | 0.19 |
| MgSO4?7H2O | 30.9 | 35.5 | 40.8 | 45.6 | / |

根据以上流程图并参考表格pH数据和溶解度数据,试回答下列问题:
(1)过滤I的滤液中加入硼镁泥,调节溶液的pH=5~6,再加入NaClO溶液加热煮沸,将溶液中的Mn2+氧化成MnO2,反应的离子反应方程式为
Mn2++ClO-+H2O=MnO2↓+2H++Cl-
Mn2++ClO-+H2O=MnO2↓+2H++Cl-
.加热煮沸的主要目的是促进Al3+、Fe3+水解及Mn2+氧化成MnO2
促进Al3+、Fe3+水解及Mn2+氧化成MnO2
.(2)沉淀B中除MnO2、SiO2外还含有
Fe(OH)3、Al(OH)3
Fe(OH)3、Al(OH)3
(填化学式)等物质.(3)检验过滤Ⅱ后的滤液中是否含有Fe3+的实验方法是
取过滤II后的滤液1~2ml于试管中,加入少量KSCN溶液,如果溶液不显红色,证明滤液中无Fe3+
取过滤II后的滤液1~2ml于试管中,加入少量KSCN溶液,如果溶液不显红色,证明滤液中无Fe3+
;(4)沉淀C的化学式是
CaSO4?2H2O或CaSO4
CaSO4?2H2O或CaSO4
.过滤Ⅲ需趁热过滤的理由是以防MgSO4在温度低时结晶析出
以防MgSO4在温度低时结晶析出
.(Ⅰ)某化学兴趣小组的同学得上用下图所示实验装置进行实验(图中a、b、c表示止水夹).
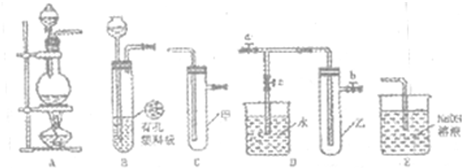
(1)请利用上述装置设计一个简单的实验验证Cl-和Br-的还原性强弱.
①选择合理的装置连接: → → (填字母编号).
②选择所需的试剂: (填字母编号).
a.固体氯化钠 b.固体二氧化锰 c.浓硫酸
d.浓盐酸 e.稀盐酸 f.溴化钠溶液
③实验现象及结论: .
(Ⅱ)电极材料由Ni(OH)2、碳粉、氧化铁等涂覆在铝箔上制成.由于电池使用后电极材料对环境有危害,某兴趣小组对该电池电极材料进行资源回收并制备NiSO4?7H2O晶体,设计实验流程如下:
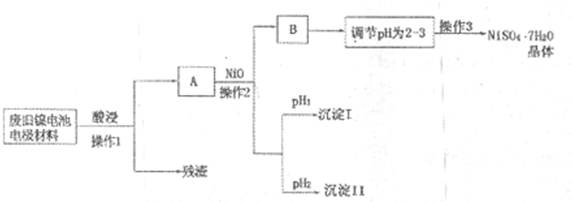
已知:①NiSO4易溶于水,Fe3+不能氧化Ni2+
②某温度下一些金属氢氧化物的KSP及析出理论pH如下表所示:
回答下列问题:
(1)根据上表数据判断操作2依次析出的沉淀I是 沉淀II是 (填化学式),pH1 pH2(填“>”、“<”或“=”);
(2)操作1和操作2所用到的仪器除铁架台(带铁圈)、酒精灯、烧杯、玻璃棒外还需要的主要仪器为 .
(3)“调节pH为2-3”的目的是 ;
(4)NiSO4在强碱溶溶中用NaClO氧化,可制得碱性镍镉电池电极材料--NiOOH.该反应的离子方程式是 .
查看习题详情和答案>>

(1)请利用上述装置设计一个简单的实验验证Cl-和Br-的还原性强弱.
①选择合理的装置连接:
②选择所需的试剂:
a.固体氯化钠 b.固体二氧化锰 c.浓硫酸
d.浓盐酸 e.稀盐酸 f.溴化钠溶液
③实验现象及结论:
(Ⅱ)电极材料由Ni(OH)2、碳粉、氧化铁等涂覆在铝箔上制成.由于电池使用后电极材料对环境有危害,某兴趣小组对该电池电极材料进行资源回收并制备NiSO4?7H2O晶体,设计实验流程如下:

已知:①NiSO4易溶于水,Fe3+不能氧化Ni2+
②某温度下一些金属氢氧化物的KSP及析出理论pH如下表所示:
| M(OH)n | Ksp | pH | |
| 开始沉淀 | 沉淀完全 | ||
| Al(OH)3 | 1.9×10-23 | 3.43 | 4.19 |
| Fe(OH)3 | 3.8×10-38 | 2.53 | 2.94 |
| Ni(OH)2 | 1.6×10-14 | 7.60 | 9.75 |
(1)根据上表数据判断操作2依次析出的沉淀I是
(2)操作1和操作2所用到的仪器除铁架台(带铁圈)、酒精灯、烧杯、玻璃棒外还需要的主要仪器为
(3)“调节pH为2-3”的目的是
(4)NiSO4在强碱溶溶中用NaClO氧化,可制得碱性镍镉电池电极材料--NiOOH.该反应的离子方程式是
硼镁泥是一种工业废料,主要成份是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业.从硼镁泥中提取MgSO4?7H2O的流程如下:

根据题意回答问题:
(1)实验中需用1mol/L的硫酸800mL,若用98%的浓硫酸(ρ=1.84g/mL)来配制,量取浓硫酸时,需使用的量筒的规格为
A.10mL B.20mL C.50mL D.100mL
(2)加入的NaClO可与Mn2+反应:Mn2++ClO-+H2O→MnO2↓+2H++Cl-,还有一种离子也会被NaClO氧化,该反应的离子方程式为 .
(3)滤渣的主要成份除含有Fe(OH)3、Al(OH)3外,还有 .
(4)在“除钙”前,需检验滤液中Fe3+是否被除尽,简述检验方法 .
(5)已知MgSO4、CaSO4的溶解度如下表:
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明操作步骤 .“操作I”是将滤液继续蒸发浓缩,冷却结晶, ,便得到了MgSO4?7H2O.
(6)实验中提供的硼镁泥共100g,得到的MgSO4?7H2O为172.2g,则MgSO4?7H2O的产率为 .
查看习题详情和答案>>

根据题意回答问题:
(1)实验中需用1mol/L的硫酸800mL,若用98%的浓硫酸(ρ=1.84g/mL)来配制,量取浓硫酸时,需使用的量筒的规格为
A.10mL B.20mL C.50mL D.100mL
(2)加入的NaClO可与Mn2+反应:Mn2++ClO-+H2O→MnO2↓+2H++Cl-,还有一种离子也会被NaClO氧化,该反应的离子方程式为
(3)滤渣的主要成份除含有Fe(OH)3、Al(OH)3外,还有
(4)在“除钙”前,需检验滤液中Fe3+是否被除尽,简述检验方法
(5)已知MgSO4、CaSO4的溶解度如下表:
| 温度(℃) | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
(6)实验中提供的硼镁泥共100g,得到的MgSO4?7H2O为172.2g,则MgSO4?7H2O的产率为