摘要:3].下列过程中属于化学变化的是:①白色的硫酸铜粉置于潮湿空气中变成蓝色,②同素异形体之间的互变, ③久置的氯水变色,④同分异构体之间的互变,⑤氯化铵受热分解,⑥氯化钠溶液通电后导电 A.只有①②④⑤ B.只有①④⑤ C.只有①②③④⑤ D.全部
网址:http://m.1010jiajiao.com/timu3_id_387774[举报]
某化学小组在讨论鉴别稀酸和浓硫酸的实验时,设计了如下表格.请按照给出的甲方案的式样,写出另外三种不同的鉴别方法.
(1)甲、乙两同学欲对上述整套装置检查气密性:
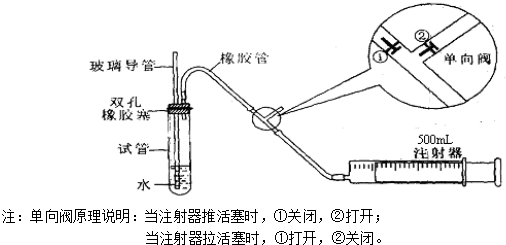
甲同学是用手捂住试管(或微热试管),观察导管中是否有液面上升的现象.是否能? (填能或不能);
乙同学是先从玻璃导管向试管中注入水,观察导管中液面与试管中液面是否形成高度差,且在一段时间后,观察液面差是否变化的方法.是否能? (填能或不能);
若上述两种方案均不能,请思考新方案,并填下列空白(若上述可行,则不填下列空白):先在试管中装入适量水(保证玻璃导管的下端浸没在水中),然后(填操作方法) ,看到 (填实验现象),证明该装置的气密性良好.
(2)向试管中加入0.00127%的碘水10g,用适量的蒸馏水稀释后,再加入2~3滴淀粉溶液,配置成溶液A.测定指定地点空气中SO2的含量时,推拉注射器的活塞反复抽气,试管中发生的化学反应方程式为SO2+I2+2H2O=H2SO4+2HI,A溶液由 色变为 时表明反应恰好完全进行,此时应停止抽气.
(3)我国环境空气质量标准中对每次空气质量测定中SO2的最高浓度限值(mg/m3):一级标准:0.15;二级标准:0.50;三级标准:0.70.该课外活动小组分成第一活动小组和第二活动小组,使用相同的实验装置和溶液A,在同一地点、同时测量空气中SO2的含量.当反应恰好完全进行,记录抽气时间和次数如下(假定每次抽气500mL).请将下表填写完整(计算时保留2位有效数字):
①在实验过程中,需缓缓抽动活塞的目的是 ;若快速抽拉,则测定的结果将 (填偏大、偏小或无影响);
②判断该地点的空气中SO2含量属于 (填数字)级标准, (填“第一”或“第二”)小组的测定结果准确,另一小组实验结果产生较大偏差的原因是 (两个小组所用药品和装置均无问题).
查看习题详情和答案>>
| 方案 | 操作 | 结论 |
| 甲 | 分别加入到盛水的试管中 | 放热者为浓硫酸 |
| 乙 | ||
| 丙 | ||
| 丁 |

甲同学是用手捂住试管(或微热试管),观察导管中是否有液面上升的现象.是否能?
乙同学是先从玻璃导管向试管中注入水,观察导管中液面与试管中液面是否形成高度差,且在一段时间后,观察液面差是否变化的方法.是否能?
若上述两种方案均不能,请思考新方案,并填下列空白(若上述可行,则不填下列空白):先在试管中装入适量水(保证玻璃导管的下端浸没在水中),然后(填操作方法)
(2)向试管中加入0.00127%的碘水10g,用适量的蒸馏水稀释后,再加入2~3滴淀粉溶液,配置成溶液A.测定指定地点空气中SO2的含量时,推拉注射器的活塞反复抽气,试管中发生的化学反应方程式为SO2+I2+2H2O=H2SO4+2HI,A溶液由
(3)我国环境空气质量标准中对每次空气质量测定中SO2的最高浓度限值(mg/m3):一级标准:0.15;二级标准:0.50;三级标准:0.70.该课外活动小组分成第一活动小组和第二活动小组,使用相同的实验装置和溶液A,在同一地点、同时测量空气中SO2的含量.当反应恰好完全进行,记录抽气时间和次数如下(假定每次抽气500mL).请将下表填写完整(计算时保留2位有效数字):
| 分组 | 第一小组 | 第二小组 |
| 抽气时间 | 20分钟 | 21分钟 |
| 抽气次数 | 100 | 130 |
| SO2含量mg/m3 |
②判断该地点的空气中SO2含量属于
Ⅰ.某化学兴趣小组对下列三组物质进行研究:
A.HCl H2SO4 H2CO3 HNO3
B.溶液 水 悬浊液 胶体
C.Na2CO3 NaNO3 AgNO3 Ba(NO3)2
请你帮他们完善下列空白:
| | A | B | C |
| 分类标准 | 含氧酸 | 分散系 | |
| 不属于该类别的物质 | | | Na2CO3 |
Ⅱ.现有下列物质:①铝 ②氢氧化铁胶体 ③氯化氢 ④SO2 ⑤NaHSO4固体 ⑥Ba(OH)2固体 ⑦稀硫酸 ⑧醋酸 ⑨烧碱 ⑩熔融NaNO3
(1)按物质的分类方法填写表格的空白处:(填编号)
| 分类标准 | 能导电的物质[ | 电解质 | 强电解质 |
| 属于该类的物质 | | | |
(2)①与⑨的溶液反应的离子方程式为
(3)用Fe(OH)3胶体进行下列实验:
(a)将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附的颜色逐渐变 (填“深”或“浅”),这表明 。
(b)向其中逐滴加入过量稀硫酸溶液,现象是_______ _______;
(4)向Ba(OH)2溶液逐滴加入NaHSO4溶液至恰好不再生成沉淀为止,写出此步的离子方程式 。 查看习题详情和答案>>
Ⅰ.某化学兴趣小组对下列三组物质进行研究:
A.HCl H2SO4 H2CO3 HNO3
B.溶液 水 悬浊液 胶体
C.Na2CO3 NaNO3 AgNO3 Ba(NO3)2
请你帮他们完善下列空白:
Ⅱ.现有下列物质:①铝 ②氢氧化铁胶体 ③氯化氢 ④SO2 ⑤NaHSO4固体 ⑥Ba(OH)2固体 ⑦稀硫酸 ⑧醋酸 ⑨烧碱 ⑩熔融NaNO3
(1)按物质的分类方法填写表格的空白处:(填编号)
(2)①与⑨的溶液反应的离子方程式为
(3)用Fe(OH)3胶体进行下列实验:
(a)将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附的颜色逐渐变 (填“深”或“浅”),这表明 。
(b)向其中逐滴加入过量稀硫酸溶液,现象是_______ _______;
(4)向Ba(OH)2溶液逐滴加入NaHSO4溶液至恰好不再生成沉淀为止,写出此步的离子方程式 。
A.HCl H2SO4 H2CO3 HNO3
B.溶液 水 悬浊液 胶体
C.Na2CO3 NaNO3 AgNO3 Ba(NO3)2
请你帮他们完善下列空白:
| | A | B | C |
| 分类标准 | 含氧酸 | 分散系 | |
| 不属于该类别的物质 | | | Na2CO3 |
Ⅱ.现有下列物质:①铝 ②氢氧化铁胶体 ③氯化氢 ④SO2 ⑤NaHSO4固体 ⑥Ba(OH)2固体 ⑦稀硫酸 ⑧醋酸 ⑨烧碱 ⑩熔融NaNO3
(1)按物质的分类方法填写表格的空白处:(填编号)
| 分类标准 | 能导电的物质[ | 电解质 | 强电解质 |
| 属于该类的物质 | | | |
(2)①与⑨的溶液反应的离子方程式为
(3)用Fe(OH)3胶体进行下列实验:
(a)将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附的颜色逐渐变 (填“深”或“浅”),这表明 。
(b)向其中逐滴加入过量稀硫酸溶液,现象是_______ _______;
(4)向Ba(OH)2溶液逐滴加入NaHSO4溶液至恰好不再生成沉淀为止,写出此步的离子方程式 。
(2011?宝鸡三模)A、B、C、.D都是中学化学常见的物质,其中A、B、C均含有同一种元素.在一定条件下相互转化关系如图所示(部分产物已略去).
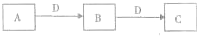
请按要求回答下列问题:
(1)若B、C为两种氧化物气体,B转化为C时,颜色由无色变为红棕色,则A可能是
(2)若A是一种常见的含有两个碳原子的有机物,且A和C反应生成一种有水果香味的物质.写出A与C生成水果香味的物质的反应方程式
(3)若A、B、C、D不仅满足上述转化关系,而且A和C在溶液中通过反应生成B.请回答下面三个问题:
①若D为强电解质、B为难溶于水的沉淀时,则A和C反应的离子方程式是
a.硫酸 b.醋酸 c.氢氧化钠 d.氨水 e.氯化钡. f.硝酸镁
②若D为非电解质时、B为难溶于水的沉淀时,则A和C反应的离子方程式是
③若C、D均为金属单质,向A溶液中滴加硝酸银溶液,产生不溶于稀硝酸的白色沉淀,则A和C反应的离子方程式是
查看习题详情和答案>>

请按要求回答下列问题:
(1)若B、C为两种氧化物气体,B转化为C时,颜色由无色变为红棕色,则A可能是
N2
N2
或NH3
NH3
.(2)若A是一种常见的含有两个碳原子的有机物,且A和C反应生成一种有水果香味的物质.写出A与C生成水果香味的物质的反应方程式
CH3CH2OH+CH3COOH
CH3COOCH2CH3+H2O
| 浓硫酸 |
| △ |
CH3CH2OH+CH3COOH
CH3COOCH2CH3+H2O
.| 浓硫酸 |
| △ |
(3)若A、B、C、D不仅满足上述转化关系,而且A和C在溶液中通过反应生成B.请回答下面三个问题:
①若D为强电解质、B为难溶于水的沉淀时,则A和C反应的离子方程式是
Al3++3AlO2-+6H2O=4Al(OH)3↓
Al3++3AlO2-+6H2O=4Al(OH)3↓
.符合条件的D物质可能是下列物质中的ac
ac
(填序号).a.硫酸 b.醋酸 c.氢氧化钠 d.氨水 e.氯化钡. f.硝酸镁
②若D为非电解质时、B为难溶于水的沉淀时,则A和C反应的离子方程式是
Ca2++OH-+HCO3-=CaCO3↓+H2O
Ca2++OH-+HCO3-=CaCO3↓+H2O
.③若C、D均为金属单质,向A溶液中滴加硝酸银溶液,产生不溶于稀硝酸的白色沉淀,则A和C反应的离子方程式是
2Fe3++Fe=3Fe2+
2Fe3++Fe=3Fe2+
,B溶液在储存时应加入少量的铁与盐酸
铁与盐酸
.X、Y、Z、L、M五种元素的原子序数依次增大.X、Y、Z、L是组成蛋白质的基础元素,M是生活中最常用的金属,它与L可以形成三种化合物.
请回答下列问题:
(1)Y在元素周期表中的位置为
(2)硒(se)是人体必需的微量元素,与L同一主族,该族2~5周期元素单质分别与H2反应生成l mol气态氢化物的反应热如下,表示生成1mol硒化氢反应热的是
a.+99.7mol?L-1 b.+29.7mol?L-1 c.-20.6mol?L-1 d.-241.8kJ?mol-1
(3)已知(YZ)2分子所有的原子都满足8电子,请写出其结构式
(4)L、X两元素按原子数目比l:1和1:2形成分子A和B.
①用电子式表示B的形成过程
 .
.
②M在高温下可以与B反应,写出该反应的化学方程式
某同学将反应得到的黑色粉末全部溶于足量的硫酸溶液中,发现有少量的气泡产生,溶液呈棕黄色,该同学判断溶液中一定同时存在两种M的金属阳离子.请你选择合适的试剂与合理的步骤证明该同学的推断
③若该同学将上述棕黄色溶液1mL加入到2mL A的浓溶液中,预计会看到的实验现象是
查看习题详情和答案>>
请回答下列问题:
(1)Y在元素周期表中的位置为
第二周期,第ⅣA族
第二周期,第ⅣA族
.(2)硒(se)是人体必需的微量元素,与L同一主族,该族2~5周期元素单质分别与H2反应生成l mol气态氢化物的反应热如下,表示生成1mol硒化氢反应热的是
b
b
(填字母代号).a.+99.7mol?L-1 b.+29.7mol?L-1 c.-20.6mol?L-1 d.-241.8kJ?mol-1
(3)已知(YZ)2分子所有的原子都满足8电子,请写出其结构式
N≡C-C≡N
N≡C-C≡N
;(YZ)2可以与X2化合生成XYZ,其水溶液是一种酸,某浓度该酸的钾盐(KYZ)溶液能使酚酞溶液显红色,请用离子方程式表示原因CN-+H2O HCN+OH-
HCN+OH-
 HCN+OH-
HCN+OH-CN-+H2O HCN+OH-
HCN+OH-
. HCN+OH-
HCN+OH-(4)L、X两元素按原子数目比l:1和1:2形成分子A和B.
①用电子式表示B的形成过程


②M在高温下可以与B反应,写出该反应的化学方程式
3Fe+4H2O
Fe3O4+4H2↑
| ||
3Fe+4H2O
Fe3O4+4H2↑
.
| ||
某同学将反应得到的黑色粉末全部溶于足量的硫酸溶液中,发现有少量的气泡产生,溶液呈棕黄色,该同学判断溶液中一定同时存在两种M的金属阳离子.请你选择合适的试剂与合理的步骤证明该同学的推断
取溶液少许,滴加KSCN溶液,溶液变红色,证明有Fe3+,另取溶液少许,加入KMnO4酸性溶液,紫色褪去,证明有Fe2+.
取溶液少许,滴加KSCN溶液,溶液变红色,证明有Fe3+,另取溶液少许,加入KMnO4酸性溶液,紫色褪去,证明有Fe2+.
.③若该同学将上述棕黄色溶液1mL加入到2mL A的浓溶液中,预计会看到的实验现象是
有大量气泡出现
有大量气泡出现
.