网址:http://m.1010jiajiao.com/timu3_id_387578[举报]
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式
(2)若将(1)中的反应设计成原电池,请在右边方框内画出原电池的装置图,标出正、负极,并写出电极反应式.
正极反应
(3)腐蚀铜板后的混合溶液中,若Cu2+、Fe3+和Fe2+的浓度均为0.10mol/L,请参照下表给出的数据和药品,简述除去CuCl2溶液中Fe3+和Fe2+的实验步骤
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ Fe2+ Cu2+ |
1.9 7.0 4.7 |
3.2 9.0 6.7 |
| 提供的药品:Cl2 浓H2SO4 NaOH溶液 CuO Cu | ||
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式___________________________________。
(2)若将(1)中的反应设计成原电池,请画出原电池的装置图,标出正、负极,并写出电极反应式。
正极反应:_______________________________________,
负极反应:_______________________________________。
(3)
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH |
Fe3+ Fe2+ Cu2+ | 1.9 7.0 4.7 | 3.2 9.0 6.7 |
提供的药品:Cl2、浓H2SO4、NaOH溶液、CuO、Cu | ||
某科研人员发现劣质不锈钢在酸中腐蚀缓慢,但在某些盐溶液中腐蚀现象明显。请从上表提供的药品中选择两种(水可任选),设计最佳实验,验证劣质不锈钢易被腐蚀。
有关反应的化学方程式___________________、___________________,劣质不锈钢腐蚀的实验现象_______________________________________________________________。
查看习题详情和答案>>铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂
![]() 等。
等。![]()
![]()
![]()
![]()
![]() (1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式 。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式 。
![]() (2)若将(1)中的反应设计成原电池,请画出原电池的装置图,标出正、负极,并写出电极反应式。
(2)若将(1)中的反应设计成原电池,请画出原电池的装置图,标出正、负极,并写出电极反应式。
![]() 正极反应 负投反应 。
正极反应 负投反应 。
![]() (3)腐蚀铜板后的混合溶液中,若Cu2+、Fe3+和Fe2+的浓度均为0.10mol·L-1,请参照下表给出的数据和药品,简述除去CuCl2溶液中Fe3+和Fe2+的实验步骤 。
(3)腐蚀铜板后的混合溶液中,若Cu2+、Fe3+和Fe2+的浓度均为0.10mol·L-1,请参照下表给出的数据和药品,简述除去CuCl2溶液中Fe3+和Fe2+的实验步骤 。
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+
| 1.9
| 3.2
|
| 提供的药品:Cl2 浓H2SO4 NaOH溶液 CuO Cu | ||
(4)某科研人员发现劣质不锈钢在酸中腐蚀缓慢,但在某些盐溶液中腐蚀现象明显。请从上表提供的药品中选择两种(水可任选),设计最佳实验,验证劣质不锈钢易被腐蚀。
![]() 有关反应的化学方程式
有关反应的化学方程式
![]() 劣质不锈钢腐蚀的实验现象
劣质不锈钢腐蚀的实验现象
铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式 。
(2)若将(1)中的反应设计成原电池,请下面的框图中画出原电池的装置图,标出正、负极,并写出电极反应式。

正极反应: ,
负极反应: 。
(3)腐蚀铜板后的混合溶液中,若Cu2+、Fe3+和Fe2+的浓度均为0.10 mol·L-1,请参照下表给出的数据和药品,简述除去CuCl2溶液中Fe3+和Fe2+的实验步骤:
。
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ Fe2+ Cu2+ | 1.9 7.0 4.7 | 3.2 9.0 6.7 |
| 提供的药品: Cl2 浓H2SO4 溶液NaOH CuO Cu | ||
(4)某科研人员发现劣质不锈钢在酸中腐蚀缓慢,但在某些盐溶液中腐蚀现象明显。请从上表提供的药品中选择两种(水可任选),设计最佳实验,验证劣质不锈钢易被腐蚀。
有关反应的化学方程式 、
劣质不锈钢腐蚀的实验现象:
查看习题详情和答案>>铁及铁的化合物应用广泛,如 FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出 FeCl3溶液腐蚀印刷电路铜板的离子方程式。 。
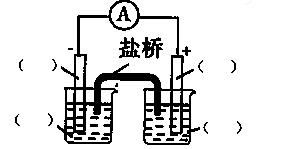
(2)若将(1)中的反应设计成原电池,请补充右边原电池的装置图,在括号内填上正、负极的材料、电解质溶液,并写出电极反应式。正极反应
负极反应
(3)腐蚀铜板后的混合溶液中,若 Cu2+、Fe3+和 Fe2+的浓度均为 0.10mol.L-1,请参照下表给出的数据和药品,简述除去 CuCl2溶液中 Fe3+和Fe2+的实验步骤:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Cu2+ | 4.7 | 6.7 |
| 提供的药品:Cl2 浓H2SO4 NaCl-溶液 CuO Cu | ||
实验步骤:
查看习题详情和答案>>