网址:http://m.1010jiajiao.com/timu3_id_386520[举报]
A、B、C、D、E五种短周期元素,原子序数依次递增,A原子形成的阳离子是一个质子,B原子的最外层电子数是次外层的2倍,C原子的最外层电子数与B原子的核外电子总数相等,D在同周期元素中原子半径最大,而E在同周期元素中原子半径最小。A、C、D三种元素可形成化合物甲,B、C、D三种元素可形成化合物乙,甲和乙均为中学化学常见物质。请回答:
(1)甲的电子式为 ,其中所含化学键类型为 。
(2)A的单质与C的单质在碱性条件下构成燃料电池,其正极反应式为 ;负极反应式 为。
(3)常温下,甲与乙的水溶液pH均为9,这两种溶液中由水电离出的OH—的物质的量浓度c(OH—)甲:c(OH—)乙= .
(4)A与C、D与C可形成化合物A2C、A2C2、D2C、D2C2,说出的一种用途 ;
写出A2C2与E的单质反应的化学方程式 。
(5)浓氨水与固体甲混合,可用于快速制取少量氨气,其原因是
(请用必要的方程式和简要的文字加以说明)。
查看习题详情和答案>>A、B、C、D、E五种短周期元素,原子序数依次递增,A原子形成的阳离子是一个质子,B原子的最外层电子数是次外层的2倍,C原子的最外层电子数与B原子的核外电子总数相等,D在同周期元素中原子半径最大,而E在同周期元素中原子半径最小。A、C、D三种元素可形成化合物甲,B、C、D三种元素可形成化合物乙,甲和乙均为中学化学常见物质。请回答:
(1)甲的电子式为 ,其中所含化学键类型为 。
(2)A的单质与C的单质在碱性条件下构成燃料电池,其正极反应式为 ;负极反应式 为。
(3)常温下,甲与乙的水溶液pH均为9,这两种溶液中由水电离出的OH—的物质的量浓度c(OH—)甲:c(OH—)乙= .
(4)A与C、D与C可形成化合物A2C、A2C2、D2C、D2C2,说出的一种用途 ;
写出A2C2与E的单质反应的化学方程式 。
(5)浓氨水与固体甲混合,可用于快速制取少量氨气,其原因是
(请用必要的方程式和简要的文字加以说明)。
已知:E为常见金属,C、D、F、I均为常见气体,其中C、D为单质,F、I为化合物,且组成元素相同,D、F有毒,I为直线型非极性分子,B的结构为三角双锥(如图所示),图中○代表F分子,●代表E原子,它们有如下框图关系:
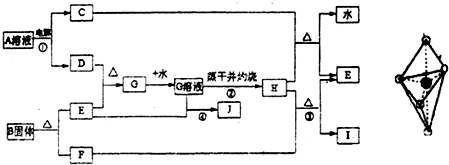
(1)H的颜色是______;B的化学式是______;I的电子式是______.
(2)反应①阳极的电极反应式______.
(3)反应③的化学方程式是______,该反应在工业上的用途是______.
(4)反应④的离子方程式______.
(5)从G溶液制得G的结晶水合物的操作是______.
(6)反应②蒸干并灼烧最终得H而不是无水的G,试用简要文字和方程式解释:______.
查看习题详情和答案>>
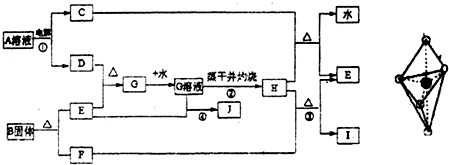
(1)H的颜色是______;B的化学式是______;I的电子式是______.
(2)反应①阳极的电极反应式______.
(3)反应③的化学方程式是______,该反应在工业上的用途是______.
(4)反应④的离子方程式______.
(5)从G溶液制得G的结晶水合物的操作是______.
(6)反应②蒸干并灼烧最终得H而不是无水的G,试用简要文字和方程式解释:______.
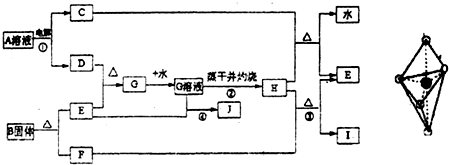
(1)H的颜色是
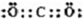
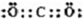
(2)反应①阳极的电极反应式
(3)反应③的化学方程式是
| ||
| ||
(4)反应④的离子方程式
(5)从G溶液制得G的结晶水合物的操作是
(6)反应②蒸干并灼烧最终得H而不是无水的G,试用简要文字和方程式解释:
| ||
| ||