摘要:29. 已知Cl2.Al2(SO4)3.CaC2.C2H5Br.CH3COCH3等物质均能与水反应.反应中各物质和水分别解离成两部分.然后两两重新组合形成新的物质.今有下列五种物质.常温下很容易与水发生反应: 试问: (1)在后面所给出的五种物质与水反应的产物中.属于最高价氧化物的水化物的是 .属于无氧酸的是 . (2)分别将0.01 mol的这五种物质放入0.1 L水中反应.结果使溶液的pH值接近3的原物质是 .
网址:http://m.1010jiajiao.com/timu3_id_386050[举报]
SnCl4的制备需分两步进行:第一步是金属Sn的制备,第二步由Sn和Cl2反应生成SnCl4.
第一步:金属Sn的制备--以锡石SnO2为原料,用足量的焦炭作还原剂,在高温下可制得粗锡,该反应的化学方程式为
已知锡与碳同族,粗锡经电解精炼可得纯锡,精炼时的阴极反应式为
第二步:SnCl4的制备--用干燥、纯净的Cl2与熔融的Sn反应制SnCl4,同时放出大量的热.已知SnCl4常温下是无色液体,沸点114℃,遇潮湿空气便发生水解反应,Sn的熔点:231℃,如图1是制取SnCl4的实验装置.

试回答以下问题:
(1)本试验中检查制气装置A气密性的方法是
装置A中反应的化学方程式为
(2)装置B、C中的药品名称分别是
(3)当反应生成SnCl4时,应熄灭
(4)老师说该实验装置E设计仍不完整,请你协助该研究小组设计出所缺装置(须标出试剂的名称,装置图尽可能简单)并在图2的方框中画出.
(5)实验制得的SnCl4中因溶解了Cl2而略显黄色.提纯SnCl4的方法是
查看习题详情和答案>>
第一步:金属Sn的制备--以锡石SnO2为原料,用足量的焦炭作还原剂,在高温下可制得粗锡,该反应的化学方程式为
SnO2+2C
Sn+2CO
| ||
SnO2+2C
Sn+2CO
.
| ||
已知锡与碳同族,粗锡经电解精炼可得纯锡,精炼时的阴极反应式为
Sn2++2eˉ=Sn
Sn2++2eˉ=Sn
.第二步:SnCl4的制备--用干燥、纯净的Cl2与熔融的Sn反应制SnCl4,同时放出大量的热.已知SnCl4常温下是无色液体,沸点114℃,遇潮湿空气便发生水解反应,Sn的熔点:231℃,如图1是制取SnCl4的实验装置.

试回答以下问题:
(1)本试验中检查制气装置A气密性的方法是
将A右端导管放人盛有水的烧杯中,微热烧瓶导管口出现气泡,冷却导管中出现一段稳定水柱
将A右端导管放人盛有水的烧杯中,微热烧瓶导管口出现气泡,冷却导管中出现一段稳定水柱
.装置A中反应的化学方程式为
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
| ||
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
.
| ||
(2)装置B、C中的药品名称分别是
饱和食盐水
饱和食盐水
、浓硫酸
浓硫酸
.(3)当反应生成SnCl4时,应熄灭
D
D
处的酒精灯,理由是依靠反应放出的热量维持SnCl4的生成
依靠反应放出的热量维持SnCl4的生成
.(4)老师说该实验装置E设计仍不完整,请你协助该研究小组设计出所缺装置(须标出试剂的名称,装置图尽可能简单)并在图2的方框中画出.
(5)实验制得的SnCl4中因溶解了Cl2而略显黄色.提纯SnCl4的方法是
蒸馏
蒸馏
.A、B、C、D、E、F、G、H、I、J 均为有机化合物,其转化关系如图所示.已知B 和 C 均为有支链的有机化合物;C在反应③中只能生成一种有机产物;G能使溴的四氯化碳溶液褪色.回答问题: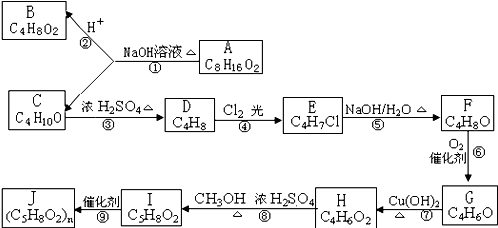
(1)G的结构简式: .⑦的反应类型 .
(2)步骤⑤的化学方程式 .
(3)A在隔绝加热条件下可发生消去反应得到D,请写出该消去反应中除D外的另一个产物的结构简式 .
(4)步骤④中的“Cl2、光”能否改为“饱和氯水”?请说明原因:
(5)写出与H 具有相同官能团的同分异构体的结构简式
(6)在一定条件下,酯与醇会发生酯交换,生成新的酯和醇.请尝试书写I与F发生的酯交换反应方程式: .
(7)一定条件下,G和H发生1:1聚合,聚合产物有多种.写出其中两种聚合产物的结构简式: .
查看习题详情和答案>>

(1)G的结构简式:
(2)步骤⑤的化学方程式
(3)A在隔绝加热条件下可发生消去反应得到D,请写出该消去反应中除D外的另一个产物的结构简式
(4)步骤④中的“Cl2、光”能否改为“饱和氯水”?请说明原因:
(5)写出与H 具有相同官能团的同分异构体的结构简式
(6)在一定条件下,酯与醇会发生酯交换,生成新的酯和醇.请尝试书写I与F发生的酯交换反应方程式:
(7)一定条件下,G和H发生1:1聚合,聚合产物有多种.写出其中两种聚合产物的结构简式:
(2013?丰台区二模)工业上用某矿渣(含有Cu2O、Al2O3、Fe2O3、SiO2)提取铜的操作流程如下:
已知:Cu2O+2H+=Cu+Cu2++H2O
(1)固体混合物A中的成分是
(2)反应Ⅰ完成后,铁元素的存在形式为
请写出生成该离子的离子方程式
(3)x、y对应的数值范围分别是
(4)电解法获取Cu时,阴极反应式为
(5)下列关于NaClO调pH的说法正确的是
a.加入NaClO可使溶液的pH降低
b.NaClO能调节pH的主要原因是由于发生反应ClO-+H+?HClO,ClO-消耗H+,从而达到调节pH的目的
c.NaClO能调节pH的主要原因是由于NaClO水解ClO-+H2O?HClO+OH-,OH-消耗H+,从而达到调节pH的目的
(6)用NaClO调pH,生成沉淀B的同时生成一种具有漂白作用的物质,该反应的离子方程式为
查看习题详情和答案>>

已知:Cu2O+2H+=Cu+Cu2++H2O
| 沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀pH | 5.4 | 4.0 | 1.1 | 5.8 |
| 沉淀完全pH | 6.7 | 5.2 | 3.2 | 8.8 |
SiO2、Cu
SiO2、Cu
.(2)反应Ⅰ完成后,铁元素的存在形式为
Fe2+
Fe2+
.(填离子符号)请写出生成该离子的离子方程式
2Fe3++Cu=Cu2++2Fe2+
2Fe3++Cu=Cu2++2Fe2+
.(3)x、y对应的数值范围分别是
3.2≤pH<4.0
3.2≤pH<4.0
、5.2≤pH<5.4
5.2≤pH<5.4
.(4)电解法获取Cu时,阴极反应式为
Cu2++2e-=Cu
Cu2++2e-=Cu
,阳极反应式为2Cl--2e-=Cl2↑
2Cl--2e-=Cl2↑
.(5)下列关于NaClO调pH的说法正确的是
b
b
.a.加入NaClO可使溶液的pH降低
b.NaClO能调节pH的主要原因是由于发生反应ClO-+H+?HClO,ClO-消耗H+,从而达到调节pH的目的
c.NaClO能调节pH的主要原因是由于NaClO水解ClO-+H2O?HClO+OH-,OH-消耗H+,从而达到调节pH的目的
(6)用NaClO调pH,生成沉淀B的同时生成一种具有漂白作用的物质,该反应的离子方程式为
5ClO-+2Fe2++5H2O=2Fe(OH)3+Cl-+4HClO
5ClO-+2Fe2++5H2O=2Fe(OH)3+Cl-+4HClO
.有机物A由C、H、O、Cl四种元素组成,其相对分子质量为198.5,Cl在侧链上.当A与Cl2分别在Fe作催化剂和光照条件下以物质的量之比为1:1反应时,分别是苯环上一氯取代产物有两种和侧链上一氯取代产物有一种;A与NaHCO3溶液反应时有气体放出.已知A经下列反应可逐步生成B~G.

请你按要求回答下列问题:
(1)A的化学式为
 .
.
(2)上述反应中属于取代反应的是
(3)C中含氧官能团的名称分别为
(4)E的同分异构体中,满足下列条件:①含有苯环,苯环上只有一个侧链,且侧链上只含有一个一CH3;②能发生银镜反应;③属于酯类.请写出一种符合上述条件E的同分异构体的结构简式:
 .
.
(5)写出下列指定反应的化学方程式(有机物写结构简式):
A与NaOH的醇溶液共热: +2NaOH
+2NaOH
 +NaCl+2H2O
+NaCl+2H2O +2NaOH
+2NaOH
 +NaCl+2H2O;
+NaCl+2H2O;
E在一定条件下生成F:
 .
.
查看习题详情和答案>>

请你按要求回答下列问题:
(1)A的化学式为
C10H11O2Cl
C10H11O2Cl
;D的结构简式为

(2)上述反应中属于取代反应的是
①⑥
①⑥
(填编号);(3)C中含氧官能团的名称分别为
羧基、羟基
羧基、羟基
;(4)E的同分异构体中,满足下列条件:①含有苯环,苯环上只有一个侧链,且侧链上只含有一个一CH3;②能发生银镜反应;③属于酯类.请写出一种符合上述条件E的同分异构体的结构简式:


(5)写出下列指定反应的化学方程式(有机物写结构简式):
A与NaOH的醇溶液共热:
 +2NaOH
+2NaOH| 醇 |
| △ |
 +NaCl+2H2O
+NaCl+2H2O +2NaOH
+2NaOH| 醇 |
| △ |
 +NaCl+2H2O
+NaCl+2H2OE在一定条件下生成F:


透明聚酯玻璃钢可用于制造导弹的雷达罩和宇航员使用的氧气瓶.制备它的一种配方中含有下列四种物质:
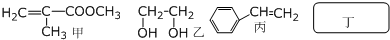
填写下列空白:
(1)下列试剂能与甲反应而褪色的是
a.Br2/CCl4溶液 b.石蕊溶液 c.酸性KMnO4溶液
(2)甲的同分异构体有多种,写出其中一种不含甲基的羧酸的结构简式:
(3)淀粉通过下列转化可以得到乙(其中A~D均为有机物):
淀粉
A
B
C
D
乙
B的分子式是
已知:
(4)根据上述信息,以苯、乙烯、氯化氢为原料经三步反应合成丙,写出其中属于取代反应的化学方程式
(5)化合物丁含碳、氢、氧三种元素,相对分子质量为110,丁与FeCl3溶液作用显现特有的紫色,且丁分子中苯环上的一氯代物只有一种,丁的结构简式为
 .
.
查看习题详情和答案>>
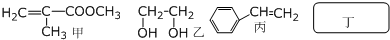
填写下列空白:
(1)下列试剂能与甲反应而褪色的是
ac
ac
(填标号)a.Br2/CCl4溶液 b.石蕊溶液 c.酸性KMnO4溶液
(2)甲的同分异构体有多种,写出其中一种不含甲基的羧酸的结构简式:
CH2=CH-CH2-CH2-COOH
CH2=CH-CH2-CH2-COOH
.(3)淀粉通过下列转化可以得到乙(其中A~D均为有机物):
淀粉
| 稀硫酸 |
| △ |
| 一定条件 |
| 浓硫酸 |
| 170℃ |
| 试剂X |
| NaOH溶液 |
| △ |
B的分子式是
C2H6O
C2H6O
,试剂X可以是Br2/CCl4(或Cl2/CCl4或X2/CCl4)
Br2/CCl4(或Cl2/CCl4或X2/CCl4)
.已知:

(4)根据上述信息,以苯、乙烯、氯化氢为原料经三步反应合成丙,写出其中属于取代反应的化学方程式
CH3CH2Cl+C6H6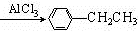 +HCl
+HCl
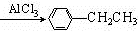 +HCl
+HClCH3CH2Cl+C6H6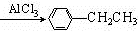 +HCl
+HCl
.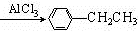 +HCl
+HCl(5)化合物丁含碳、氢、氧三种元素,相对分子质量为110,丁与FeCl3溶液作用显现特有的紫色,且丁分子中苯环上的一氯代物只有一种,丁的结构简式为

