网址:http://m.1010jiajiao.com/timu3_id_385803[举报]
(14分) CO2、SO2、NOx是对环境影响较大的气体,控制和治理CO2、SO2、NOx是解决温室效应、减少酸雨和光化学烟雾的有效途径。
(1)下列措施中,有利于降低大气中的CO2、SO2、NOx浓度的是 (填序号)
| A.减少化石燃料的使用,开发新能源 |
| B.使用无氟冰箱,减少氟利昂排放 |
| C.多步行或乘公交车,少用私家车 |
| D.将工业废气用碱液吸收后再排放 |
①若A为CO2,B为H2,C为CH3OH,则正极的电极反应式为 ;
②若A为SO2,B为O2,C为H2SO4,则负极的电极反应式为 ;
当电路中有1 mol e-流过,正极区溶液中的H+的物质的量的变化量
 n(H+)= mol。
n(H+)= mol。(3)在研究氮的氧化物的转化时,某小组查阅到以下数据:l7℃、l.01×l05Pa时,2NO2(g)
 N2O4(g) △H<0的平衡常数K=13.3。
N2O4(g) △H<0的平衡常数K=13.3。①若该条件下密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.0300mol.L-1,
则c(N2O4)= 。(保留两位有效数字)
②若改变上述体系的某一个条件,达到新的平衡后,测得混合气体中c(NO2)="0.04" mol.L-1,c(N2O4)="0.007" mol.L-1,则改变的条件为 。
(4)为了降低汽车尾气对大气的污染,有关部门拟用甲醇替代作为公交车的燃料。由CO和H2合成甲醇的方法是CO(g)+2H2(g)
 CH3OH(g),己知该反应在300OC时的化学平衡常数为0.27,该温度下将2moI CO、3mol H2利2molCH3OH(g)充入容积为2 L的密闭容器中,此时反应将 。(填“向正反应方向进行”、“向逆反应方向进行”或“处于平衡状态”)。
查看习题详情和答案>>
CH3OH(g),己知该反应在300OC时的化学平衡常数为0.27,该温度下将2moI CO、3mol H2利2molCH3OH(g)充入容积为2 L的密闭容器中,此时反应将 。(填“向正反应方向进行”、“向逆反应方向进行”或“处于平衡状态”)。
查看习题详情和答案>>
(14分) CO2、SO2、NOx是对环境影响较大的气体,控制和治理CO2、SO2、NOx是解决温室效应、减少酸雨和光化学烟雾的有效途径。
(1)下列措施中,有利于降低大气中的CO2、SO2、NOx浓度的是 (填序号)
A、减少化石燃料的使用,开发新能源
B、使用无氟冰箱,减少氟利昂排放
C、多步行或乘公交车,少用私家车
D、将工业废气用碱液吸收后再排放
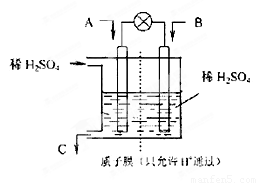
(2)有学者设想以右图所示装置用电化学原理将CO2、SO2转化为重要化工原料。
①若A为CO2,B为H2,C为CH3OH,则正极的电极反应式为 ;
②若A为SO2,B为O2,C为H2SO4,则负极的电极反应式为 ;
当电路中有1 mol e-流过,正极区溶液中的H+的物质的量的变化量 n(H+)=
mol。
n(H+)=
mol。
(3)在研究氮的氧化物的转化时,某小组查阅到以下数据:l7℃、l.01×l05Pa时,2NO2(g) N2O4(g)
△H<0的平衡常数K=13.3。
N2O4(g)
△H<0的平衡常数K=13.3。
①若该条件下密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.0300mol.L-1,
则c(N2O4)= 。(保留两位有效数字)
②若改变上述体系的某一个条件,达到新的平衡后,测得混合气体中c(NO2)=0.04 mol.L-1,c(N2O4)=0.007 mol.L-1,则改变的条件为 。
(4)为了降低汽车尾气对大气的污染,有关部门拟用甲醇替代作为公交车的燃料。由CO和H2合成甲醇的方法是CO(g)+2H2(g) CH3OH(g),己知该反应在300OC时的化学平衡常数为0.27,该温度下将2moI CO、3mol H2利2molCH3OH(g)充入容积为2 L的密闭容器中,此时反应将
。(填“向正反应方向进行”、“向逆反应方向进行”或“处于平衡状态”)。
CH3OH(g),己知该反应在300OC时的化学平衡常数为0.27,该温度下将2moI CO、3mol H2利2molCH3OH(g)充入容积为2 L的密闭容器中,此时反应将
。(填“向正反应方向进行”、“向逆反应方向进行”或“处于平衡状态”)。
查看习题详情和答案>>
(14分).酸碱中和滴定是中学化学常见实验。
Ⅰ右图表示50mL酸式滴定管中液面的位置,如果液面处的读数是a,则滴定管中剩余液体的体积是______mL
A、a B、大于a C、小于(50-a) D、大于(50-a)
Ⅱ 某同学欲测定某浓硫酸样品的物质的量浓度,进行了以下实验操作:
A.冷却至室温后,在100mL容量瓶中定容配成100mL稀硫酸。
B.量取20.00mL稀硫酸于锥形瓶中并滴入几滴指示剂。
C.将酸式滴定管和碱式滴定管用蒸馏水洗涤干净,并用各待盛溶液润洗。
D.将物质的量浓度为1.50mol·L-1标准NaOH溶液装入碱式滴定管,调节液面记下读数V1。
E.继续滴定至终点,记下读数为V2。
F.在锥形瓶下垫一张白纸,把锥形瓶移到碱式滴定管下小心滴入NaOH标准溶液,边滴边摇动锥形瓶。
G.量取浓硫酸样品5mL,在烧杯中用蒸馏水溶解。
H.重复以上实验。
请回答下列问题:
(1)该实验正确操作步骤的顺序为 → A→ → →D→ → → H(用编号字母填写)。
(2)量取5mL浓硫酸的仪器是 ;量取20.00mL稀硫酸的仪器是 。
(3)选用的指示剂是 。滴定过程中,视线应注视 ;判断到达滴定终点的现象是 。
(4)下表是实验测得的有关数据:
|
滴定序号 |
待测稀硫酸的体积(mL) |
所消耗NaOH标准溶液液的体积(mL) |
|
|
V1 |
V2 |
||
|
① |
20.00 |
0.50 |
22.60 |
|
② |
20.00 |
6.00 |
27.90 |
请计算出该浓硫酸样品的浓度为 mol·L-1(不必写出计算过程)。
查看习题详情和答案>>
(14分)孔雀石的主要成分为Cu2(OH)2CO3,还含少量Fe、Si的化合物。实验室以孔雀石为原料制备CuCl2·3H2O及CaCO3的步骤如下:
为解决有关问题,兴趣小组同学查得有关物质沉淀的pH数据如下:
| 物质 | pH (开始沉淀) | pH(完全沉淀) |
| Fe(OH)3 | 1.9 | 3.2 |
| Fe(OH)2 | 7.0 | 9.0 |
| Cu(OH)2 | 4.7 | 6.7 |
⑵操作X包括 、 、过滤和洗涤等。CuCl2·3H2O加热灼烧的最终产物的化学式是 。
⑶某种胃药片的治酸剂为CaCO3,该药片中CaCO3质量分数的测定步骤如下:
a.配制0.1mol·L-1的HCl溶液和0.1mol·L-1的NaOH溶液各250mL。
b.取0.1g磨碎后的胃药于锥形瓶中。
c.向锥形瓶内加入25.00mL 0.1 mol·L-1的HCl溶液。
d.以酚酞为指示剂,用0.1mol·L-1的NaOH溶液滴定,至达到滴定终点。
e.重复bcd三步的操作2次。
①操作c中量取盐酸体积的仪器是 。
②若洗涤后的碱式滴定管未用NaOH溶液润洗,则所测CaCO3的质量分数将 (选填“偏大”、“偏小”或“无影响”)。
③若滴定中NaOH溶液的平均用量为15.00mL,则胃药中碳酸钙的质量分数为 。 查看习题详情和答案>>
(14分).酸碱中和滴定是中学化学常见实验。
Ⅰ右图表示50mL酸式滴定管中液面的位置,如果液面处的读数是a,则滴定管中剩余液体的体积是______mL
A、a B、大于a C、小于(50-a) D、大于(50-a)
Ⅱ 某同学欲测定某浓硫酸样品的物质的量浓度,进行了以下实验操作:
A.冷却至室温后,在100mL容量瓶中定容配成100mL稀硫酸。
B.量取20.00mL稀硫酸于锥形瓶中并滴入几滴指示剂。
C.将酸式滴定管和碱式滴定管用蒸馏水洗涤干净,并用各待盛溶液润洗。
D.将物质的量浓度为1.50mol·L-1标准NaOH溶液装入碱式滴定管,调节液面记下读数V1。
E.继续滴定至终点,记下读数为V2。
F.在锥形瓶下垫一张白纸,把锥形瓶移到碱式滴定管下小心滴入NaOH标准溶液,边滴边摇动锥形瓶。
G.量取浓硫酸样品5mL,在烧杯中用蒸馏水溶解。
H.重复以上实验。
请回答下列问题:
(1)该实验正确操作步骤的顺序为 → A→ → →D→ → → H(用编号字母填写)。
(2)量取5mL浓硫酸的仪器是 ;量取20.00mL稀硫酸的仪器是 。
(3)选用的指示剂是 。滴定过程中,视线应注视 ;判断到达滴定终点的现象是 。
(4)下表是实验测得的有关数据:
| 滴定序号 | 待测稀硫酸的体积(mL) | 所消耗NaOH标准溶液液的体积(mL) | |
| V1 | V2 | ||
| ① | 20.00 | 0.50 | 22.60 |
| ② | 20.00 | 6.00 | 27.90 |
请计算出该浓硫酸样品的浓度为 mol·L-1(不必写出计算过程)。
查看习题详情和答案>>