网址:http://m.1010jiajiao.com/timu3_id_385524[举报]
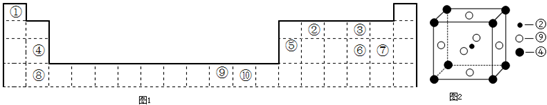
请回答下列问题:
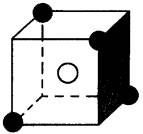
(1)科学发现,②、④、⑨三种元素的原子形成的晶体具有超导性,其晶胞的结构特点如图2所示(图中②、④、⑨分别位于晶胞的体心、顶点、面心),则该化合物的化学式为
(2)元素②的一种氢化物是重要的化工原料,常把该氢化物的产量作为衡量石油化工发展水平的标志.有关该氢化物分子的说法正确的是
A.分子中含有分子间氢键 B.属于含有极性键的非极性分子
C.只含有4个σ键和1个p-p的π键 D.该氢化物分子中②原子采用sp2杂化
(3)某元素的价电子排布式为nsnnpn+1,该元素与元素①形成的18电子的X分子的结构式为
(4)比较③,⑤,⑥,⑦,⑧五种元素的电负性大小,由小到大排列的顺序为
(5)⑩元素单质晶体是面心立方体,立方体的每个面5个⑩原子紧密堆砌,⑩原子半径为d cm,求该金属的密度为
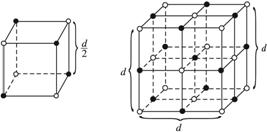
晶体具有规则的几何外形,晶体中最基本的重复单元称为晶胞。NaCl晶体结构如上图所示。已知FexO晶体晶胞结构为NaCl型,由于晶体缺陷,x值小于1。测知FexO晶体密度为ρ=5.71 g·cm-3,晶胞边长为4.28×10-10m。
(1)FexO中x值(精确至0.01)为__________。
(2)晶体中的Fen+分别为Fe2+、Fe3+,在Fe2+和Fe3+的总数中,Fe2+所占分数(用小数表示,精确至0.001)为__________。
(3)此晶体化学式为____________________。
(4)与某个Fe2+(或Fe3+)距离最近且等距离的O2-围成的空间几何形状是__________。
(5)在晶体中,铁元素的离子间最短距离为__________m。
查看习题详情和答案>>
图3
(1)FexO中x值(精确至0.01)为___________________。
(2)晶体中的Fen+分别为Fe2+、Fe3+,在Fe2+和Fe3+的总数中,Fe2+所占分数(用小数表示,精确至0.001)为_______________。
(3)此晶体化学式为_________________。
(4)与某个Fe2+(或Fe3+)距离最近且等距离的O2-围成的空间几何形状是_______________。
(5)在晶体中,铁元素的离子间最短距离为___________m。
查看习题详情和答案>>晶体具有规则的几何外形,晶体中最基本和重复单位称为晶胞。NaCl的晶体结构如图所示。已知FexO晶体晶胞结构为NaCl型,由于晶体缺陷,x值小于1。测知FexO的晶体密度为ρ=5.71g?cm-3,晶胞边长为4.28×10-10m。
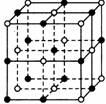
(1)FexO中x值(精确到0.01)为____________。
(2)晶体中的Fe分中Fe2+和Fe3+。其中Fe2+所占分数(用小数表示,精确到0.001)为_____________。
(3)此晶体的化学式:_______________。
(4)与某个Fe2+(或Fe3+)距离最近且等距离为O2-围成的空间几何形状是________。
(5)在晶体中,铁元素的离子间最短距离为____________m。
查看习题详情和答案>>