网址:http://m.1010jiajiao.com/timu3_id_384114[举报]
无水氯化铝是一种重要的化工原料,利用明矾石[K2SO4?Al2(SO4)3?2Al2O3?6H2O]制备无水氯化铝的流程如下:

(1)焙烧炉中产生的SO2直接排放到空气中会形成酸雨,若某地酸雨的pH为4.6,在空气中放置一段时间后,pH变为4.0,其原因为______;(用必要的文字简述).
(2)氯化炉中发生的主要反应为:2Al2O3(s)+6Cl2(g)?4AlCl3(g)+3O2(g)△H>0.反应达平衡时,加焦炭能使平衡向正反应方向移动,理由是______.
(3)生产氯化铝的过程中会产生SO2、Cl2等大气污染物,若将二者按照一定比例通入水中可减少或消除污染.试设计简单实验检验二者是否恰好完全反应.(简要描述实验步骤、现象和结论)______.
仪器自选,可供选择试剂如下:
①滴加酚酞的氢氧化钠溶液 ②氯化亚铁溶液 ③硫氰化钾溶液 ④品红溶液
(4)工业上利用如下装置制备氯气:已知左侧原电池的工作原理为:2Na2S2+NaBr3 Na2S4+3NaBr
Na2S4+3NaBr
①用惰性电极电解饱和食盐水的化学方程式为______.
②如图所示原电池放电时,电池中的Na+向______(填“左槽”或“右槽”)移动.左槽中发生的电极反应式为______.
③该原电池工作一段时间后,测得左槽中Na+物质的量由a mol变为b mol,则电解池中b电极上得到的气体在标准状况下的体积为______L(不考虑气体的损失).
查看习题详情和答案>>
(10分)工业上电解制烧碱的技术是用离子交换膜法,主要原料是饱和食盐水。下图为离子交换膜法电解原理示意图:
请回答下列问题:
(1)电解槽中部的阳离子交换膜把电解槽隔成了阴极室和阳极室,这种阳离子交换膜,只允许溶液中的__________通过(填写下列微粒的编号),而两边的水不能自由流通。
①H+ ② Cl- ③Na+ ④OH-
(2)A极为电解槽的________极,电极反应式为__________________________________,
(3)如果没有阳离子交换膜,阴阳两极的某两种产物在常温下会在溶液中发生反应而使烧碱不纯,其反应的离子方程式为___________ 。
(4)若将标准状况下6.72L的阳极气体通入热的氢氧化钠溶液中,反应中只有一种元素的化合价发生改变,得到了两种含氯化合物,其中还原产物与氧化产物物质的量之比为5:1,写出该反应的离子方程式_____________________________________________。
(10分)工业上电解制烧碱的技术是用离子交换膜法,主要原料是饱和食盐水。下图为离子交换膜法电解原理示意图:

请回答下列问题:
(1)电解槽中部的阳离子交换膜把电解槽隔成了阴极室和阳极室,这种阳离子交换膜,只允许溶液中的__________通过(填写下列微粒的编号),而两边的水不能自由流通。
①H+ ② Cl- ③Na+ ④OH-
(2)A极为电解槽的________极,电极反应式为__________________________________,
(3)如果没有阳离子交换膜,阴阳两极的某两种产物在常温下会在溶液中发生反应而使烧碱不纯,其反应的离子方程式为___________ 。
(4)若将标准状况下6.72L的阳极气体通入热的氢氧化钠溶液中,反应中只有一种元素的化合价发生改变,得到了两种含氯化合物,其中还原产物与氧化产物物质的量之比为5:1,写出该反应的离子方程式_____________________________________________。
查看习题详情和答案>>
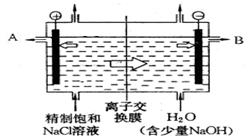
请回答下列问题:
(1)电解槽中部的阳离子交换膜把电解槽隔成了阴极室和阳极室,这种阳离子交换膜,只允许溶液中的__________通过(填写下列微粒的编号),而两边的水不能自由流通。
①H+ ② Cl- ③Na+ ④OH-
(2)A极为电解槽的________极,电极反应式为__________________________________,
(3)如果没有阳离子交换膜,阴阳两极的某两种产物在常温下会在溶液中发生反应而使烧碱不纯,其反应的离子方程式为___________ 。
(4)若将标准状况下6.72L的阳极气体通入热的氢氧化钠溶液中,反应中只有一种元素的化合价发生改变,得到了两种含氯化合物,其中还原产物与氧化产物物质的量之比为5:1,写出该反应的离子方程式_____________________________________________。
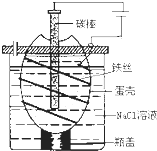 工业上通过电解饱和氯化钠溶液的方法获得氢氧化钠和氯气,图为某实验小组自制的电解饱和食盐水的简易装置,
工业上通过电解饱和氯化钠溶液的方法获得氢氧化钠和氯气,图为某实验小组自制的电解饱和食盐水的简易装置,(1)写出电解饱和氯化钠溶液时,总离子反应方程式:
| ||
| ||
(2)下列有关说法正确的是
A.电解一段时间后,往蛋壳内溶液中滴加几滴
紫色石蕊试液,先变红后又褪色
B.蛋壳表面缠绕铁丝发生氧化反应
C.为增强导电性,可将石墨棒换成铜电极
D.蛋壳可阻止生成的氯气与氢气、氢氧化钠溶液接触
(3)电解200mL 0.5mol/L的NaCl溶液,在标准状况下,阴极收集到2.24L气体时,
阳极产生的气体为
(4)若将电解后阳极所产生的气体全部通入1mol/L 500mL Na2SO3的溶液中,使之充分反应(假设溶液的体积变化忽略不计),则所得溶液中SO42-的物质的量浓度最多为