摘要:23.下表列出了元素周期表中的部分元素: H B C N O F Si P S Cl 锗 As Se Br 锑 Te I 铋 At 117 (1)表中用元素符号所列出的元素除H外.其余非金属元素原子 . a.最外层电子数都大于4 b.主族序数等于周期数 c.最外层电子数都大于电子层数 (2)以下关于元素的性质或用途的叙述正确的是 . a.P.S.Cl等元素的化合物常用来制取农药 b.硅可用于制半导体材料 c.F是最活泼非金属元素.其最高价氧化物的水化物的酸性最强 (3)以下方法可以比较S.Cl非金属性强弱的是 . a.分别测定Na2S溶液和NaCl溶液的pH b.将Fe分别与S.Cl2反应.分析产物中Fe的化合价 c.将H2S通入氯水中.观察到有淡黄色固体析出:H2S + Cl2 → 2HCl + S↓ (4)美俄科学家2006年10月5日宣布他们已制得了118号元素.试分析.若制得117号元素.按元素周期表中金属与非金属的分区.它应是一种 (选填“金属 .“非金属 )元素.写出117号元素最外层电子排布式 .
网址:http://m.1010jiajiao.com/timu3_id_384080[举报]
下表列出了前三周期部分元素在周期表中的位置。请根据表中信息回答下列问题:
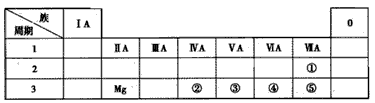
(1)②的元素符号为____。
(2)③,④,⑤中原子半径最大的是____(填元素符号)。
(3) Mg与⑤两种元素形成的化合物为____(填“离子”或“共价”)化合物。
(4)上表中非金属性最强的是____(填元素名称),请用元素周期律的知识说明原因:____。
查看习题详情和答案>>
(2)③,④,⑤中原子半径最大的是____(填元素符号)。
(3) Mg与⑤两种元素形成的化合物为____(填“离子”或“共价”)化合物。
(4)上表中非金属性最强的是____(填元素名称),请用元素周期律的知识说明原因:____。
元素周期表是学习物质结构和性质的重要工具,下面是元素周期表的一部分,表中所列字母A、D、E、G、Q、M、R、T分别代表某一化学元素.请用所给元素回答下列问题.
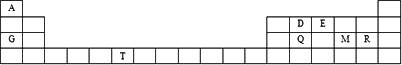
(1)八种元素中,电负性最大的是________,D、E、G、Q四种元素第一电离能由大到小的顺序是________(填元素符号).
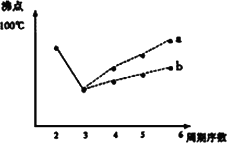
(2)两同学就M同主族的元素的氢化物的沸点的变化趋势画出了两条曲线(如下图),你认为正确的是:________(填“a”或“b”),理由是:________.
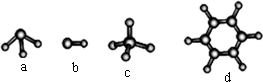
(3)A与D形成分子的空间结构可能是(填序号)________.
(4)写出T原子的基态的核外电子排布式________,TO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断TO2Cl2是________(填“极性”或“非极性”)分子.
下列为元素周期表中的一部分,按要求回答下列问题.
(1)这些元素中最不活泼的元素名称为:
(2)元素⑥⑦⑩的最高价氧化物对应的水化物中碱性最强的是(填化学式):
(3)元素⑨的单质与H2O反应的离子方程式为:
(4)元素③的氧化物与氢氧化钾溶液反应的离子方程式为
(5)元素①④⑩形成的化合物中的化学键类型为:
(6)比较元素⑥⑦⑧⑨离子的半径由大到小的顺序(填化学符号)为:
(7)元素周期表体现了元素周期律,元素周期律的本质是原子核外电子排布的
查看习题详情和答案>>
| ⅠA | 0 | |||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ④ | ⑤ | |||||
| 3 | ⑥ | ⑦ | ③ | ⑧ | ⑨ | |||
| 4 | ⑩ | |||||||
氖
氖
;(2)元素⑥⑦⑩的最高价氧化物对应的水化物中碱性最强的是(填化学式):
KOH
KOH
;(3)元素⑨的单质与H2O反应的离子方程式为:
Cl2+H2O═H++Cl-+HClO
Cl2+H2O═H++Cl-+HClO
;(4)元素③的氧化物与氢氧化钾溶液反应的离子方程式为
Al2O3+2OH-+3H2O=2[Al(OH)4]-
Al2O3+2OH-+3H2O=2[Al(OH)4]-
;(5)元素①④⑩形成的化合物中的化学键类型为:
离子键,共价键
离子键,共价键
.(6)比较元素⑥⑦⑧⑨离子的半径由大到小的顺序(填化学符号)为:
S2->Cl->Na+>Mg2+
S2->Cl->Na+>Mg2+
.(7)元素周期表体现了元素周期律,元素周期律的本质是原子核外电子排布的
周期性变化
周期性变化
,请写出主族元素在元素周期表中的位置与元素原子结构的关系:元素的周期数即为原子核外电子层数,元素的主族序数即为元素原子的最外层电子数
元素的周期数即为原子核外电子层数,元素的主族序数即为元素原子的最外层电子数
.下表给出了X、Y、Z、W四种短周期元素的部分信息,请根据这些信息判断下列说法中正确的是( )
|
查看习题详情和答案>>
下表给出了X、Y、Z、W四种短周期元素的部分信息,请根据这些信息判断下列说法中正确的是( )
| 元素 | X | Y | Z | W |
| 原子半径(nm) | 0.102 | 0.16 | 0.074 | 0.071 |
| 最高正价或最低价 | +6 | +2 | -2 | -1 |
A.原子序数X<Y<W<Z B.纯净的X与纯净的Z反应生成XZ3
C.Z的最高正价为+6 D.HW是热稳定性最强的氢化物
查看习题详情和答案>>