网址:http://m.1010jiajiao.com/timu3_id_383306[举报]
某校科技小组的同学们采集酸雨样品,每隔一段时间测定样品的pH,得到下列数据:
| 时间 | 开始 | 8h后 | 16h后 | 24h后 | 32h后 | 40h后 | 48h后 |
| pH | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 | 4.0 |
(1)酸雨放置时,pH发生变好的主要原因为
(2)煤中含有游离态的硫,试写出它经过一系列变化最后变成酸雨主要成分的有关化学方程式.(空线不一定填满)
| ||
| ||
B.有A.B两种烃,它们的组成相同,都约含85.7%的碳,烃A对氢气的相对密度是28;烃B式量比空气的平均式量稍小,且最简式与A相同,烃A.B都能使溴的四氯化碳溶液褪色,根据以上实验事实计算并回答问题.
(1)推算A.B两烃的化学式.(推算步骤写在下面)
A
(2)A、B中
(3)写出B与溴的四氯化碳溶液反应的化学方程式:
回答下列问题:
(1)反应②的主要用途是:
(2)已知反应③中还有一种无色气体生成,写出反应③的离子方程式:
(3)L中两种沉淀为
(4)若将M溶于稀硫酸中可形成溶液Z,请设计简单的实验,证明Z溶液中所含的金属阳离子:

图表法、图象法是常用的科学研究方法.下表列出前20号元素中的某些元素性质的一些数据:
| 元素 性质 |
A | B | C | D | E | F | G | H | I | J |
| 原子半径(10-10m) | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
| 最高价态 | +6 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
| 最低价态 | -2 | - | -2 | - | -4 | -3 | -1 | - | -3 | -4 |
(1)以上10种元素中第一电离能最小的是:
(2)由上述C、E、G三种元素中的某两种元素形成的化合物中,每个原子的最外层都满足8电子稳定结构的可能是
(3)元素E与C及氢元素可形成一种相对分子质量为60的一元羧酸分子.其分子中共形成
(4)短周期某主族元素K的电离能情况如图(A)所示.则K元素位于周期表的第

图B是研究部分元素的氢化物的沸点变化规律的图象,折线c可以表达出第
(15分)氟化钠是一种重要的氟盐,主要用作农业杀菌剂、杀虫剂、木材防腐剂和生产含氟牙膏等。实验室可通过下图所示的流程以氟硅酸(H2SiF6)等物质为原料制取氟化钠,并得到副产品氯化铵:
有关物质在水中溶解度(g/100gH2O)如下:
| 温度 | 10℃ | 20℃ | 30℃ | 溶解度:20℃NaF—4 0℃NH4F—100; 常温Na2SiF6微溶于水 |
| NH4Cl溶解度 | 33.3 | 37.2 | 41.4 |
请回答下列问题:
(1)操作Ⅰ需要用到的玻璃仪器有 。
(2)上述流程中发生两步反应,化学方程式为:
(3)操作II的作用是
操作Ⅲ的具体过程是
(4)流程中NH4HCO3必须过量,其原因是
_______________________________________________________________________
查看习题详情和答案>>
(15分)回答下列问题。
(1) 漂白粉与浓盐酸相遇时有黄绿色气体生成,若产生气体在标准状况下的体积为11.2L,则有 molHCl被氧化。
(2) 向氯水中加入CaCO3固体后,氯水的杀菌、漂白能力将 (填增强或减弱)其原因是 。
(3)二氧化硫气体与含1.5 mol Cl元素的一种含氧酸(该酸的某盐常用于实验室制取氧气)的溶液在一定条件下反应,可生成一种强酸和一种气态氯氧化物A,若有1.5×6.02×1023个电子转移时,该反应的化学方程式是: 。
(4)我国卫生部已明确提出:要逐步用氯的氧化物A替代氯气进行饮用水的消毒。
①氯的氧化物A不稳定,可与NaOH溶液、H2O2反应,Cl元素转化为比较稳定的正三价物质,该反应的化学方程式为 。
② 用氯的氧化物A处理过的自来水中会残留少量A,可用FeCl2将其还原为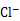 。现用VL(已换算为标准状况) A处理一定量自来水,再加入a mol FeCl2可将残留的A恰好除去,则该自来水中残留A的物质的量为
。
。现用VL(已换算为标准状况) A处理一定量自来水,再加入a mol FeCl2可将残留的A恰好除去,则该自来水中残留A的物质的量为
。
查看习题详情和答案>>