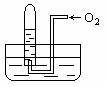
摘要:如图所示.当向试管内通入21mLO2时.最后试管中 的液面仍在原来的位置.则原试管中NO为( ) A.6mL B.12mL C.16mL D.18mL
网址:http://m.1010jiajiao.com/timu3_id_383275[举报]
如图所示,当向大试管中缓缓加入浓硫酸时,烧杯中的水溶液会变浑浊,试回答:
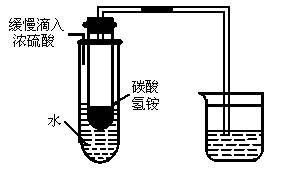
(1)烧杯中所盛的水溶液是_____________;发生反应的化学方程式为_____________________________________。
(2)小试管内的碳酸氢铵发生了什么变化?___________________,写出有关的化学方程式:__________________________。
(3)解释发生上述反应的原因:________________________________
(4)碳酸氢铵化肥应如何使用和保存?_________________________________________。
查看习题详情和答案>>
如图所示,当向大试管中缓缓加入浓硫酸时,烧杯中的水溶液会变浑浊,试回答:
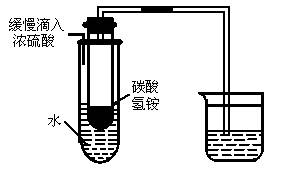
(1)烧杯中所盛的水溶液是_____________;发生反应的化学方程式为_____________________________________。
(2)小试管内的碳酸氢铵发生了什么变化?___________________,写出有关的化学方程式:__________________________。
(3)解释发生上述反应的原因:________________________________
(4)碳酸氢铵化肥应如何使用和保存?_________________________________________。
查看习题详情和答案>>
如图所示是一个制取氯气并以氯气为原料进行特定反应的装置,多余的氯气可以贮存在b瓶中,其中各试剂瓶中所装试剂为:B(氢硫酸)、C(碘化钾淀粉溶液)、D(水)、F(紫色石蕊试液).
(1)若A中烧瓶中的固体为MnO2,液体为浓盐酸,则其发生反应的化学方程式为
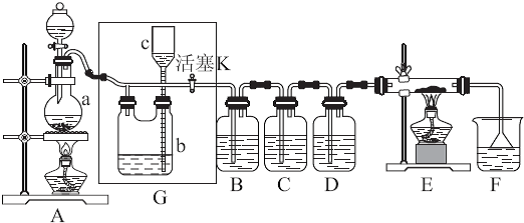
(2)G中b瓶内宜加入的液体是
(3)实验开始后B中的现象是
(4)E装置中硬质玻璃管内盛有炭粉,若E中发生氧化还原反应,其产物为二氧化碳和氯化氢,写出E中反应的化学方程式:
(5)在F中,紫色石蕊试液的颜色由紫色变为红色,再变为无色,其原因是
查看习题详情和答案>>
(1)若A中烧瓶中的固体为MnO2,液体为浓盐酸,则其发生反应的化学方程式为
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
| ||
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
.
| ||

(2)G中b瓶内宜加入的液体是
饱和食盐水
饱和食盐水
,怎样检验装置G的气密性:用止水夹夹住A、G之间的胶管,关闭G中活塞K,从c中向容器内加液体,当c的下端浸入液面且c中液面高于b瓶内液面,静置一段时间,若c中液面不下降,则说明气密性好
用止水夹夹住A、G之间的胶管,关闭G中活塞K,从c中向容器内加液体,当c的下端浸入液面且c中液面高于b瓶内液面,静置一段时间,若c中液面不下降,则说明气密性好
.(3)实验开始后B中的现象是
上部空间由无色变黄绿色,溶液中有浅黄色沉淀生成
上部空间由无色变黄绿色,溶液中有浅黄色沉淀生成
,C中的现象是上部空间由无色变为黄绿色,溶液变蓝色
上部空间由无色变为黄绿色,溶液变蓝色
.(4)E装置中硬质玻璃管内盛有炭粉,若E中发生氧化还原反应,其产物为二氧化碳和氯化氢,写出E中反应的化学方程式:
C+2H2O+2Cl2
CO2+4HCl
| ||
C+2H2O+2Cl2
CO2+4HCl
.
| ||
(5)在F中,紫色石蕊试液的颜色由紫色变为红色,再变为无色,其原因是
E中生成的酸性气体进入F中可使紫色石蕊试液变红,但未反应完的氯气进入F中与水作用生成HClO,HClO具有漂白作用,使溶液的红色褪去
E中生成的酸性气体进入F中可使紫色石蕊试液变红,但未反应完的氯气进入F中与水作用生成HClO,HClO具有漂白作用,使溶液的红色褪去
.如图所示,是一个制取氯气并以氯气为原料进行特定反应的装置,其中各试剂瓶装的试剂为:B(氢硫酸)、C(溴化亚铁溶液)、D(碘化钾淀粉溶液)、E(混有二氧化硫的氯化钡溶液)、F(水)、H(紫色石蕊试液)

(1)A是氯气发生装置,其化学反应方程式是:
(2)Ⅰ中b瓶内加入的液体最好是
(3)用图示的Ⅱ或Ⅲ代替Ⅰ是否可行?
(4)实验开始时,先点燃A处酒精灯,打开分液漏斗旋塞和Ⅰ处活塞,让氯气充满整个装置,再点燃G处酒精灯.
回答下列问题:
①怎样证明氯气已充满了整个装置?
②下列装置中的现象是:C
(5)G装置的硬质玻璃管内盛有碳粉,发生氧化还原反应,其产物为二氧化碳和氯化氢,写出G中的反应的化学方程式
(6)在H处现象为
查看习题详情和答案>>

(1)A是氯气发生装置,其化学反应方程式是:
MnO2+4HCl
MnCl2+Cl2↑+2H2O
| ||
MnO2+4HCl
MnCl2+Cl2↑+2H2O
.
| ||
(2)Ⅰ中b瓶内加入的液体最好是
饱和食盐水
饱和食盐水
.(3)用图示的Ⅱ或Ⅲ代替Ⅰ是否可行?
Ⅱ可行,Ⅲ不行.Ⅱ与Ⅰ原理相同,而Ⅲ中因c瓶口密封,体积不能改变,增大压强会有危险
Ⅱ可行,Ⅲ不行.Ⅱ与Ⅰ原理相同,而Ⅲ中因c瓶口密封,体积不能改变,增大压强会有危险
.(4)实验开始时,先点燃A处酒精灯,打开分液漏斗旋塞和Ⅰ处活塞,让氯气充满整个装置,再点燃G处酒精灯.
回答下列问题:
①怎样证明氯气已充满了整个装置?
观察当整个装置内充满黄绿色气体时,说明氯气已充满整个装置
观察当整个装置内充满黄绿色气体时,说明氯气已充满整个装置
.②下列装置中的现象是:C
溶液由浅绿色变为深红棕色
溶液由浅绿色变为深红棕色
;D溶液变蓝
溶液变蓝
;E生成白色沉淀
生成白色沉淀
.(5)G装置的硬质玻璃管内盛有碳粉,发生氧化还原反应,其产物为二氧化碳和氯化氢,写出G中的反应的化学方程式
C+2H2O+2Cl2═CO2↑+4HCl↑
C+2H2O+2Cl2═CO2↑+4HCl↑
.装置F的作用是向G中提供反应所需的水蒸气
向G中提供反应所需的水蒸气
.(6)在H处现象为
生成的HCl使紫色石蕊试液变红色,剩余的氯气又与水作用生成次氯酸,又起漂白作用,使红色褪去
生成的HCl使紫色石蕊试液变红色,剩余的氯气又与水作用生成次氯酸,又起漂白作用,使红色褪去
.