网址:http://m.1010jiajiao.com/timu3_id_381438[举报]
A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的气球。关闭K2,将等量且少量的NO2通过K1、K3分别充入A、B中,反应起始时,A、B的体积相同。(已知:2NO2(g)![]() N2O4(g) ΔH<0)
N2O4(g) ΔH<0)

(1)一段时间后,反应达到平衡,此时A、B中生成的N2O4的速率是vA vB。(填“>”、“<”或“=”);若打开活塞K2,气球B将 (填“变大”、“变小”或“不变”)。
(2)若在A、B中再充入与初始量相等的NO2,则达到平衡时,NO2的转化率αA将________(填“增大”、“减小”或“不变”);若通人等量的Ne气,则达到平衡时,A中NO2的转化率将________,B中NO2的转化率将 (填“变大”、“变小”或“不变”)。
(3)室温下,若A、B都保持体积不变,将A套上一个绝热层,B与外界可以进行热传递,则达到平衡时, 中的颜色较深。
(4)若在容器A中充入4.6 g的NO2,达到平衡后容器内混合气体的平均相对分子质量为57.5,则平衡时N2O4的物质的量为 。
查看习题详情和答案>>A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的气球。关闭K2,将等量且少量的NO2通过K1、K3分别充入A、B中,反应起始时,A、B的体积均为VL。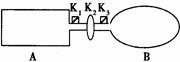
(已知:2NO2 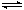 N2O4;△H<0。忽略气球材料对平衡移动的影响 )
N2O4;△H<0。忽略气球材料对平衡移动的影响 )
(1)一段时间后,反应达到平衡,此时A、B中生成的N2O4的速率是v(A) v(B)。(填“>”、“<”、“=”);若打开活塞K2,气球B将 (填:变大、变小、不变)。
(2)若在A、B中再充入与初始量相等的NO2,则达到平衡时,NO2的转化率α(A)将 (填增大或减小、不变,下同);若通入等量的Ne气,则达到平衡时,A中NO2的转化率将 ,B中NO2的转化率将 。
A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的气球。关闭K2,将等量且少量的NO2通过K1、K3分别充入A、B中,反应起始时,A、B的体积均为VL。
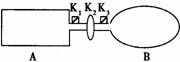
(已知:2NO2
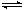 N2O4;△H<0。忽略气球材料对平衡移动的影响 )
N2O4;△H<0。忽略气球材料对平衡移动的影响 )
(1)一段时间后,反应达到平衡,此时A、B中生成的N2O4的速率是v(A) v(B)。(填“>”、“<”、“=”);若打开活塞K2,气球B将 (填:变大、变小、不变)。
(2)若在A、B中再充入与初始量相等的NO2,则达到平衡时,NO2的转化率α(A)将 (填增大或减小、不变,下同);若通入等量的Ne气,则达到平衡时,A中NO2的转化率将 ,B中NO2的转化率将 。
查看习题详情和答案>>
A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的透明气球。关闭K2,将等量且少量的NO2通过K1、K3分别充入A、B中,反应起始时,A、B的体积相同。(已知:2NO2 N2O4△H<0)下列叙述正确的是
N2O4△H<0)下列叙述正确的是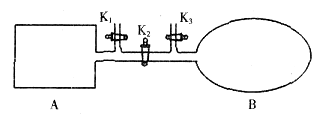
A. 到达平衡时A和B中NO2气体体积分数相同
B. 若在A、B中再充入与初始量相等的NO2,则达到平衡时A、B中NO2的转化率都增大
C. 若气球的体积不再改变,表明B中反应已达到平衡
D. 室温下,若设法使A、B都保持体积不变,将A套上一个绝热层,B与外界可以进行热传递,则达到平衡时B中气体的颜色较深
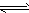 N2O4;△H<0) (如下图)
N2O4;△H<0) (如下图)