摘要:在一定条件下.反应N2(g) +3H2(g) 2NH3(g)达到平衡: (1)该反应的平衡常数表达式为 , (2)其它条件不变.减小压强平衡向 反应方向移动, (3)可以判断此反应达到化学平衡状态的是 , A.等温等容下体系的压强不变 B.等温等容混合气体的密度不变 C.混合气体平均相对分子质量不变 D.等温等压下混合气体的体积不变 (4)当温度与压强不变时.增大N2的物质的量.则逆反应速率 (填“变大 “变小 或“不变 ).平衡常数 (填“变大 “变小 或“不变 ).
网址:http://m.1010jiajiao.com/timu3_id_380973[举报]
在一定条件下,反应N2
+ 3H2  2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7 g,则反应速率为
2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7 g,则反应速率为
A.v(H2)=0.03 mol/(L·min) B.v(N2)=0.02 mol/(L·min)
C.v(NH3)=0.01 mol/(L·min) D.v(NH3)=0.17 mol/(L·min)
查看习题详情和答案>>
在一定条件下,反应N2 + 3H2 2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7 g,则反应速率为
2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7 g,则反应速率为
| A.v(H2)="0.03" mol/(L·min) | B.v(N2)="0.02" mol/(L·min) |
| C.v(NH3)="0.01" mol/(L·min) | D.v(NH3)="0.17" mol/(L·min) |
在一定条件下,反应N2 + 3H2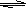 2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7 g,则反应速率为
2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7 g,则反应速率为
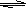 2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7 g,则反应速率为
2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7 g,则反应速率为| A.v(H2)="0.03" mol/(L·min) | B.v(N2)="0.02" mol/(L·min) |
| C.v(NH3)="0.01" mol/(L·min) | D.v(NH3)="0.17" mol/(L·min) |