网址:http://m.1010jiajiao.com/timu3_id_380686[举报]
氨气与灼热的氧化铜反应生成铜、氮气和水。利用下图所示实验装置可测定氨分子的组成(图中夹持、固定装置部分均略去)。回答下列问题:
(1)写出氨气与氧化铜反应的化学方程式: 。
(2)在A的锥形瓶中放入NaOH固体的目的是 。
(3)在干燥管B中不能选用的干燥剂是 (填序号);
A.碱石灰 B.生石灰 C.五氧化二磷 D.氢氧化钠
(4)E装置中盛装浓硫酸的目的是: ;
(5)待实验完毕后,若实验测得N2的体积(折算成标准状况)a L,干燥管D增重b g, 则氨分子中氮、氢的原子个数比为(用含a、b字母的代数式表示) 。
(6)实验室可用下图所示装置(缺少收集装置,夹持固定装置略去)制备并收集NH3
①在图中方框内画出用烧瓶收集甲的仪器装置简图.
②烧杯中溶液由无色变为红色,其原因是(用电离方程式表示) 。
查看习题详情和答案>>
氨气与灼热的氧化铜反应生成铜、氮气和水。利用下图所示实验装置可测定氨分子的组成(图中夹持、固定装置部分均略去)。回答下列问题: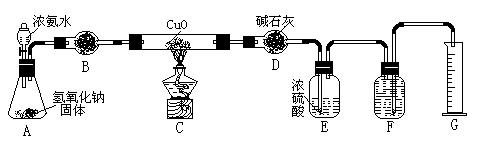
(1)写出氨气与氧化铜反应的化学方程式: 。
(2)在A的锥形瓶中放入NaOH固体的目的是 。
(3)在干燥管B中不能选用的干燥剂是 (填序号);
| A.碱石灰 | B.生石灰 | C.五氧化二磷 | D.氢氧化钠 |
(
 5)待实验完毕后,若实验测得N2的体积(折算成标准状况)a L,干燥管D增重b g, 则氨分子中氮、氢的原子个数比为(用含a、b字母的代数式表示) 。
5)待实验完毕后,若实验测得N2的体积(折算成标准状况)a L,干燥管D增重b g, 则氨分子中氮、氢的原子个数比为(用含a、b字母的代数式表示) 。(6)实验室可用下图所示装置(缺少收集装置,夹持固定装置略去)制备并收集NH3
①在图中方框内画出用烧瓶收集甲的仪器装置简图.
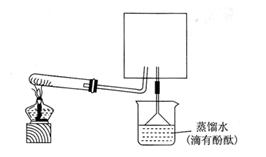
②烧杯中溶液由无色变为红色,其原因是(用电离方程式表示)
 。
查看习题详情和答案>>
。
查看习题详情和答案>>
氨气与灼热的氧化铜反应生成铜、氮气和水。利用下图所示实验装置可测定氨分子的组成(图中夹持、固定装置部分均略去)。回答下列问题:
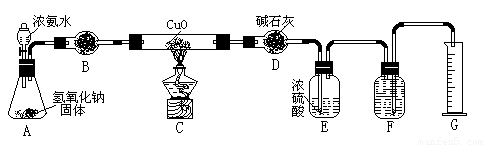
(1)写出氨气与氧化铜反应的化学方程式: 。
(2)在A的锥形瓶中放入NaOH固体的目的是 。
(3)在干燥管B中不能选用的干燥剂是 (填序号);
A.碱石灰 B.生石灰 C.五氧化二磷 D.氢氧化钠
(4)E装置中盛装浓硫酸的目的是: ;
(5)待实验完毕后,若实验测得N2的体积(折算成标准状况)a L,干燥管D增重b g, 则氨分子中氮、氢的原子个数比为(用含a、b字母的代数式表示) 。
(6)实验室可用下图所示装置(缺少收集装置,夹持固定装置略去)制备并收集NH3
①在图中方框内画出用烧瓶收集甲的仪器装置简图.
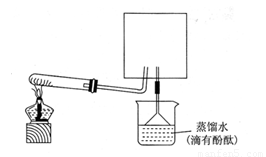
②烧杯中溶液由无色变为红色,其原因是(用电离方程式表示) 。
查看习题详情和答案>>
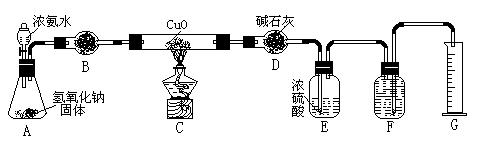
(1)写出氨气与氧化铜反应的化学方程式: 。
(2)在A的锥形瓶中放入NaOH固体的目的是 。
(3)在干燥管B中不能选用的干燥剂是 (填序号);
| A.碱石灰 | B.生石灰 | C.五氧化二磷 | D.氢氧化钠 |
(
 5)待实验完毕后,若实验测得N2的体积(折算成标准状况)a L,干燥管D增重b g, 则氨分子中氮、氢的原子个数比为(用含a、b字母的代数式表示) 。
5)待实验完毕后,若实验测得N2的体积(折算成标准状况)a L,干燥管D增重b g, 则氨分子中氮、氢的原子个数比为(用含a、b字母的代数式表示) 。(6)实验室可用下图所示装置(缺少收集装置,夹持固定装置略去)制备并收集NH3
①在图中方框内画出用烧瓶收集甲的仪器装置简图.
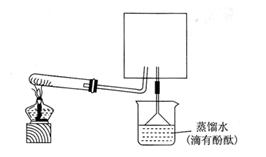
②烧杯中溶液由无色变为红色,其原因是(用电离方程式表示)
 。
。方法一,将氨气通入灼热的氧化铜粉末,得到纯净的氮气和铜。
方法二,将空气通过灼热的铜,得到较纯净的氮气和氧化铜粉末。
方法三,将亚硝酸钠(NaNO2)和氯化铵的混合溶液加热,逸出氮气。
下列是进行实验时可选择的实验仪器(其他必要的仪器如:铁架台、铁夹、铁圈、石棉网、酒精灯等未列出):
请完成下列问题:
(1)方法一制氮气:氨气是用浓氨水跟生石灰反应得到,此反应最好选用(填仪器的编号)________作发生装置,该反应的化学方程式为_______________________。要制取并收集纯净的氮气(可含有少量的水),还使用上述仪器中的________________________(填仪器的编号,并按气流方向从左向右列出)。
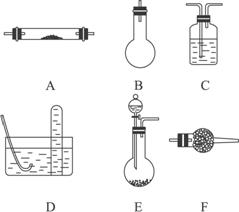
图1-9
(2)在制取氮气的三种方法中,方法一和方法二越来越受到人们的关注,经常被联合使用。这两种方法与方法三相比,其优越性在于_______________________________________。
查看习题详情和答案>>