摘要:22.各地电视台的天气预报中都要预报城市的空气质量.预报中一般将城市空气中的SO2含量和可吸入颗粒的含量(可用g/cm3表示)分为8个等级.目前.测定空气中SO2含量时主要用一些氧化还原法. 已知:SO2气体与酸性KMnO4溶液反应时.MnO4-被还原为Mn2+.SO2被氧化为SO42-. 现有药品:KMnO4固体.硫酸.颗粒吸附剂.品红试纸.pH试纸. 完成下列各题: (1)配制250mL0.100mol/L的酸性KMnO4溶液需用的仪器有 . .玻璃棒.胶头滴管.烧杯.量筒等.玻璃棒的作用是 和 . (2)写出SO2与酸性KMnO4溶液反应的离子方程式: , (3)向200mL0.1mol/L的酸性KMnO4溶液通入空气至恰好褪色.若气体的流速为a cm3/min.当t min时.则空气中SO2的含量为 g/cm3 .
网址:http://m.1010jiajiao.com/timu3_id_380623[举报]
各地电视台的天气预报中都要预报城市的空气质量。一般将城市空气中的SO2含量和可吸入颗粒的含量(可用g/cm3表示)分为8个等级。目前,测定空气中SO2含量时主要是采用一些氧化还原法。已知:SO2气体与酸性KMnO4溶液反应时,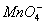 被还原成Mn2+,SO2被氧化成
被还原成Mn2+,SO2被氧化成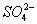 。
。
现有药品:0.1mol/L的酸性KMnO4溶液、颗粒吸附剂、品红试纸、pH试纸。
(1)配置250mL0.1mol/L的酸性KMnO4溶液需要用到的仪器有__________________、__________________、玻璃棒、胶头滴管、烧杯等,玻璃棒的作用是________________和________________。
(2)在测定SO2含量和可吸入颗粒的含量时,首先应测定________________,因为__________________________。
(3)写出SO2与酸性KMnO4溶液反应的离子方程式:_________________________________。
(4)若气体的流速为acm3/min,当tmin时,200mL0.1mol/L的酸性KMnO4溶液恰好完全褪色,则空气中的SO2的含量为___________g/cm3。
查看习题详情和答案>>