摘要:3.注意FeCl3.Fe2(SO4)3的水溶液蒸干所得剩余固体的区别. FeCl3溶液加热浓缩时.因Fe3+水解和HCl的挥发.得到的固体为Fe(OH)3.如灼烧后得到红色的Fe2O3固体.但Fe2(SO4)3溶液蒸干时.因硫酸是难挥发性酸.将不能得到Fe(OH)3固体.
网址:http://m.1010jiajiao.com/timu3_id_380358[举报]
在实验室常用下面的方法制备氢氧化铁胶体:用洁净的烧杯取少量的蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入1mol/LFeCl3溶液,至液体呈透明的红褐色.请按要求回答下列问题:
(1)反应的化学方程式为
(2)氢氧化铁胶体中微粒直径的范围是
(3)判断胶体制备成功的方法是
(4)若向此分散系中逐滴加入盐酸稀溶液,会发生一系列变化:
①先出现红褐色沉淀,原因是
②随后沉淀会溶解,溶液呈黄色,写出此反应的离子方程式
查看习题详情和答案>>
(1)反应的化学方程式为
FeCl3+3H2O?Fe(OH)3(胶体)+3HCl
FeCl3+3H2O?Fe(OH)3(胶体)+3HCl
;(2)氢氧化铁胶体中微粒直径的范围是
1nm~100nm
1nm~100nm
; (3)判断胶体制备成功的方法是
用一束光线照射,能产生一条光亮的通路(也可利用胶体的其他性质进行检验,但要注意表达规范)
用一束光线照射,能产生一条光亮的通路(也可利用胶体的其他性质进行检验,但要注意表达规范)
;(4)若向此分散系中逐滴加入盐酸稀溶液,会发生一系列变化:
①先出现红褐色沉淀,原因是
加电解质,使胶体聚沉
加电解质,使胶体聚沉
;②随后沉淀会溶解,溶液呈黄色,写出此反应的离子方程式
Fe(OH)3+3H+=Fe3++3H2O
Fe(OH)3+3H+=Fe3++3H2O
.学习化学应该明确“从生活中来,到生活中去”道理.在生产生活中,我们会遇到各种各样的化学反应.请你写出下列反应的化学方程式.(注意反应条件并配平)
(1)已知氯化铁溶液跟铜反应生成氯化铜和氯化亚铁.电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电板
(2)玻璃中含有SiO2,不能用带磨口玻璃塞的试剂瓶保存碱性溶液的原因
(3)胃舒平含有氢氧化铝,可用来治疗胃酸(盐酸)过多
(4)在高温下一氧化碳与氧化铁反应可以制得金属铁
(5)将铁加入硫酸铜溶液中炼铜(湿法炼铜)
(6)工业上用氯气和消石灰(氢氧化钙乳浊液)反应制取漂白粉(主要成分是氯化钙和次氯酸钙)
查看习题详情和答案>>
(1)已知氯化铁溶液跟铜反应生成氯化铜和氯化亚铁.电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电板
2FeCl3+Cu=CuCl2+2FeCl2
2FeCl3+Cu=CuCl2+2FeCl2
.(2)玻璃中含有SiO2,不能用带磨口玻璃塞的试剂瓶保存碱性溶液的原因
SiO2+2NaOH=Na2SiO3+H2O
SiO2+2NaOH=Na2SiO3+H2O
.(3)胃舒平含有氢氧化铝,可用来治疗胃酸(盐酸)过多
Al(OH)3+3HCl=AlCl3+3H2O
Al(OH)3+3HCl=AlCl3+3H2O
.(4)在高温下一氧化碳与氧化铁反应可以制得金属铁
3CO+Fe2O3
3CO2+2Fe
| ||
3CO+Fe2O3
3CO2+2Fe
.
| ||
(5)将铁加入硫酸铜溶液中炼铜(湿法炼铜)
Fe+CuSO4=FeSO4+Cu
Fe+CuSO4=FeSO4+Cu
.(6)工业上用氯气和消石灰(氢氧化钙乳浊液)反应制取漂白粉(主要成分是氯化钙和次氯酸钙)
2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
.(2013?朝阳区二模)由废铁制备FeCl2的主要过程如下:
Ⅰ.按下图所示过程制备FeCl3?6H2O
(1)①中产生气体的电子式是
(2)用离子方程式表示过程②中稀硝酸的作用
Ⅱ.由FeCl3?6H2O制得干燥FeCl2的过程如下:
ⅰ.向盛有FeCl3?6H2O的容器中加入SOCl2,加热,获得无水FeCl3
ⅱ.将无水FeCl3置于反应管中,通入①中产生的气体一段时间后加热,生成FeCl2
ⅲ.收集FeCl2,保存备用
(3)SOCl2与水接触会迅速产生白雾和SO2.加热分解FeCl3?6H2O不能得到无水FeCl3,而步骤ⅰ中可得到无水FeCl3,结合必要化学方程式解释得到无水FeCl3的原因
(4)过程ⅱ中产生FeCl2的化学方程式是
Ⅲ.FeCl2的包装上贴有安全注意事项,部分内容如下:
(5)下列说法正确的是
a.密闭保存、远离火源
b.可以与强氧化剂共同存放、运输
c.不宜用铁制容器包装而要用聚乙烯塑料桶包装
(6)FeCl2在空气中受热可生成氯化铁、氧化铁等,反应的化学方程式是
查看习题详情和答案>>
Ⅰ.按下图所示过程制备FeCl3?6H2O

(1)①中产生气体的电子式是
H:H
H:H
.(2)用离子方程式表示过程②中稀硝酸的作用
3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O
3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O
,在该过程中要不断向溶液中补充盐酸,目的是补充H+使NO3-继续氧化Fe2+直至NO3-完全消耗既不产生Fe(NO3)3又不引入其他杂质
补充H+使NO3-继续氧化Fe2+直至NO3-完全消耗既不产生Fe(NO3)3又不引入其他杂质
.Ⅱ.由FeCl3?6H2O制得干燥FeCl2的过程如下:
ⅰ.向盛有FeCl3?6H2O的容器中加入SOCl2,加热,获得无水FeCl3
ⅱ.将无水FeCl3置于反应管中,通入①中产生的气体一段时间后加热,生成FeCl2
ⅲ.收集FeCl2,保存备用
(3)SOCl2与水接触会迅速产生白雾和SO2.加热分解FeCl3?6H2O不能得到无水FeCl3,而步骤ⅰ中可得到无水FeCl3,结合必要化学方程式解释得到无水FeCl3的原因
6SOCl2+FeCl3?6H2O═FeCl3+12HCl↑+6SO2↑生成的HCl会抑制FeCl3的水解得到无水FeCl3
6SOCl2+FeCl3?6H2O═FeCl3+12HCl↑+6SO2↑生成的HCl会抑制FeCl3的水解得到无水FeCl3
.(4)过程ⅱ中产生FeCl2的化学方程式是
2FeCl3+H2
2FeCl2+2HCl
| ||
2FeCl3+H2
2FeCl2+2HCl
.
| ||
Ⅲ.FeCl2的包装上贴有安全注意事项,部分内容如下:
| 品 名 | 氯化亚铁 |
| 理化特性 | 白色,遇空气易变成黄色,易吸水,有腐蚀性… |
| 注意事项 | 避免接触空气、碱等;聚乙烯塑料桶包装;避免受热 |
ac
ac
.a.密闭保存、远离火源
b.可以与强氧化剂共同存放、运输
c.不宜用铁制容器包装而要用聚乙烯塑料桶包装
(6)FeCl2在空气中受热可生成氯化铁、氧化铁等,反应的化学方程式是
4FeCl2+H2O+O2
2FeCl3+Fe2O3+2HCl
| ||
4FeCl2+H2O+O2
2FeCl3+Fe2O3+2HCl
.
| ||
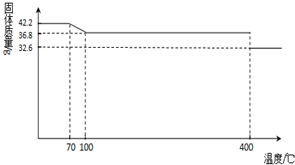 (2013?德州模拟)食盐中的抗结剂是亚铁氰化钾,其化学式为K4[Fe(CN)6]?3H2O.
(2013?德州模拟)食盐中的抗结剂是亚铁氰化钾,其化学式为K4[Fe(CN)6]?3H2O.42.2g K4[Fe(CN)6]?3H2O样品受热脱水过程的热重曲线(样品质量随温度的变化曲线)如下图所示.试回答下列问题:
(1)试确定150℃时固体物质的化学式为
K4[Fe(CN)6]
K4[Fe(CN)6]
.(2)查阅资料知:虽然亚铁氰化钾自身毒性很低,但其水溶液与酸反应放出极毒的氰化氢(HCN)气体;亚铁氰化钾加热至一定温度时能分解产生氰化钾(KCN).据此判断,烹饪食品时应注意的问题为
应避免与醋、西红柿等酸性物质一起烹饪;控制烹饪温度不超过400℃
应避免与醋、西红柿等酸性物质一起烹饪;控制烹饪温度不超过400℃
.(3)在25℃下,将a mol?L-1的KCN溶液与0.01mol?L-1的盐酸等体积混合,反应平衡时,测得溶液pH=7,则KCN溶液的物质的量浓度a
>
>
0.01mol?L-1(填“>”、“<”或“=”);用含a的代数式表示HCN的电离常数Ka=(100a-1)×10-7 mol?L-1
(100a-1)×10-7 mol?L-1
.(4)在Fe2+、Fe3+的催化作用下,可实现2SO2+O2+2H2O═2H2SO4的转化.已知,含SO2的废气通入Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2++O2+4H+═4Fe3++2H2O,则另一反应的离子方程式为
2Fe3++SO2+2H2 ═2Fe2++SO42-+4H+
2Fe3++SO2+2H2 ═2Fe2++SO42-+4H+
.则上述转化的重要意义在于变废为宝,消除污染
变废为宝,消除污染
.(5)已知Fe(OH)3的溶度积常数Ksp=1.1×10-36.室温时在FeCl3溶液中滴加NaOH溶液,当溶液pH为3时,通过计算说明Fe3+是否沉淀完全
c(Fe3+)=1.1×10-3(mol/L)>10-5 mol?L-1故Fe3+没有沉淀完全
c(Fe3+)=1.1×10-3(mol/L)>10-5 mol?L-1故Fe3+没有沉淀完全
.(提示:当某离子浓度小于10-5 mol?L-1时可以认为该离子沉淀完全了)