网址:http://m.1010jiajiao.com/timu3_id_379910[举报]
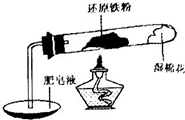 铁不能与冷、热水反应,但能与水蒸气反应.中学教材中用下图所示实验装置,完成还原铁粉与水蒸气反应的演示实验.
铁不能与冷、热水反应,但能与水蒸气反应.中学教材中用下图所示实验装置,完成还原铁粉与水蒸气反应的演示实验.资料显示,在不同温度下,还原铁粉与水蒸气反应的产物是不同的,温度低于570℃时,生成FeO;高于570℃时,生成Fe3O4.
(1)实验中使用肥皂液的作用是
(2)甲同学对实验后试管内的黑色固体X含有哪些物质进行了探究.
提出假设:①所得固体是FeO
②所得固体是Fe3O4
③所得固体是
实验探究:
| 实验编号 | 实验操作 | 实验现象 |
| ① | 取少量黑色粉末X放入试管1中,加入盐酸,微热. | 黑色粉末逐渐溶解,有少量气泡产生. |
| ② | 取试管1反应后的溶液少许,滴加几滴KSCN溶液,振荡. | 溶液没有出现血红色. |
| ③ | 取试管1反应后的溶液少许,滴加几滴酸性KMnO4溶液,振荡 | 高锰酸钾溶液褪色 |
(3)乙同学设计下列实验方案以确定实验后试管内的固体是否存在Fe3O4.
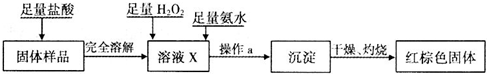
①溶液X中发生氧化还原反应的离子方程式为
②操作a包括过滤和洗涤,检验沉淀是否已经洗涤干净的操作是
③如果取固体样品m1克,反应后得到红棕色固体m2克,则m1与m2之比最少应大于
(14分)
I.常温下浓度均为0.l mol/L的下列溶液:①Na2CO3溶液②NaHCO3溶液③盐酸④氨水
回答下列问题。
(1)上述溶液中有水解反应发生的是 (填编号,下同),溶液中溶质存在电离平衡的是 。
(2)四种溶液中对水的电离抑制作用最大的是 ;比较①、②溶液,pH较大的是 。
(3)在溶液④中加入NH4Cl固体,NH+4浓度与OH-浓度的比值将____(填“变大”、“变小”、“不变”)
II.有一瓶无色澄清溶渡,其中可能含有:NH+4、K+、Mg2+、Al3+、Fe2+、NO-3、Cl-、SO2-4、CO2-3取该溶液进行下列实验:
(1)取部分溶液,向其中逐滴滇入Ba(OH)2溶液至过量,有白色沉淀生成,沉淀量与加入Ba(OH)2溶液量的关系如右图所示。
(2)取(I)反应后过滤所得沉淀和滤液,在沉淀中加入稀盐酸后,沉淀不减少。将滤液分为两等份,一份加热,未产生刺激性气味的气体;另一份如HNO3酸化时有白色沉淀产生,继续加HNO3,沉淀又消失,再加AgNO3没有变化。
根据以上事实确定:该溶液中肯定存在的离子有 ;
肯定不存在的离子有____ 。
查看习题详情和答案>>
A.加BaCl2溶液,有白色沉淀生成,再加入盐酸无现象,则原溶液中有SO![]() ??
??
B.加入盐酸有无色气体逸出,该气体能使澄清石灰水变浑浊,则原溶液中有CO![]() ??
??
C.加入KSCN溶液,不变红色,再滴几滴氯水,溶液立刻变成红色,则原溶液中有Fe2+??
D.加入烧碱溶液,微热时有气体放出,该气体能使湿润的红色石蕊试纸变蓝,则原溶液中有NH![]() ??
??
A.加入BaCl2溶液有白色沉淀生成,再加入稀盐酸,沉淀不溶解,则原溶液中含![]()
B.向溶液中加硝酸酸化,再加少许AgNO3溶液,有白色沉淀生成,则原溶液中含Cl-
C.向溶液中加入盐酸,有无色气体逸出,此气体能使澄清石灰水变浑浊,则溶液中含有![]()
D.加入NaOH溶液,微热时有气体放出,该气体能使润湿的红色石蕊试纸变蓝,则溶液中含有![]()
(14分)
I.常温下浓度均为0.l mol/L的下列溶液:①Na2CO3溶液②NaHCO3溶液③盐酸④氨水
回答下列问题。
(1)上述溶液中有水解反应发生的是 (填编号,下同),溶液中溶质存在电离平衡的是 。
(2)四种溶液中对水的电离抑制作用最大的是 ;比较①、②溶液,pH较大的是 。
(3)在溶液④中加入NH4Cl固体,NH+4浓度与OH-浓度的比值将____(填“变大”、“变小”、“不变”)
II.有一瓶无色澄清溶渡,其中可能含有:NH+4、K+、Mg2+、Al3+、Fe2+、NO-3、Cl-、SO2-4、CO2-3取该溶液进行下列实验:
(1)取部分溶液,向其中逐滴滇入Ba(OH)2溶液至过量,有白色沉淀生成,沉淀量与加入Ba(OH)2溶液量的关系如右图所示。

(2)取(I)反应后过滤所得沉淀和滤液,在沉淀中加入稀盐酸后,沉淀不减少。将滤液分为两等份,一份加热,未产生刺激性气味的气体;另一份如HNO3酸化时有白色沉淀产生,继续加HNO3,沉淀又消失,再加AgNO3没有变化。
根据以上事实确定:该溶液中肯定存在的离子有 ;
肯定不存在的离子有____ 。
查看习题详情和答案>>