网址:http://m.1010jiajiao.com/timu3_id_379597[举报]
一、二级标准:4.00,三级标准:6.00 。一环保检测中心对采集的0.02m3(标况)某区域空气样品中所含CO的浓度进行测定,其方法和实验步骤如下:
①首先将空气样品通过盛有I2O5固体的加热管,反应生成CO2和I2(不考虑其他气体的反应);
②用30.0mL 5.00×10-5mol·L-1过量的硫代硫酸钠溶液完全吸收反应所产生的碘,发生的反应为:I2+2S2O32-=2I-+S4O62-
③ 将②反应后溶液取出1/2,放入锥形瓶中,加入几滴指示剂,用1.00×10-5mol·L-1的标准碘溶液进行滴定,滴定至终点,实验记录如下:
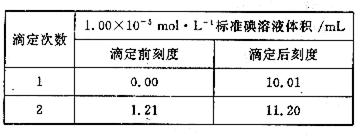
(1) 写出中反应的化学方程式:
(2) 计算该空气样品中CO的浓度,并说明符合几级标准。
《环境空气质量标准》中,有害气体的浓度常用标准状况下,每立方米气体中含有害气体的毫克值(mg/m3)来表示,对CO的浓度限值规定为:
一、二级标准:4.00,三级标准:6.00 。一环保检测中心对采集的0.02m3(标况)某区域空气样品中所含CO的浓度进行测定,其方法和实验步骤如下:
① 首先将空气样品通过盛有I2O5固体的加热管,反应生成CO2和I2(不考虑其他气体的反应);
② 用30.0mL 5.00×10-5mol·L-1过量的硫代硫酸钠溶液完全吸收反应所产生的碘,发生的反应为:I2+2S2O32-=2I-+S4O62-
③ 将②反应后溶液取出1/2,放入锥形瓶中,加入几滴指示剂,用1.00×10-5mol·L-1的标准碘溶液进行滴定,滴定至终点,实验记录如下:

(1) 写出中反应的化学方程式:
(2) 计算该空气样品中CO的浓度,并说明符合几级标准。
查看习题详情和答案>>《环境空气质量标准》中,有害气体的浓度常用标准状况下,每立方米气体中含有害气体的毫克值(mg/m3)来表示,对CO的浓度限值规定为:一级、二级标准:4.00,三级标准:6.00 。某环保检测中心对采集的0.02m3(标况)某区域空气样品中所含CO的浓度进行测定,其方法和实验步骤如下:
① 首先将空气样品通过盛有I2O5固体的加热管,反应生成CO2和I2
(不考虑其他气体的反应);
② 用30.0mL 5.00×10-5mol?L-1过量的硫代硫酸钠溶液完全吸收反应所产生的碘,发生的反应为:I2+2S2O32-=2I-+S4O62-
③ 将②反应后溶液取出1/2,放入锥形瓶中,加入几滴指示剂,用1.00×10-5mol?L-1的标准碘溶液进行滴定,滴定至终点,实验记录如下:
| 滴定次数 | 1.00×10-3mol?L-1标准碘溶液体积/mL | |
| 滴定前刻度 | 滴定后刻度 | |
| 1 | 0.00 | 10.01 |
| 2 | 1.21 | 11.20 |
(1)写出①中反应的化学方程式:
(2)计算该空气样品中CO的浓度,并说明符合几级标准。
查看习题详情和答案>>①首先将该空气样品通过盛有I2O5固体的加热管,反应生成CO2和I2(不考虑其他气体的反应);
②用30.0 mL 5.00×10-5 mol·L-1过量的硫代硫酸钠溶液完全吸收反应所产生的碘,发生的反应为:I2+2![]() ====2I-+
====2I-+![]() ;
;
③将②反应后溶液取出![]() ,放入锥形瓶中,加入几滴指示剂,用1.00×10-5 mol·L-1的标准碘溶液进行滴定,滴定至终点,实验记录如下:
,放入锥形瓶中,加入几滴指示剂,用1.00×10-5 mol·L-1的标准碘溶液进行滴定,滴定至终点,实验记录如下:
滴定次数 | 1.00×10-5 mol·L-1标准碘溶液体积/mL | |
滴定前刻度 | 滴定后刻度 | |
1 | 0.00 | 10.01 |
2 | 1.21 | 11.20 |
(1)写出①中反应的化学方程式;
(2)计算该空气样品中CO的浓度,并说明符合几级标准。