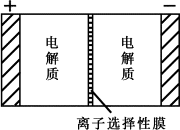
摘要: 一种大型蓄电系统的电池总反应为:2Na2S2+NaBr3 Na2S4+3NaBr.电池中的左右两侧为电极.中间为离子选择性膜(在电池放电和充电时该膜允许钠离子通过),放电前.被膜隔开的电解质为Na2S2和NaBr3.放电后.分别变为Na2S4和NaBr.下列说法正确的是 A. 充电过程中.Na+ 离子的流向为从右到左 B. 充电过程中.阳极的电极反应为:3NaBr –2e- = NaBr3 + 2Na+ C. 放电前.左侧电解质为Na2S2.右侧电解质为NaBr3 D. 放电过程中.电子由负极通过外电路流向正极 10. 在25mL 0.1mol·L-1NaOH溶液中逐滴加入0.2mol·L-1CH3COOH溶液.溶液pH变化曲线如图所示.下列有关离子浓度的比较正确的是 A.在A.B间任一点.溶液中可能 有c(Na+)>c(CH3COO-)>c(OH-)>c(H+) B.在B点.a>12.5.且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+) C.在C点.c(Na+)>c(CH3COO-) >c(H+)>c(OH-) D.在D点.c(CH3COO-)+c(CH3COOH)=c(Na+)
网址:http://m.1010jiajiao.com/timu3_id_379448[举报]
|
一种大型蓄电系统的电池总反应为:2Na2S2+NaBr3 中的左右两侧为电极,中间为离子选择性膜(在电池放电和充电时该膜允许钠离 子通过);放电前,被膜隔开的电解质为Na2S2和NaBr3,放电后,分别变为Na2S4 和NaBr.下列说法正确的是
| |
| [ ] | |
A. |
充电过程中,Na+离子的流向为从右到左 |
B. |
充电过程中,阳极的电极反应为:3NaBr-2e-=NaBr3+2Na+ |
C. |
放电前,左侧电解质为Na2S2,右侧电解质为NaBr3 |
D. |
放电过程中,电子由负极通过外电路流向正极 |
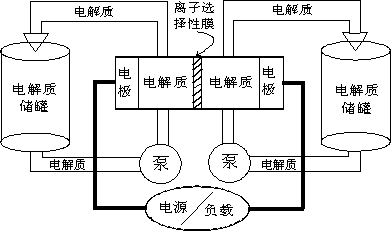
下图是一种正在投入生产的大型蓄电系统。左右两侧为电解质储罐,中央为电池,电解质通过泵不断在储罐和电池间循环;电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜可允许钠离子通过;放电前,被膜隔开的电解质为Na2S2和NaBr3,放电后,分别变为Na2S4和NaBr。下列说法正确的是
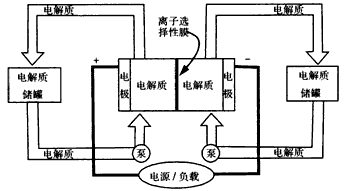
[ ]
A.电池充电时,阳极电极反应式为:3Br--2e-=Br3-
B.电池放电时,负极电极反应式为:2S22-+2e-=S42-
C.电池放电时,电池的总反应式为:Na2S4+3NaBr=2Na2S2+NaBr3
D.在充电过程中钠离子通过膜的流向为从左到右
查看习题详情和答案>>
B.电池放电时,负极电极反应式为:2S22-+2e-=S42-
C.电池放电时,电池的总反应式为:Na2S4+3NaBr=2Na2S2+NaBr3
D.在充电过程中钠离子通过膜的流向为从左到右
|
下图是一种正在投入生产的大型蓄电系统.左右两侧为电解质储罐,中央为电池,电解质通过泵不断在储罐和电池间循环;电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜可允许钠离子通过;放电前,被膜隔开的电解质为Na2S2(右罐)和NaBr3(左罐),放电后,分别变为Na2S4和NaBr.下列说法正确的是
| |
A. |
电池充电时阳极电极反应式为:3Br--2e-=Br3- |
B. |
电池放电时,负极电极反应式为:2S22-+2e-=S42- |
C. |
电池放电时,电池的总反应方程式为:Na2S4+3NaBr=2Na2S2+NaBr3 |
D. |
在充电过程中Na+通过膜的流向为从左到右 |