摘要:19.如图所示的电路.A1的读数为1.2A.A2的读数为2A.则 A.R1<R2.表A的示数大于3.2 A B. R1>R2.表A的示数等于3.2 A C. R1=R2.表A的示数等于4 A D. R1>R2.表A的示数无法判定 B A 20.如图所示.质量相同的木块A.B.用轻弹簧相连接.置于光滑的水平面上.开始弹簧处于自然状态.先用水平恒力F推木块A.则弹簧在第一次被压缩到最短的过程中下列说法中不正确的是 A.A .B速度相同时.加速度aA=aB B.A .B速度相同时.加速度aA>aB C.A .B加速度相同时.速度vA<vB D. A .B加速度相同时.速度vA>vB
网址:http://m.1010jiajiao.com/timu3_id_378854[举报]
|
在如图所示的电路中,有一烧杯中盛有Ba(OH)2溶液,由滴管逐滴向烧杯中加H2SO4溶液至过量,则灯泡L和电流表
| |
A. |
L先亮后暗, |
B. |
L逐渐变暗, |
C. |
L先亮后暗, |
D. |
L先暗后亮, |
(2012?西安模拟)单质A与粉末化合物B组成的混合物能发生如图所示的一系列反应:
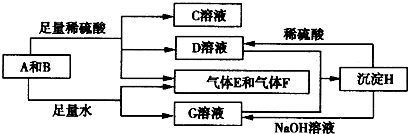
请回答下列问题:
(1)组成A单质的元素在周期表中处于第
(2)化合物B的电子式为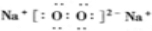
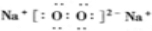 .
.
(3)D与G两溶液混合后发生反应的离子方程式为
(4)常温下,D溶液的pH
(5)10.8g A单质与足量的NaOH溶液反应,消耗氧化剂的质量为
(6)用碳棒、稀硫酸、气体E和气体F组成燃料电池,该电池的正极反应式为
查看习题详情和答案>>

请回答下列问题:
(1)组成A单质的元素在周期表中处于第
3
3
周期ⅢA
ⅢA
族.(2)化合物B的电子式为
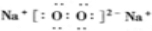
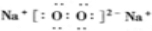
(3)D与G两溶液混合后发生反应的离子方程式为
Al3++3AlO2-+6H2O=4Al(OH)3↓
Al3++3AlO2-+6H2O=4Al(OH)3↓
.(4)常温下,D溶液的pH
<
<
7(填“>”、“<”或“=”),其原因是Al3++3H2O?Al(OH)3+3H+
Al3++3H2O?Al(OH)3+3H+
(用离子方程式表示).(5)10.8g A单质与足量的NaOH溶液反应,消耗氧化剂的质量为
21.6
21.6
g.(6)用碳棒、稀硫酸、气体E和气体F组成燃料电池,该电池的正极反应式为
O2+4H++4e-=2H2O
O2+4H++4e-=2H2O
.以该电池为电源,用惰性电极电解100g 8%的C溶液,当电解到溶质的质量分数为l2.5%时停止电解,则电解过程中,生成的气体在标准状况下的体积共为67.2
67.2
L,电路上通过电子的物质的量为4
4
mol.(2011?石家庄二模)如图所示的四个容器中分别盛有不同的溶液,除A、B外,其余电极均为石墨电极.甲为铅蓄电池,其工作原理为:Pb+PbO2+2H2SO4
2PbSO4+2H2O,其两个电极的电极材料分别是PbO2和Pb.
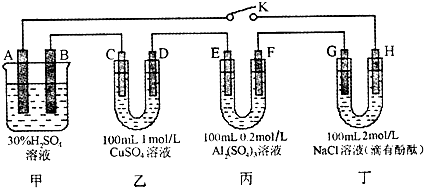
闭合K,发现G电极附近的溶液变红,20min后,将K断开,此时C、D两极上产生的气体体积相同;据此回答:
(1)A电极的电极材料是
(2)电解后,要使丙中溶液恢复到原来的浓度,需加入的物质是
(3)到20min时,电路中通过电子的物质的量为
(4)0~20min,H电极上发生反应的电极反应式为:
(5)20min后将乙装置与其他装置断开,然后在C、D两极间连上灵敏电流计,发现电流计指针偏转,则此时C电极为
查看习题详情和答案>>
| 放电 | 充电 |

闭合K,发现G电极附近的溶液变红,20min后,将K断开,此时C、D两极上产生的气体体积相同;据此回答:
(1)A电极的电极材料是
PbO2
PbO2
(填“PbO2”或“Pb”).(2)电解后,要使丙中溶液恢复到原来的浓度,需加入的物质是
H2O
H2O
(填化学式).(3)到20min时,电路中通过电子的物质的量为
0.4mol
0.4mol
.(4)0~20min,H电极上发生反应的电极反应式为:
2Cl--2e-=Cl2↑;2H++2e-=H2↑
2Cl--2e-=Cl2↑;2H++2e-=H2↑
.(5)20min后将乙装置与其他装置断开,然后在C、D两极间连上灵敏电流计,发现电流计指针偏转,则此时C电极为
负极
负极
极,D电极上发生的电极反应式为:2H++2e-=H2↑
2H++2e-=H2↑
.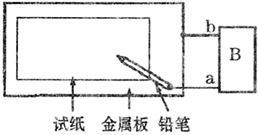 取一张用饱和的NaCl溶液浸湿的石蕊试纸,平铺在一块金属板上,按如图所示的方法连接电路.
取一张用饱和的NaCl溶液浸湿的石蕊试纸,平铺在一块金属板上,按如图所示的方法连接电路.(1)若金属板为一铂片,B处为一直流电源,接通电源后,
①若试纸为红色石蕊试纸,用铅笔在试纸上写字,出现蓝色字迹.则a电极为电源的
负极
负极
(填“正极”或“负极”),铅笔芯与试纸接触的电极反应为2H++2e-=H2↑(或2H2O+2e-=H2↑+2OH-)
2H++2e-=H2↑(或2H2O+2e-=H2↑+2OH-)
.②若试纸为蓝色石蕊试纸,将铅笔芯放置在试纸上一段时间后,接触处出现一个双色同心圆,内圈为白色,外圈呈浅红色.则a电极为电源的
正极
正极
(填“正极”或“负极”),铅笔芯与试纸接触处的电极反应为2Cl-2e-=Cl2↑
2Cl-2e-=Cl2↑
.(2)若试纸为红色石蕊 试纸,金属板为一锌片,B处为一灵敏电流计,接通电路,将铅笔芯放置在试纸上一段时间,发现电流计指针发生偏转,则接触处将
变蓝
变蓝
(填“变白”、“变蓝”或“不变色”),铅笔芯与试纸接触处的电极反应为O2+2H2O+4e-=4OH-
O2+2H2O+4e-=4OH-
.
单质A与粉末化合物B组成的混合物能发生如图所示的一系列反应:
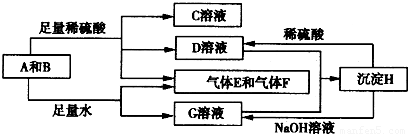
请回答下列问题:
(1)组成A单质的元素在周期表中处于第______周期______族.
(2)化合物B的电子式为______.
(3)D与G两溶液混合后发生反应的离子方程式为______.
(4)常温下,D溶液的pH______7(填“>”、“<”或“=”),其原因是______(用离子方程式表示).
(5)10.8g A单质与足量的NaOH溶液反应,消耗氧化剂的质量为______g.
(6)用碳棒、稀硫酸、气体E和气体F组成燃料电池,该电池的正极反应式为______.以该电池为电源,用惰性电极电解100g 8%的C溶液,当电解到溶质的质量分数为l2.5%时停止电解,则电解过程中,生成的气体在标准状况下的体积共为______L,电路上通过电子的物质的量为______mol.
查看习题详情和答案>>

请回答下列问题:
(1)组成A单质的元素在周期表中处于第______周期______族.
(2)化合物B的电子式为______.
(3)D与G两溶液混合后发生反应的离子方程式为______.
(4)常温下,D溶液的pH______7(填“>”、“<”或“=”),其原因是______(用离子方程式表示).
(5)10.8g A单质与足量的NaOH溶液反应,消耗氧化剂的质量为______g.
(6)用碳棒、稀硫酸、气体E和气体F组成燃料电池,该电池的正极反应式为______.以该电池为电源,用惰性电极电解100g 8%的C溶液,当电解到溶质的质量分数为l2.5%时停止电解,则电解过程中,生成的气体在标准状况下的体积共为______L,电路上通过电子的物质的量为______mol.
查看习题详情和答案>>
