摘要:⑴A.A中O和F原子的最外层电子数等于8.B中O和F原子的最外层电子数不等于8 ⑵O..< ⑶-338.次氟酸不稳定.易分解为HF和O2 ⑷H2O2HOF+H2O(热)=H2O2+HF ⑸MnO2 .FeCl3
网址:http://m.1010jiajiao.com/timu3_id_378199[举报]
从原子、分子水平上帮助我们认识物质构成的规律;以微粒之间不同的作用力为线索,研究不同类型物质的有关性质;从物质结构决定性质的视角预测物质的有关性质.

(1)下列说法正确的是 (填字母).
A.元素电负性由大到小的顺序为F>O>N
B.一个苯分子含3个π键和6个σ键
C.氯化钠和氯化铯晶体中氯离子的配位数相同
D.第一电离能的大小为Br>Se>As
(2)根据等电子体原理,羰基硫(OCS)分子的结构式为 .光气(COCl2)各原子最外层都满足8电子稳定结构,COCl2分子空间构型为 (用文字描述).
(3)Cu 2+基态的电子排布式为 .向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中会析出深蓝色的[Cu(NH3)4]SO4晶体,该物质中配位原子的杂化方式为 ,不考虑空间构型,其内界结构可用示意图表示为 .
查看习题详情和答案>>
 《物质结构与性质》
《物质结构与性质》从原子、分子水平上帮助我们认识物质构成的规律;以微粒之间不同的作用力为线索,研究不同类型物质的有关性质;从物质结构决定性质的视角预测物质的有关性质.
(1)下列说法正确的是
A
A
(填字母).A.元素电负性由大到小的顺序为F>O>N
B.一个苯分子含3个π键和6个σ键
C.氯化钠和氯化铯晶体中氯离子的配位数相同
D.第一电离能的大小为Br>Se>As
(2)根据等电子体原理,羰基硫(OCS)分子的结构式为
O=C=S
O=C=S
.光气(COCl2)各原子最外层都满足8电子稳定结构,COCl2分子空间构型为平面三角形
平面三角形
(用文字描述).(3)Cu 2+基态的电子排布式为
1s22s22p63s23p63d9
1s22s22p63s23p63d9
.向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中会析出深蓝色的[Cu(NH3)4]SO4晶体,该物质中配位原子的杂化方式为sp3
sp3
,不考虑空间构型,其内界结构可用示意图表示为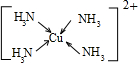

20世纪50年代科学家提出价层电子对互斥模型(简称VSEPR模型),用于预测简单分子立体结构.其要点可以概括为:
Ⅰ、用AXnEm表示只含一个中心原子的分子组成,A为中心原子,X为与中心原子相结合的原子,E为中心原子最外层未参与成键的电子对(称为孤对电子),(n+m)称为价层电子对数.分子中的价层电子对总是互相排斥,均匀的分布在中心原子周围的空间;
Ⅱ、分子的立体构型是指分子中的原子在空间的排布,不包括中心原子未成键的孤对电子;
Ⅲ、分子中价层电子对之间的斥力主要顺序为:i、孤对电子之间的斥力>孤对电子对与共用电子对之间的斥力>共用电子对之间的斥力; ii、双键与双键之间的斥力>双键与单键之间的斥力>单键与单键之间的斥力; iii、X原子得电子能力越弱,A-X形成的共用电子对之间的斥力越强; iv、其他.
请仔细阅读上述材料,回答下列问题:
(1)根据要点I可以画出AXnEm的VSEPR理想模型,请填写下表:
(2)请用VSEPR模型解释CO2为直线型分子的原因
(3)H2O分子的立体构型为:
(4)SO2Cl2和SO2F2都属AX4E0型分子,S=O之间以双键结合,S-Cl、S-F之间以单键结合.请你预测 SO2Cl2和SO2F2分子的立体构型:
查看习题详情和答案>>
Ⅰ、用AXnEm表示只含一个中心原子的分子组成,A为中心原子,X为与中心原子相结合的原子,E为中心原子最外层未参与成键的电子对(称为孤对电子),(n+m)称为价层电子对数.分子中的价层电子对总是互相排斥,均匀的分布在中心原子周围的空间;
Ⅱ、分子的立体构型是指分子中的原子在空间的排布,不包括中心原子未成键的孤对电子;
Ⅲ、分子中价层电子对之间的斥力主要顺序为:i、孤对电子之间的斥力>孤对电子对与共用电子对之间的斥力>共用电子对之间的斥力; ii、双键与双键之间的斥力>双键与单键之间的斥力>单键与单键之间的斥力; iii、X原子得电子能力越弱,A-X形成的共用电子对之间的斥力越强; iv、其他.
请仔细阅读上述材料,回答下列问题:
(1)根据要点I可以画出AXnEm的VSEPR理想模型,请填写下表:
| n+m | 2 | 4 4 |
| VSEPR理想模型 | 直线形 直线形 |
正四面体 |
| 价层电子对之间的理想键角 | 180° 180° |
109°28′ |
CO2属AX2E0,n+m=2,故CO2为直线形
CO2属AX2E0,n+m=2,故CO2为直线形
.(3)H2O分子的立体构型为:
V形
V形
,请你预测水分子中∠H-O-H的大小范围为<109°28′
<109°28′
,原因是水分子属AX2E2,n+m=4,VSEPR理想模型为正四面体,价层电子对之间的夹角均为109°28′.根据Ⅲ-i,应有∠H-O-H<109°28′
水分子属AX2E2,n+m=4,VSEPR理想模型为正四面体,价层电子对之间的夹角均为109°28′.根据Ⅲ-i,应有∠H-O-H<109°28′
.(4)SO2Cl2和SO2F2都属AX4E0型分子,S=O之间以双键结合,S-Cl、S-F之间以单键结合.请你预测 SO2Cl2和SO2F2分子的立体构型:
四面体
四面体
.
(1)下列现象和应用与电子跃迁无关的是______.
A.激光 B.焰色反应 C.燃烧放热
D.原子光谱 E.霓虹灯 F.石墨导电
(2)A、B、C三种短周期元素,A是原子半径最小的元素,B原子最外层电子数是次外层的两倍,C元素的基态原子L层有两个未成对电子.
①某直线形分子由A、B两种元素组成且原子个数比为1:1,该分子中含有______个σ键,______个π键.
②由A、B、C三种元素组成的无机阴离子,可形成二聚离子或多聚链状离子,从该阴离子的结构特点分析能够相互缔合的原因:______.
(3)CO的结构可表示为C≡O,N2的结构可表示为N≡N.下表是两者的键能数据:(单位:kJ/mol)
结合数据说明CO比N2活泼的原因:______.
(4)Fe、Co、Ni、Cu等金属能形成配合物与这些金属原子的电子层结构有关.
①基态28Ni原子的核外电子排布式为______.
②Fe(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)5晶体属于______(填晶体类型).
③CuSO4?5H2O(胆矾)中含有水合铜离子因而呈蓝色,写出胆矾晶体中水合铜离子的结构简式(必须将配位键表示出来)______.
查看习题详情和答案>>
A.激光 B.焰色反应 C.燃烧放热
D.原子光谱 E.霓虹灯 F.石墨导电
(2)A、B、C三种短周期元素,A是原子半径最小的元素,B原子最外层电子数是次外层的两倍,C元素的基态原子L层有两个未成对电子.
①某直线形分子由A、B两种元素组成且原子个数比为1:1,该分子中含有______个σ键,______个π键.
②由A、B、C三种元素组成的无机阴离子,可形成二聚离子或多聚链状离子,从该阴离子的结构特点分析能够相互缔合的原因:______.
(3)CO的结构可表示为C≡O,N2的结构可表示为N≡N.下表是两者的键能数据:(单位:kJ/mol)
| A-B | A=B | A≡B | |
| C≡O | 357.7 | 798.9 | 1071.9 |
| N≡N | 154.8 | 418.4 | 941.7 |
(4)Fe、Co、Ni、Cu等金属能形成配合物与这些金属原子的电子层结构有关.
①基态28Ni原子的核外电子排布式为______.
②Fe(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)5晶体属于______(填晶体类型).
③CuSO4?5H2O(胆矾)中含有水合铜离子因而呈蓝色,写出胆矾晶体中水合铜离子的结构简式(必须将配位键表示出来)______.
查看习题详情和答案>>
已知A、B、C、D、E、F、G是原子序数依次增大的短周期元素,其中A原子的核内无中子;B原子的最外层电子数是内层电子数的2倍且B、C、D同周期并相邻;D与G同主族;E、F、G同周期且它们的最高价氧化物的水化物两两之间都可以相互反应生成盐和水.请回答下列问题:
(1)D的简单阴离子的结构示意图是
 ;F元素在周期表中的位置是
;F元素在周期表中的位置是
(2)D、E、F的单核离子半径由大到小的顺序为
(3)D与A按1:1原子个数比组成的化合物的电子式为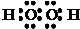
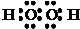 ;D与E按1:1原子个数比组成的化合物与二氧化碳反应的化学方程式为
;D与E按1:1原子个数比组成的化合物与二氧化碳反应的化学方程式为
(4)由D、F、G组成的一种常见易溶性盐可用作净水剂,其原因是
(5)工业上常用A、C元素组成的一种常见气态化合物经过三步反应来制取硝酸,则第一步反应的化学方程式为
查看习题详情和答案>>
(1)D的简单阴离子的结构示意图是


第3周期第ⅢA
第3周期第ⅢA
.(2)D、E、F的单核离子半径由大到小的顺序为
O 2->Na+>Al 3+
O 2->Na+>Al 3+
(用离子符号表示);证明B、G非金属性强弱的实验方法和现象是向Na2CO3溶液中加入稀硫酸产生大量无色无味气体
向Na2CO3溶液中加入稀硫酸产生大量无色无味气体
.(3)D与A按1:1原子个数比组成的化合物的电子式为
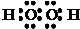
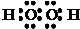
2Na2O2+2CO2=Na2CO3+O2
2Na2O2+2CO2=Na2CO3+O2
.(4)由D、F、G组成的一种常见易溶性盐可用作净水剂,其原因是
Al 3++3H2O?Al(OH)3(胶体)+3H+,生成的胶体与水中的杂质作用形成沉淀
Al 3++3H2O?Al(OH)3(胶体)+3H+,生成的胶体与水中的杂质作用形成沉淀
(用离子方程式及必要的文字说明).(5)工业上常用A、C元素组成的一种常见气态化合物经过三步反应来制取硝酸,则第一步反应的化学方程式为
4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
;将G元素的一种常见气态氧化物通入C元素最高价氧化物对应的水化物中,反应的离子方程式为
| ||
| △ |
3SO2+2NO3-+2H2O=3SO42-+2NO+4H+
3SO2+2NO3-+2H2O=3SO42-+2NO+4H+
.