网址:http://m.1010jiajiao.com/timu3_id_377224[举报]
(10分,每空格2分)原子结构与元素周期表存在着内在联系。请回答下列问题:
(1)具有(n-1)d10ns电子构型的元素位于周期表中 区。
(2)被誉为“21世纪金属”的钛(Ti)元素原子的价电子排布式为: 。
(3)写出地壳中含量最多的金属元素原子的核外电子排布式 。
(4)写出3p轨道上有2个未成对电子的元素的符号: 。
(5)已知Ti3+可形成配位数为6,颜色不同的两种配合物晶体,一种为紫色,另一为绿色。两种晶体的组成都为TiCl3·6H2O。为测定这两种晶体的化学式,设计了如下实验:a分别取等质量的两种配合物晶体的样品配成待测溶液;b分别往待测溶液中滴入AgNO3溶液,均产生白色沉淀;c沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水溶液得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的 。该绿色晶体配合物的化学式为
。该绿色晶体配合物的化学式为
查看习题详情和答案>>
(08年江苏卷)(10分)金矿开采、冶炼和电镀工业会产生大量含氰化合物的污水,其中含氰化合物以HCN、CN -和金属离子的配离子M(CN)nm-的形式存在于水中。测定污水中含氰化合物含量的实验步骤如下:
①水样预处理:水样中加入磷酸和EDTA,在pH<2的条件下加热蒸馏,蒸出所有的HCN,并用NaOH溶液吸收。
②滴定:将吸收液调节至pH>11,以试银灵作指示剂,用AgNO3标准溶液滴定
 Ag++2CN - == [Ag(CN)2] -
Ag++2CN - == [Ag(CN)2] -
终点时,溶液由黄色变成橙红色。
根据以上知识回答下列问题:
⑴水样预处理的目的是 。
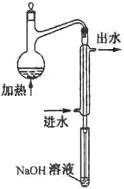
⑵水样预处理的装置如右图,细导管插入吸收液中是为了 ____
⑶蒸馏瓶比吸收液面要高出很多,其目的是 。
⑷如果用盐酸代替磷酸进行预处理,实验结果将 (填“偏高”、“无影响”或“偏低”)。
⑸准确移取某工厂污水100mL,经处理后用浓度为0.01000mol?L-1的硝酸银标准溶液滴定,终点时消耗了21.00mL。此水样中含氰化合物的含量为 mg?L-1的(以计,计算结果保留一位小数)。
查看习题详情和答案>>(10分)硫酸铵是一种常用的铵态氮肥。下表是硫酸铵化肥品质的主要指标。
| 指标 项目 | 优等品 | 一等品 | 合格品
|
| 外观 | 白色结晶,无可见机械杂质 | 无可见机械杂质 | |
| 氮(N)含量 | ≥21.0% | ≥21.0% | ≥20. 5% |
新华中学化学研究性学习小组为本地农业生产服务,对某农用品商店出售的一等品硫酸铵化肥的品质进行探究。
[观察外观] 该硫酸铵化肥无可见机械杂质。
[实验探究]按右图所示装置进行实验。
(1)烧瓶内发生反应的离子方程式为:_________________________________________________
烧杯中盛放的试剂最好是 ___ __(填“浓硫酸”、“稀硫酸”或“水”)。
(2)实验过程中,需往烧瓶中加入足量浓氢氧化钠溶液并充分加热的原因是_________________________________。
[交流讨论]?
甲同学:根据此实验测得的数据,计算硫酸铵化肥的含氮量可能偏高,因为实验装置中存在一个明显缺陷是:__________________________________________________。
乙同学:实验装置中还存在另一个明显缺陷是:___________________________________________________________________________________________________ 。
经过大家充分讨论一致认为:针对甲、乙两位同学指出的实验装置中存在的明显缺陷,需改进实验装置,重新进行实验。
[探究结论]
称取13.5 g硫酸铵化肥样品,用改进后的实验装置重新进行实验,测得实验前后B装置增重3.40 g。该化肥 (填“是”或“不是”)一等品。
查看习题详情和答案>>
(10分)金矿开采、冶炼和电镀工业会产生大量含氰化合物的污水,其中含氰化合物以HCN、CN -和金属离子的配离子M(CN)nm-的形式存在于水中。测定污水中含氰化合物含量的实验步骤如下:
①水样预处理:水样中加入磷酸和EDTA,在pH<2的条件下加热蒸馏,蒸出所有的HCN,并用NaOH溶液吸收。
②滴定:将吸收液调节至pH>11,以试银灵作指示剂,用AgNO3标准溶液滴定
Ag++2CN - ="=" [Ag(CN)2] -
终点时,溶液由黄色变成橙红色。
根据以上知识回答下列问题:
(1)水样预处理的目的是 。
(2)水样预处理的装置如右图,细导管插入吸收液中是为了 。
(3)蒸馏瓶比吸收液面要高出很多,其目的是 。
(4)如果用盐酸代替磷酸进行预处理,实验结果将 (填“偏高”、“无影响”或“偏低”)。
(5)准确移取某工厂污水100mL,经处理后用浓度为0.01000mol·L-1的硝酸银标准溶液滴定,终点时消耗了21.00mL。此水样中含氰化合物的含量为 mg·L-1(以CN-计,计算结果保留一位小数)。
(10分,每空格2分)原子结构与元素周期表存在着内在联系。请回答下列问题:
(1)具有(n-1)d10ns电子构型的元素位于周期表中 区。
(2)被誉为“21世纪金属”的钛(Ti)元素原子的价电子排布式为: 。
(3)写出地壳中含量最多的金属元素原子的核外电子排布式 。
(4)写出3p轨道上有2个未成对电子的元素的符号: 。
(5)已知Ti3+可形成配位数为6,颜色不同的两种配合物晶体,一种为紫色,另一为绿色。两种晶体的组成都为TiCl3·6H2O。为测定这两种晶体的化学式,设计了如下实验:a分别取等质量的两种配合物晶体的样品配成待测溶液;b分别往待测溶液中滴入AgNO3溶液,均产生白色沉淀;c沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水溶液得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的 。该绿色晶体配合物的化学式为
。该绿色晶体配合物的化学式为