摘要:既能跟强酸(H+)反应.又能跟强碱(OH-)反应的化合物可称为两性化合物.包括两性氧化物.两性氢氧化物.弱酸的酸式盐以及氨基酸等.1.铝.氢氧化铝.氧化铝的两性 (1)2Al+6 H+==2 Al3++3H2↑ 2Al+2OH-+2H2O==2AlO2-+3H2↑ (2)Al2O3+6H+==2Al3++3H2O Al2O3+2OH-=2AlO2-+H2O 3既能与强酸反应又能与强碱反应: Al(OH)3既能与强酸反应又能与强碱反应.说明Al(OH)3必须同时能电离出H+和OH-.即能发生“两性电离 : 根据平衡移动原理.:当向上述平衡体系中加强酸.[H+]增大.同时又中和OH-使[OH-]下降.平衡向右移动.结果Al(OH)3逐渐溶解成Al3+,当向上述平衡中加强碱.[OH-]增大.同时又中和H+使[H+]下降.平衡向左移动.结果Al(OH)3固体逐渐溶解成为AlO2-.相关方程式: Al(OH)3+3H+==Al3++3H2O(不能与H2CO3等弱酸反应) Al(OH)3+OH-==AlO2-+2H2O
网址:http://m.1010jiajiao.com/timu3_id_374284[举报]
A、B、C、E、F是原子序数依次增大的六种常见短周期元素.A与C可形成A2C和A2C2两种液体;B单质在C单质中燃烧可生成BC、BC2两种气体;C和D元素成的化合物甲具有两性;E的单质在C单质中燃烧的产物乙可使品红溶液褪色;A单质在F单质中燃烧产生苍白色火焰.请回答下列问题:
(1)元素E的名称为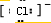
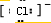 .
.
(2)A2C2的电子式为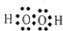
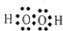 ,BC2结构式为
,BC2结构式为
(3)A单质在F单质中燃烧反应的化学方程式为
(4)甲对应的水化物既能跟强酸溶液也能跟强碱溶液反应,请分别写出甲对应的水化物与硫酸及氢氧化钠反应的离子方程式:
(5)B2A4气体和乙气体均能使溴水褪色,写出:
B2A4气体和溴水反应的化学方程式:
乙气体和溴水反应的离子方程式为
查看习题详情和答案>>
(1)元素E的名称为
硫
硫
,F简单阴离子的电子式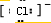
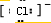
(2)A2C2的电子式为
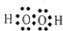
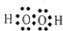
O=C=O
O=C=O
(3)A单质在F单质中燃烧反应的化学方程式为
H2+Cl2
2HCl
| ||
H2+Cl2
2HCl
.
| ||
(4)甲对应的水化物既能跟强酸溶液也能跟强碱溶液反应,请分别写出甲对应的水化物与硫酸及氢氧化钠反应的离子方程式:
Al(OH)3+3H+=Al3++3H2O
Al(OH)3+3H+=Al3++3H2O
,Al(OH)3+OH-=AlO2-+2H2O
Al(OH)3+OH-=AlO2-+2H2O
.(5)B2A4气体和乙气体均能使溴水褪色,写出:
B2A4气体和溴水反应的化学方程式:
CH2=CH2+Br2→BrCH2CH2Br
CH2=CH2+Br2→BrCH2CH2Br
,反应类型为加成反应
加成反应
.乙气体和溴水反应的离子方程式为
SO2+Br2+2H2O=SO42-+2Br-+4H+
SO2+Br2+2H2O=SO42-+2Br-+4H+
.下列说法正确的是( )
| A、油脂饱和程度越大,熔点越低 | B、氨基酸、二肽、蛋白质均既能跟强酸反应又能跟强碱反应 | C、蔗糖、麦芽糖、硬脂酸甘油酯酸性水解都能得到2种物质 | D、麻黄碱( )的催化氧化产物能发生银镜反应 )的催化氧化产物能发生银镜反应 |