摘要: 已知下列热化学方程式: ,△H=-258.8kJ/mol ,△H=-2220.0kJ/mol 5mol和的混合气体.完全燃烧时放热3847kJ.则混合气体中和的体积比为多少?
网址:http://m.1010jiajiao.com/timu3_id_374085[举报]
下列热化学方程或说法正确的是:
[ ]
A.甲烷的标准燃烧热为-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ·mol-1
B.500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g) + 3H2 (g) 2NH3(g) △H=-38.6kJ·mol-1
2NH3(g) △H=-38.6kJ·mol-1
C.同温同压下,等物质的量的H2与足量的Cl2在光照和点燃条件下充分反应,所产生的热量相同
D.已知中和热为57.3 kJ/mol,则稀硫酸与氢氧化钡溶液反应的热化学方程式为
2H+(aq)+SO42-(aq)+ Ba2+(aq)+2OH-(aq)=BaSO4(s)+2H2O(l) △H=-57.3kJ·mol-1
查看习题详情和答案>>
B.500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g) + 3H2 (g)
 2NH3(g) △H=-38.6kJ·mol-1
2NH3(g) △H=-38.6kJ·mol-1 C.同温同压下,等物质的量的H2与足量的Cl2在光照和点燃条件下充分反应,所产生的热量相同
D.已知中和热为57.3 kJ/mol,则稀硫酸与氢氧化钡溶液反应的热化学方程式为
2H+(aq)+SO42-(aq)+ Ba2+(aq)+2OH-(aq)=BaSO4(s)+2H2O(l) △H=-57.3kJ·mol-1
下列热化学方程或说法正确的是:
[ ]
A.甲烷的标准燃烧热为-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3kJ·mol-1
B.500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g) + 3H2 (g) 2NH3(g) △H=-38.6kJ·mol-1
2NH3(g) △H=-38.6kJ·mol-1
C.已知中和热为57.3 kJ/mol,则稀硫酸与氢氧化钡溶液中和反应的热化学方程式为
2H+(aq)+SO42-(aq)+ Ba2+(aq)+2OH-(aq)=BaSO4(s)+2H2O(l) △H=-57.3kJ·mol-1
D.氯化镁溶液与氨水反应:Mg2+ + 2NH3·H2O = Mg(OH)2↓+ 2NH4+
查看习题详情和答案>>
B.500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g) + 3H2 (g)
 2NH3(g) △H=-38.6kJ·mol-1
2NH3(g) △H=-38.6kJ·mol-1 C.已知中和热为57.3 kJ/mol,则稀硫酸与氢氧化钡溶液中和反应的热化学方程式为
2H+(aq)+SO42-(aq)+ Ba2+(aq)+2OH-(aq)=BaSO4(s)+2H2O(l) △H=-57.3kJ·mol-1
D.氯化镁溶液与氨水反应:Mg2+ + 2NH3·H2O = Mg(OH)2↓+ 2NH4+
通常情况下空气中CO2的体积分数为0.030%,当空气中CO2的体积分数超过0.050%时,会引起明显的温室效应.为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究.
(1)目前,用超临界CO2(其状态介于气态和液态之间)代替氟利昂作致冷剂已成为一种趋势,这一做法对环境的积极意义在于
(2)利用二氧化碳制造全降解塑料,可以缓解温室效应.已知过氧键(-O-O-)不稳定,请写出环氧乙烷与CO2通过加聚制造全降解塑料的化学方程式:
 .
.
(3)CCTV《科技博览》报道:2004年3月中科院首创用CO2合成可降解塑料聚二氧化碳(CO2)n.下列相关说法合理的是
A.聚二氧化碳塑料是通过加聚反应制得的
B.聚二氧化碳塑料与干冰互为同分异构体
C.聚二氧化碳塑料与干冰都是纯净物
D.聚二氧化碳塑料的使用会产生白色污染
(4)最近有科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使之变为可再生燃料甲醇.“绿色自由”构想技术流程如下:

①分解池中反应的化学方程式为
②在合成塔中,若有4.4kgCO2与足量H2恰好完全反应,可放出4947kJ的热量,试写出合成塔中发生反应的热化学方程
(5)小李同学拟用沉淀法测定空气中CO2的体积分数,为了提高测量的精确度,小李应该选用的试剂为
A.Ca(OH)2 B.Ba(OH)2 C.BaCl2 D. BaCl2和NaOH.
查看习题详情和答案>>
(1)目前,用超临界CO2(其状态介于气态和液态之间)代替氟利昂作致冷剂已成为一种趋势,这一做法对环境的积极意义在于
保护臭氧层
保护臭氧层
.(2)利用二氧化碳制造全降解塑料,可以缓解温室效应.已知过氧键(-O-O-)不稳定,请写出环氧乙烷与CO2通过加聚制造全降解塑料的化学方程式:


(3)CCTV《科技博览》报道:2004年3月中科院首创用CO2合成可降解塑料聚二氧化碳(CO2)n.下列相关说法合理的是
A
A
.A.聚二氧化碳塑料是通过加聚反应制得的
B.聚二氧化碳塑料与干冰互为同分异构体
C.聚二氧化碳塑料与干冰都是纯净物
D.聚二氧化碳塑料的使用会产生白色污染
(4)最近有科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使之变为可再生燃料甲醇.“绿色自由”构想技术流程如下:

①分解池中反应的化学方程式为
2KHCO3
K2CO3+CO2↑+H2O
| ||
2KHCO3
K2CO3+CO2↑+H2O
.
| ||
②在合成塔中,若有4.4kgCO2与足量H2恰好完全反应,可放出4947kJ的热量,试写出合成塔中发生反应的热化学方程
CO2(g)+3H2(g)
CH3OH(g)+H2O(g)△H=-49.47kJ?mol-1
| ||
| 高温高压 |
CO2(g)+3H2(g)
CH3OH(g)+H2O(g)△H=-49.47kJ?mol-1
.
| ||
| 高温高压 |
(5)小李同学拟用沉淀法测定空气中CO2的体积分数,为了提高测量的精确度,小李应该选用的试剂为
B或D
B或D
(填序号).A.Ca(OH)2 B.Ba(OH)2 C.BaCl2 D. BaCl2和NaOH.
 (2010?南昌一模)在恒温恒容的密闭容器中通入1molN2和XmolH2,发生如下反应:N2(g)+3H2(g)
(2010?南昌一模)在恒温恒容的密闭容器中通入1molN2和XmolH2,发生如下反应:N2(g)+3H2(g)| 催化剂 | 高温、高压 |
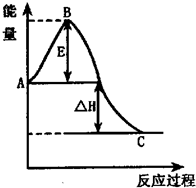
已知:①反应过程能量变化如右图;②达到平衡时,测得反应放出的热量为18.4KJ,混合气体物质的量为3.6moL,容器内压强减小10%;
请回答下列问题:
(1)图中A点表示
反应物具有的总能量
反应物具有的总能量
;C点表示生成物具有的总能量
生成物具有的总能量
;(2)该反应通常使用铁为主体的复合催化剂,使用该催化剂时,B点的变化是
降低
降低
(填“升高”或“降低”)(3)X值为
3
3
;(4)该反应的热化学方程为
N2(g)+3H2(g)?2NH3(g)△H=-92kJ/moL
N2(g)+3H2(g)?2NH3(g)△H=-92kJ/moL
;(5)若起始时充入的N2、H2、NH3物质的量分别为a、b、c,平衡时各组分的量与上述平衡均相等,且始终维持反应向正方向进行,则起始时c的取值范围为
O≤C<0.4
O≤C<0.4
.以含硫铁矿石为原料生产硫酸的工艺流程图如下:

请回答下列问题:
(1)将燃烧含硫铁矿石的化学方程式补充完整:4
2Fe2O3+8SO2.
充分煅烧含硫铁矿石Wg,反应完全后冷却至室温,称得固体物质的质量是mg,生成SO2为VL,则含硫铁矿石中硫元素的质量分数是(假设矿石中的杂质受热不分解,也不会与SO2反应)
A.
B.
C.
D.
(2)接触室中发生反应的化学方程式是
某温度下,进入接触室内SO2和O2的物质的量比为1:1,反应达到平衡时,压强减少
,则SO2的转化率为
(3)依据工艺流程图判断下列说法正确的是(选填序号字母)
a.为使黄铁矿充分燃烧,需将其粉碎
b.过量空气能提高SO2的转化率
c.使用催化剂能提高SO2的反应速率和转化率
d.沸腾炉排出的矿渣可供炼铁
(4)吸收塔用于吸收SO3气体的X物质是
已知每240g SO3气体与H2O化合放出390.9kJ的热量,该反应的热化学方程是
(5)排出的尾气SO2既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的Br2.SO2吸收Br2的离子方程式是
查看习题详情和答案>>

请回答下列问题:
(1)将燃烧含硫铁矿石的化学方程式补充完整:4
FeS2
FeS2
+11O2
| ||
充分煅烧含硫铁矿石Wg,反应完全后冷却至室温,称得固体物质的质量是mg,生成SO2为VL,则含硫铁矿石中硫元素的质量分数是(假设矿石中的杂质受热不分解,也不会与SO2反应)
D
D
.A.
| 32V |
| 22.4W |
| 22.4V |
| 32W |
| 3(W-m) |
| W |
| 8(W-m) |
| 5W |
(2)接触室中发生反应的化学方程式是
2SO2+O2
3SO3
| 催化剂 |
| △ |
2SO2+O2
3SO3
.| 催化剂 |
| △ |
某温度下,进入接触室内SO2和O2的物质的量比为1:1,反应达到平衡时,压强减少
| 1 |
| 5 |
80%
80%
.(3)依据工艺流程图判断下列说法正确的是(选填序号字母)
abd
abd
.a.为使黄铁矿充分燃烧,需将其粉碎
b.过量空气能提高SO2的转化率
c.使用催化剂能提高SO2的反应速率和转化率
d.沸腾炉排出的矿渣可供炼铁
(4)吸收塔用于吸收SO3气体的X物质是
浓硫酸
浓硫酸
(写名称).已知每240g SO3气体与H2O化合放出390.9kJ的热量,该反应的热化学方程是
SO3(g)+H2O(l)═H2SO4(l);△H=-130.3kJ/mol
SO3(g)+H2O(l)═H2SO4(l);△H=-130.3kJ/mol
.(5)排出的尾气SO2既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的Br2.SO2吸收Br2的离子方程式是
SO2+Br2+2H2O═4H++2Br-+SO42-
SO2+Br2+2H2O═4H++2Br-+SO42-
.