摘要:将一直流电源的正.负极.用玻璃片分别压在一张用食盐水.碘化钾.淀粉溶液和石蕊试液浸透的滤纸上.经过一段时间后.两极附近滤纸的颜色分别是 A B C D 阳极 蓝 白 红 蓝 阴极 白 蓝 蓝 蓝
网址:http://m.1010jiajiao.com/timu3_id_372880[举报]
 甲、乙两池电极材料如图所示.
甲、乙两池电极材料如图所示.请按要求回答下列问题:
(1)若两池中均为CuSO4溶液,反应一段时间后:①有红色物质析出的是:甲池中的
碳
碳
棒(填“铁”或“碳”)、乙池中的阴
阴
极(填“阴”或“阳”);②乙池中阳极电极反应式是
4OH-4e-=2H2O+O2↑
4OH-4e-=2H2O+O2↑
.(2)若两池中均为足量饱和NaCl溶液:
①写出乙池中总反应的化学方程式
2NaCl+2H2O
Cl2↑+H2↑+2NaOH
| ||
2NaCl+2H2O
Cl2↑+H2↑+2NaOH
;
| ||
若电极上转移0.2mole-,则阴极上生成
0.1
0.1
mol气体;再加入HCl
HCl
(填化学式)可恢复到原来浓度.②甲池中碳极上电极反应式是
O2+2H2O+4e-=4OH-
O2+2H2O+4e-=4OH-
,其原理与金属的吸氧
吸氧
腐蚀原理相同;若要防止铁的腐蚀可采取的措施为b、c
b、c
(填序号).a.将甲图碳棒换成铜棒
b.碳棒换成锌棒
c.在铁、碳之间连接一个直流电源,把铁接到负极上
d.把铁接到直流电源的正极上.
甲、乙两池电极材料如图所示.
请按要求回答下列问题:
(1)若两池中均为CuSO4溶液,反应一段时间后:①有红色物质析出的是:甲池中的______棒(填“铁”或“碳”)、乙池中的______极(填“阴”或“阳”);
②乙池中阳极电极反应式是______.
(2)若两池中均为足量饱和NaCl溶液:
①写出乙池中总反应的化学方程式______;
若电极上转移0.2mole-,则阴极上生成______mol气体;再加入______(填化学式)可恢复到原来浓度.
②甲池中碳极上电极反应式是______,其原理与金属的______腐蚀原理相同;若要防止铁的腐蚀可采取的措施为______(填序号).
a.将甲图碳棒换成铜棒
b.碳棒换成锌棒
c.在铁、碳之间连接一个直流电源,把铁接到负极上
d.把铁接到直流电源的正极上.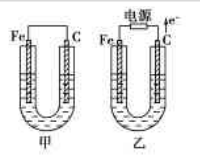
查看习题详情和答案>>
请按要求回答下列问题:
(1)若两池中均为CuSO4溶液,反应一段时间后:①有红色物质析出的是:甲池中的______棒(填“铁”或“碳”)、乙池中的______极(填“阴”或“阳”);
②乙池中阳极电极反应式是______.
(2)若两池中均为足量饱和NaCl溶液:
①写出乙池中总反应的化学方程式______;
若电极上转移0.2mole-,则阴极上生成______mol气体;再加入______(填化学式)可恢复到原来浓度.
②甲池中碳极上电极反应式是______,其原理与金属的______腐蚀原理相同;若要防止铁的腐蚀可采取的措施为______(填序号).
a.将甲图碳棒换成铜棒
b.碳棒换成锌棒
c.在铁、碳之间连接一个直流电源,把铁接到负极上
d.把铁接到直流电源的正极上.

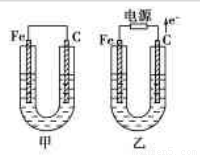
甲、乙两池电极材料如图所示.
请按要求回答下列问题:
(1)若两池中均为CuSO4溶液,反应一段时间后:①有红色物质析出的是:甲池中的 棒(填“铁”或“碳”)、乙池中的 极(填“阴”或“阳”);
②乙池中阳极电极反应式是 .
(2)若两池中均为足量饱和NaCl溶液:
①写出乙池中总反应的化学方程式 ;
若电极上转移0.2mole-,则阴极上生成 mol气体;再加入 (填化学式)可恢复到原来浓度.
②甲池中碳极上电极反应式是 ,其原理与金属的 腐蚀原理相同;若要防止铁的腐蚀可采取的措施为 (填序号).
a.将甲图碳棒换成铜棒
b.碳棒换成锌棒
c.在铁、碳之间连接一个直流电源,把铁接到负极上
d.把铁接到直流电源的正极上.
 查看习题详情和答案>>
查看习题详情和答案>>
请按要求回答下列问题:
(1)若两池中均为CuSO4溶液,反应一段时间后:①有红色物质析出的是:甲池中的 棒(填“铁”或“碳”)、乙池中的 极(填“阴”或“阳”);
②乙池中阳极电极反应式是 .
(2)若两池中均为足量饱和NaCl溶液:
①写出乙池中总反应的化学方程式 ;
若电极上转移0.2mole-,则阴极上生成 mol气体;再加入 (填化学式)可恢复到原来浓度.
②甲池中碳极上电极反应式是 ,其原理与金属的 腐蚀原理相同;若要防止铁的腐蚀可采取的措施为 (填序号).
a.将甲图碳棒换成铜棒
b.碳棒换成锌棒
c.在铁、碳之间连接一个直流电源,把铁接到负极上
d.把铁接到直流电源的正极上.
 查看习题详情和答案>>
查看习题详情和答案>>
 目前流通的第五套人民币硬币材料分别为:1元硬币为铜芯镀镍合金,5角硬币为铜芯镀铜合金,1角硬币为硬铝合金.请回答:(题目中的百分含量均为质量分数)
目前流通的第五套人民币硬币材料分别为:1元硬币为铜芯镀镍合金,5角硬币为铜芯镀铜合金,1角硬币为硬铝合金.请回答:(题目中的百分含量均为质量分数)(1)钢是含碳量为0.03%~2%的
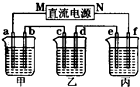
(2)如图所示的装置中,甲、乙、丙三个烧杯分别盛放足量的溶液,电极及溶液如下表所示:
| 电极 | a | b | c | d | e | f |
| 石墨 | 石墨 | 铜 | 钢 | 钢 | 铜 | |
| 溶液 | NaCl溶液 | CuSO4溶液 | CuSO4溶液 | |||
①上述装置中M极为直流电源的
②若在钢币上镀铜,应选择
(3)工业上以铝土矿(主要成分Al2O3?nH2O,含少量的氧化铁和石英等杂质)为原料生产铝.为除去铝土矿样品中氧化铁和石英杂质,要将粉碎、筛选后的铝土矿样品溶解在足量的氢氧化钠溶液中处理,请写出有关反应的离子方程式
(4)已知硬铝中含Cu:2.2%~5%、Mg:0.2%~3%、Mn:0.3%~1.5%、Si:0.5%,其余是Al.1角硬币单枚质量为2.20克,若想制得1角硬币1百万枚,理论上至少需要含Al2O3 90%的铝土矿约