网址:http://m.1010jiajiao.com/timu3_id_371824[举报]
硫元素价态众多,可与卤素、氮等元素化合形成许多复杂化合物,在科学技术和生成中有重要的应用.根据题意完成下列计算:
1.由硫与限量氯气在50~60℃反应16~20小时,可恰好完全反应,得到两种硫的氯化物A和B.A物质中的含硫量为0.131,B物质中的含氯量为0.816,A的相对分子质量比B大71.计算确定这两种氯化物的分子式分别为________.
若上述反应得到的A、B的物质的量比为3:2,则参加反应的S和氯气的物质的量之比为________.
2.硫的卤化物或卤氧化物都有强水解性,可以作脱水剂.SF4吸收V mL液态水(4℃),完全反应,得到3.2 g SO2气体(假设SO2完全逸出)和10%的酸溶液,计算吸收的液态水的体积V为________mL.
3.S4N4是亮橙色固体,不溶于水和有机溶剂,是一种重要的金属有机化学反应物.一般用S2Cl2、SCl2的惰性溶剂(CS2)氨解制得:
6S2Cl2+16NH3→S4N4+S8+12NH4Cl;
24SCl2+64NH3→4S4N4+S8+48NH4Cl.
S2Cl2、SCl2的混合液体52.86 g溶于足量的CS2中,再通入35.84 L氨气(标准状况)完全氨解,产生14.080 g硫单质.剩余氨气用40 g水完全吸收形成氨水(密度为0.923 g/mL).
计算:①该混合液体中S2Cl2、SCl2的物质的量之比为________.
②所得氨水的物质的量浓度为________(保留1位小数).
4.S4N4与Ag在一定条件下反应,失去N2而缩合成(SN)x,(SN)x合成于1910年,过了五十年,才发现它在0.26 K的低温下,可转变为超导体(superconductor).(SN)x的结构式为:

已知1.20×105 mol S4N4与Ag发生缩合,失去了1.20×105 mol N2,生成二百聚物[(SN)200]和三百聚物.测得缩合产物中二百聚物的质量分数为0.50.
计算:①缩合产物中各缩合物的物质的量.
②若Ag的实际使用量为8.64 kg,求Ag的循环使用次数.
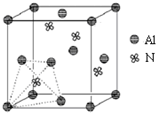 元素周期表中的第ⅢA、ⅣA、ⅤA族的部分元素往往易形成原子晶体,氮化铝、磷化硼和砷化镓属于此列,如氮化铝晶体中每个Al原子与4个N原子相连,每个N原子也与4个Al原子相连,晶胞如右图所示.磷化硼是一种受到高度关注的耐磨涂料,它可用作金属的表面保护层;砷化镓属于第三代半导体,它能直接将电能转变为光能,砷化镓灯泡寿命是普通灯泡的100倍,而耗能只有其10%.试回答下列问题:
元素周期表中的第ⅢA、ⅣA、ⅤA族的部分元素往往易形成原子晶体,氮化铝、磷化硼和砷化镓属于此列,如氮化铝晶体中每个Al原子与4个N原子相连,每个N原子也与4个Al原子相连,晶胞如右图所示.磷化硼是一种受到高度关注的耐磨涂料,它可用作金属的表面保护层;砷化镓属于第三代半导体,它能直接将电能转变为光能,砷化镓灯泡寿命是普通灯泡的100倍,而耗能只有其10%.试回答下列问题:(1)下列离子中最外层电子数不为8的是
A.P3- B.Al3+ C.Ti4+ D.Ga3+
(2)下列说法正确的是
A.硼和镓都属于S区元素,磷、砷属于P区元素
B.第一电离能:As>Ga Mg>Al
C.根据等电子体原理,砷化镓、磷化硼的晶胞与氮化铝晶体相同且类似于单晶硅
D.NH3沸点高于AsH3,其原因是NH3分子中共价键强度较大
(3)砷化镓可由(CH3)3Ga和AsH3反应得到,该反应在700℃进行,反应的化学方程式为
| 700℃ |
| 700℃ |
下列有机分子中碳原子的杂化方式与(CH3)3Ga分子中Ga原子的杂化方式相同的是
A.CH4B.CH2=CH2C.CH≡CH D.HCHO E.

(4)请画出三溴化磷分子的路易斯结构式


(1)下列离子中最外层电子数不为8的是______(选填序号).
A.P3- B.Al3+ C.Ti4+ D.Ga3+
(2)下列说法正确的是______(选填序号).
A.硼和镓都属于S区元素,磷、砷属于P区元素
B.第一电离能:As>Ga Mg>Al
C.根据等电子体原理,砷化镓、磷化硼的晶胞与氮化铝晶体相同且类似于单晶硅
D.NH3沸点高于AsH3,其原因是NH3分子中共价键强度较大
(3)砷化镓可由(CH3)3Ga和AsH3反应得到,该反应在700℃进行,反应的化学方程式为______;
下列有机分子中碳原子的杂化方式与(CH3)3Ga分子中Ga原子的杂化方式相同的是______.(填序号)
A.CH4B.CH2=CH2C.CH≡CH D.HCHO E.
(4)请画出三溴化磷分子的路易斯结构式______,请判断三溴化硼分子属于______(填“极性”“非极性”)分子.
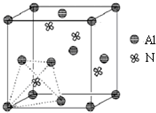
(1)下列离子中最外层电子数不为8的是______(选填序号).
A.P3- B.Al3+ C.Ti4+ D.Ga3+
(2)下列说法正确的是______(选填序号).
A.硼和镓都属于S区元素,磷、砷属于P区元素
B.第一电离能:As>Ga Mg>Al
C.根据等电子体原理,砷化镓、磷化硼的晶胞与氮化铝晶体相同且类似于单晶硅
D.NH3沸点高于AsH3,其原因是NH3分子中共价键强度较大
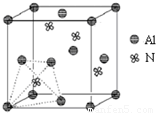
(3)砷化镓可由(CH3)3Ga和AsH3反应得到,该反应在700℃进行,反应的化学方程式为______
 查看习题详情和答案>>
查看习题详情和答案>>
硫、氮、碳、铁、铜等常见元素在化合物中常表现出多种价态,如硫有-2、-1、+2、+4、+6等价态。这些元素在化工生产中有着重要应用。
(1)31.2g镁与碳粉的混合物在一定条件下恰好完全反应,再加入足量水,得到40.6g白色沉淀,同时产生密度为1.4107g/L(标准状况)的丙二烯和不饱和烃X的混合气体。
①镁与碳粉的反应产物的化学式为 ______________ 。
②原混合物中碳粉的物质的量分数为 ___________。(用小数表示,保留2位小数)
(2)某复杂盐由三种元素组成,含两种阳离子和两种阴离子。取21.76g该复杂盐,平均分为两份。将第一份溶于足量盐酸酸化的氯化钡溶液,所得沉淀中含9.32g硫酸钡。将第二份溶于足量热浓硝酸,再滴加足量硝酸钡溶液,得13.98g白色沉淀,过滤后向蓝色滤液中加足量烧碱溶液,过滤、洗涤、灼烧,得8.00g黑色固体。
①该复杂盐的化学式为_____________。
②该复杂盐中两种阳离子的质量比为 _________________ 。
(3)某地质学家经勘测发现一种新的磁黄铁矿,主要成分为Fe1-xS1+x,杂质不含Fe、S。分析可知该磁黄铁矿中,铁元素中三价铁的质量分数为75%。取5吨 73%的该磁黄铁矿,用接触法制硫酸,若沸腾炉中煅烧的损耗率为4%,接触室中反应的转化率为94%,SO3的吸收效率为97%,则最多可制得98.3%的浓硫酸的质量是________________。(保留2位小数)