摘要:21A.A.B.C.D分别代表四种不同的元素.A原子的最外层电子排布为ns1.B原子的价电子排布为ns2np2.C原子的最外层电子数是其电子层数的3倍.D原子的L电子层的p轨道有3个电子. (1)C原子的电子排布式为 ▲ .若A原子的最外层电子排布为1s1.则按原子轨道的重迭方式判断.A与C形成的化合物中的共价键类型属于 ▲ .A与C所形成的化合物的熔沸点明显高于A与C的同主族元素所形成的化合物的熔沸点.其原因是 ▲ . (2)当n=2时.B原子的结构示意图为 ▲ .B与C形成的晶体属于 晶体.当n=3时.B与C形成的晶体中.B原子的杂化方式为 ▲ .该晶体中最小的环共有 ▲ 个微粒构成.微粒间的作用力是 ▲ . (3)若A原子的最外层电子排布为4s1.B原子的价电排布为3s23p2.A在元素周期表中的位置是 ▲ .A.B.C.D四种元素的第一电离能由大到小的顺序是 ▲ . 21B.某化学研究性学习小组进行了一系列“带火星的木炭复燃 的实验.实验装置如下图所示. (1)甲组同学探究“使带火星木炭复燃时O2的体积分数的极限 .将氧气和空气(假定空气中O2的体积分数为20%)按不同的体积比混合得100mL气体A进行实验.实验记录如下: 编号 I II III IV V V(O2)/mL 60 40 20 12 10 V/mL 40 60 80 88 90 现象 木炭复燃 木炭复燃 木炭复燃 木炭有时燃烧.有时不燃烧 木炭 不复燃 回答下列问题: ①使带火星木炭复燃的O2的体积分数最小约为 ▲ . ②用带火星木炭检验集气瓶里是否集满O2.若木炭复燃.能否认为集气瓶里的气体一定是纯净的O2?答: ▲ . ③若按照3∶2的比例混合O2和CO2气体.该混合气体能否使带火星的木炭复燃? 答: ▲ (“能 .“否 或“不一定 ). (2)乙组同学探究“NO2能否支持燃烧 的问题.设计了如下几组实验.实验记录及结论如下: 编号 制取气体A(下列反应产生的混合气体) B中的现象 结论 a 在烧瓶中加热适量浓HNO3 4HNO3 △ 4NO2↑+O2↑+2H2O↑ 充满红棕色气体.木炭不复燃.火星熄灭 NO2不支持燃烧 b 加热AgNO3固体 2AgNO3 △ 2NO2↑+O2↑+2Ag 充满红棕色气体.木炭复燃 NO2支持燃烧 c 加热Cu(NO3)2固体 2Cu(NO3)2 △ 4NO2↑+O2↑+2CuO 充满红棕色气体.木炭复燃 NO2支持燃烧 你认为a.b.c三个结论是否可靠?说出你的理由. a. ▲ .原因是 ▲ . b. ▲ .原因是 ▲ . c. ▲ .原因是 ▲ . 高三化学期未考试答案及评分标准
网址:http://m.1010jiajiao.com/timu3_id_371529[举报]
21A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出)。
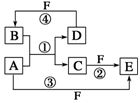
(1) 若A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,A、F所含元素同周期,则A元素在周期表中的位置 ,D的原子结构示意图为 ,
反应①的化学方程式为_____________________________________________。
(2)若A是常见的变价金属的单质,D、F是气态单质,且反应①在水溶液中进行。
反应②也在水溶液中进行,其离子方程式是________________________,
已知光照条件下D与F反应生成B,写出该反应的化学方程式:_________________。
查看习题详情和答案>>