网址:http://m.1010jiajiao.com/timu3_id_370674[举报]
(1)第一组同学称取样品m
①为完成测定,以下图示中还缺少的仪器名称是_______________________。
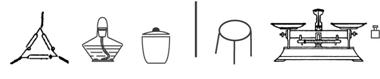
②为了减少实验误差,在加热至恒重的过程中应如何操作。
___________________________________________________________________。
③若坩埚质量为m
(2)第二组同学称取样品m g,设计了如下图所示的装置:
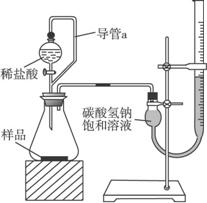
①装置中导管a的作用是________________________________________________________。
②实验结束时,该组同学在测量实验中生成气体体积时应注意哪些问题?
____________________________________________________________________
____________________________________________________________________。
(3)分析上述两组实验方案,你认为哪组实验方案的误差会小些。
____________________________________________________________________。
(4)请你设计一种除上述实验原理以外的方案,写出反应的化学方程式。
____________________________________________________________________。
查看习题详情和答案>>
已知:①反应Ⅱ包含2NaHSO3?Na2S2O5+H2O等多步反应.
②Na2S2O5遇酸发生分解:S2O52-+2H+=2SO2↑+H2O
根据要求回答下列问题:
(1)实验室制取氨气的化学反应方程式是
| ||
| ||
(2)室温下,0.1mol?L-1氯化铵溶液pH=5.1.若室温下氨水的电离常数Kb=10-x,则x=
(3)流程中“加热”时发生反应的化学方程式为
| ||
| ||
(4)要加快流程中硫磺燃烧速度,可以采取的措施是
(5)反应Ⅱ需控制参加反应的固体与气体的物质的量之比接近
①酸性高锰酸钾; ②品红溶液; ③澄清石灰水;
④饱和碳酸氢钠溶液;⑤NaOH溶液; ⑥稀硫酸.
CoCl2·6H2O是一种饲料营养强化剂.以含钴废料(含少量Fe、Al等杂质)制取CoCl2·6H2O的一种新工艺流程如下图:
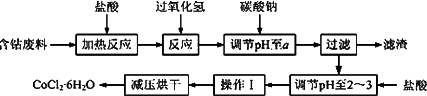
已知:
①钴与盐酸反应的化学方程式为:Co+2HCl=CoCl2+H2↑
②CoCl2·6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴.
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
请回答下列问题:
(1)在上述新工艺中,用“盐酸”代替原工艺中“盐酸与硝酸的混酸”直接溶解含钴废料,其主要优点为________.
(2)加入碳酸钠调节pH至a,a的范围是________;
(3)操作Ⅰ包含3个基本实验操作,它们是________、________和过滤.
(4)制得的CoCl2·6H2O需减压烘干的原因是________.
(5)为测定产品中CoCl2·6H2O含量,某同学将一定量的样品溶于水,再向其中加入足量的AgNO3溶液,过滤,并将沉淀烘干后称量其质量.通过计算发现产品中CoCl2·6H2O的质量分数大于100%,其原因可能是________(任写1点).
CoCl2·6H2O是一种饲料营养强化剂.以含钴废料(含少量Fe、Al等杂质)制取CoCl2·6H2O的一种新工艺流程如下图:

已知:
①钴与盐酸反应的化学方程式为:Co+2HCl=CoCl2+H2↑
②CoCl2·6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴.
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:

请回答下列问题:
(1)在上述新工艺中,用“盐酸”代替原工艺中“盐酸与硝酸的混酸”直接溶解含钴废料,其主要优点为__________________.
(2)加入碳酸钠调节pH至a,a的范围是______________.
(3)操作Ⅰ包含3个基本实验操作,它们是________和过滤.
(4)制得的CoCl2·6H2O需减压烘干的原因是_______________.
(5)为测定产品中CoCl2·6H2O含量,某同学将一定量的样品溶于水,再向其中加入足量的AgNO3溶液,过滤,并将沉淀烘干后称量其质量.通过计算发现产品中CoCl2·6H2O的质量分数大于100%,其原因可能是_______________.
(6)在实验室中,为了从上述产品中获得纯净的CoCl2·6H2O,采用的方法是_________________.
CoCl2·6H2O是一种饲料营养强化剂。以含钴废料(含少量Fe、Al等杂质)制取CoCl2·6H2O的一种新工艺流程如下图:
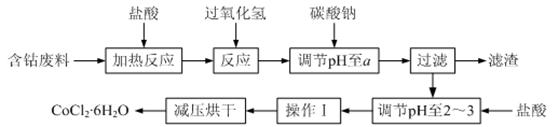
已知:
①钴与盐酸反应的化学方程式为:Co+2HCl=CoCl2+H2↑
②CoCl2·6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴。
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 7.6 | 3.4 |
| 完全沉淀 | 4.1 | 9.7 | 9.2 | 5.2 |
请回答下列问题:
⑴在上述新工艺中,用“盐酸”代替原工艺中“盐酸与硝酸的混酸”直接溶解含钴废料,其主要优点为 ▲ 。
⑵加入碳酸钠调节pH至a,a的范围是 ▲ 。
⑶操作Ⅰ包含3个基本实验操作,它们是 ▲ 和过滤。
⑷制得的CoCl2·6H2O需减压烘干的原因是 ▲ 。
⑸为测定产品中CoCl2·6H2O含量,某同学将一定量的样品溶于水,再向其中加入足量的AgNO3溶液,过滤,并将沉淀烘干后称量其质量。通过计算发现产品中CoCl2·6H2O的质量分数大于100%,其原因可能是 ▲ 。
⑹在实验室中,为了从上述产品中获得纯净的CoCl2·6H2O,采用的方法是 ▲ 。
查看习题详情和答案>>