摘要: 某稀硝酸能与5.4g铝恰好反应.当这份酸在与铁反应时.最多消耗铁的量为 A. 16.8g B. 0.3mol C. 11.2g D. 0.2mol
网址:http://m.1010jiajiao.com/timu3_id_369036[举报]
某课外学习小组,为探究稀硝酸能与Cu反应生成无色的NO气体,设计了如下图所示的装置。请回答下列问题:

(1)请写出稀硝酸与Cu反应的离子方程式__________________
(2)写出向U形管中注入稀硝酸并将左管充满的操作过程:______________
(3)将左管充满稀硝酸的原因是_______________
(4)实验开始时,反应很慢,为加快反应速率,应采取什么措施?_______________
(5)实验中HNO3与Cu的反应能否自动停止?为什么______________
(6)在实验中,证明生成的无色气体是NO的操作是_____________
(7)为防止气体从分液漏斗上口外逸,污染空气,教师建议 同学们在漏斗上口处放一小团蘸有浓NaOH的棉花,将有毒 气体吸收。其中一种气体与NaOH溶液反应生成亚硝酸盐 和硝酸盐,请写出化学方程式_________________。
查看习题详情和答案>>
(2)写出向U形管中注入稀硝酸并将左管充满的操作过程:______________
(3)将左管充满稀硝酸的原因是_______________
(4)实验开始时,反应很慢,为加快反应速率,应采取什么措施?_______________
(5)实验中HNO3与Cu的反应能否自动停止?为什么______________
(6)在实验中,证明生成的无色气体是NO的操作是_____________
(7)为防止气体从分液漏斗上口外逸,污染空气,教师建议 同学们在漏斗上口处放一小团蘸有浓NaOH的棉花,将有毒 气体吸收。其中一种气体与NaOH溶液反应生成亚硝酸盐 和硝酸盐,请写出化学方程式_________________。
 NO很容易与许多分子迅速发生反应,科学家发现在生物体中不断地产生NO,用于在细胞和细胞间传递信息;NO还参与心血管系统、免疫系统以及中枢和外围神经系统的调控.
NO很容易与许多分子迅速发生反应,科学家发现在生物体中不断地产生NO,用于在细胞和细胞间传递信息;NO还参与心血管系统、免疫系统以及中枢和外围神经系统的调控.(1)实验室用金属铜和稀硝酸制取NO的离子方程式为
3Cu+8H++2NO3-═3Cu2++4H2O+2NO↑
3Cu+8H++2NO3-═3Cu2++4H2O+2NO↑
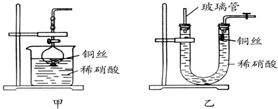
.(2)NO是有毒气体,某学生为防止污染,用分液漏斗和烧杯装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图甲所示.
打开分液漏斗的活塞使反应进行,在分液漏斗中实际看到的气体是红棕色的,原因是
2NO+O2═2NO2
2NO+O2═2NO2
(写化学方程式).(3)为证明铜丝与稀硝酸反应生成的确实是NO,某学生另设计了一套如图乙所示的装置制取NO.反应开始时,可以在U形管右端观察到无色的NO气体.长玻璃管的作用是
接收被气体压出U形管的液体,防止稀硝酸溢出
接收被气体压出U形管的液体,防止稀硝酸溢出
.(4)假设实验中12.8g Cu全部溶解,需要通入标准状况下
2.24
2.24
L O2才能使NO全部溶于水.(5)用金属铜制取硝酸铜,从节约原料和防止环境污染的角度考虑,下列4种方法中最好的是
丁
丁
(填“甲”“乙”“丙”或“丁”),理由是制取相同质量的Cu(NO3)2,丁所消耗的HNO3的量最少(原料的利用率最高)且不产生污染环境的气体
制取相同质量的Cu(NO3)2,丁所消耗的HNO3的量最少(原料的利用率最高)且不产生污染环境的气体
.甲:铜
| 浓硝酸 |
乙:铜
| 稀硝酸 |
丙:铜
| 氯气 |
| 硝酸 |
丁:铜
| 空气 |
| 硝酸 |
某学习小组设计了如图装置进行浓、稀硝酸分别与NO反应的实验,以探究浓、稀硝酸氧化性的相对强弱(夹持仪器已略去).
还可选用的药品:浓硝酸、3mol?L-1稀硝酸、蒸馏水、浓硫酸、足量氢氧化钠溶液
已知:
①浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO.由此可得出浓硝酸的氧化性强于稀硝酸的结论.
②氢氧化钠溶液不与NO反应,但能与NO2发生反应,生成NaNO3与NaNO2
(1)加药品时,若已知③中装的是稀硝酸,为了达到探究目的,并避免实验过程有害气体排放到空气中,则还应在装置②、④、⑥中依次加入的药品是
(2)滴加浓硝酸之前,应打开弹簧夹a,通入N2一段时间,目的是
(3)写出装置①中发生反应的化学方程式
(4)装置②的作用是
(5)该小组得出探究结论所依据的实验现象是
(6)实验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色.甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体.同学们分别设计了以下4个实验来判断两种看法是否正确.这些方案中可行的是(选填序号字母)
a.加热该绿色溶液,观察颜色变化
b.加水稀释该绿色溶液,观察颜色变化
c.向该绿色溶液中通入氮气,观察颜色变化
d.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化.
查看习题详情和答案>>

还可选用的药品:浓硝酸、3mol?L-1稀硝酸、蒸馏水、浓硫酸、足量氢氧化钠溶液
已知:
①浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO.由此可得出浓硝酸的氧化性强于稀硝酸的结论.
②氢氧化钠溶液不与NO反应,但能与NO2发生反应,生成NaNO3与NaNO2
(1)加药品时,若已知③中装的是稀硝酸,为了达到探究目的,并避免实验过程有害气体排放到空气中,则还应在装置②、④、⑥中依次加入的药品是
水
水
、浓硝酸
浓硝酸
、氢氧化钠溶液
氢氧化钠溶液
.(2)滴加浓硝酸之前,应打开弹簧夹a,通入N2一段时间,目的是
赶净装置中的空气,使整个装置充满氮气,防止装置②中反应生成的NO被空气氧化
赶净装置中的空气,使整个装置充满氮气,防止装置②中反应生成的NO被空气氧化
.关闭弹簧夹a后,还应进行的操作是将装置⑤中的导管末端伸入倒置的烧瓶内
将装置⑤中的导管末端伸入倒置的烧瓶内
,然后再打开弹簧夹b,滴加浓硝酸.(3)写出装置①中发生反应的化学方程式
Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
.(4)装置②的作用是
将NO2转化为NO
将NO2转化为NO
.装置⑥的作用是2NO2+2OH-=NO3-+NO2-+H2O
2NO2+2OH-=NO3-+NO2-+H2O
(用离子方程式表示).(5)该小组得出探究结论所依据的实验现象是
装置③中液面上方气体仍为无色,装置④中液面上方气体由无色变为红棕色
装置③中液面上方气体仍为无色,装置④中液面上方气体由无色变为红棕色
.(6)实验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色.甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体.同学们分别设计了以下4个实验来判断两种看法是否正确.这些方案中可行的是(选填序号字母)
acd
acd
.a.加热该绿色溶液,观察颜色变化
b.加水稀释该绿色溶液,观察颜色变化
c.向该绿色溶液中通入氮气,观察颜色变化
d.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化.
某学习小组设计了如图装置进行浓、稀硝酸分别与NO反应的实验,以探究浓、稀硝酸氧化性的相对强弱(夹持仪器已略去).

还可选用的药品:浓硝酸、3mol?L-1稀硝酸、蒸馏水、浓硫酸、足量氢氧化钠溶液
已知:
①浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO.由此可得出浓硝酸的氧化性强于稀硝酸的结论.
②氢氧化钠溶液不与NO反应,但能与NO2发生反应,生成NaNO3与NaNO2
(1)加药品时,若已知③中装的是稀硝酸,为了达到探究目的,并避免实验过程有害气体排放到空气中,则还应在装置②、④、⑥中依次加入的药品是______、______、______.
(2)滴加浓硝酸之前,应打开弹簧夹a,通入N2一段时间,目的是______.关闭弹簧夹a后,还应进行的操作是______,然后再打开弹簧夹b,滴加浓硝酸.
(3)写出装置①中发生反应的化学方程式______.
(4)装置②的作用是______.装置⑥的作用是______(用离子方程式表示).
(5)该小组得出探究结论所依据的实验现象是______.
(6)实验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色.甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体.同学们分别设计了以下4个实验来判断两种看法是否正确.这些方案中可行的是(选填序号字母)______.
a.加热该绿色溶液,观察颜色变化
b.加水稀释该绿色溶液,观察颜色变化
c.向该绿色溶液中通入氮气,观察颜色变化
d.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化.
查看习题详情和答案>>

还可选用的药品:浓硝酸、3mol?L-1稀硝酸、蒸馏水、浓硫酸、足量氢氧化钠溶液
已知:
①浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO.由此可得出浓硝酸的氧化性强于稀硝酸的结论.
②氢氧化钠溶液不与NO反应,但能与NO2发生反应,生成NaNO3与NaNO2
(1)加药品时,若已知③中装的是稀硝酸,为了达到探究目的,并避免实验过程有害气体排放到空气中,则还应在装置②、④、⑥中依次加入的药品是______、______、______.
(2)滴加浓硝酸之前,应打开弹簧夹a,通入N2一段时间,目的是______.关闭弹簧夹a后,还应进行的操作是______,然后再打开弹簧夹b,滴加浓硝酸.
(3)写出装置①中发生反应的化学方程式______.
(4)装置②的作用是______.装置⑥的作用是______(用离子方程式表示).
(5)该小组得出探究结论所依据的实验现象是______.
(6)实验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色.甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体.同学们分别设计了以下4个实验来判断两种看法是否正确.这些方案中可行的是(选填序号字母)______.
a.加热该绿色溶液,观察颜色变化
b.加水稀释该绿色溶液,观察颜色变化
c.向该绿色溶液中通入氮气,观察颜色变化
d.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化.
