网址:http://m.1010jiajiao.com/timu3_id_26943[举报]
(10分)某市热电厂使用的燃料是含硫较多的煤.该厂附近一所中学的同学经常闻到空气有异味,且空气能见度差.学习化学后,同学们意识到这有可能是该厂排出的废气超标造成的,于是在老师的指导下做了探究实验,请你填写下列空白,
【提出问题】该厂附近所降雨水是否是酸雨?空气里SO2是否超标呢?
【查阅资料】I.我国关于SO2在风景区、居民区、工厂区的空气质量最高标准分别见下表: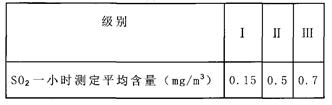
Ⅱ.硫酸钡既不溶于水,也不溶于酸(如不与稀盐酸、稀硝酸等反应).
【设计实验1】第一组同学取刚降到地面的雨水水样,用pH计(测pH的仪器)每隔几分钟测一次pH,其数据如下表所示:
所降雨水 (填“是”或“不是”)酸雨。在测定时间内酸雨pH减小的原因可能是__
【设计实验2】第二小组同学设计以下步骤来测定空气中SO2的含量.
(1)用2L的空可乐瓶采集工厂附近的空气样品,采样的具体操作是:
(2)向取回的装有空气样品的可乐瓶中倒入NaOH溶液,盖紧瓶塞后充分振荡,仿照CO2与NaOH溶液的反应,写出SO2与NaOH溶液反应的化学方程式:
(3)加入一定量氧化剂H2O2,使其中Na2SO3完全转化为Na2SO4.向可乐瓶中加入过量的BaCl2溶液.Na2SO4和BaCl2反应的化学方程式为: ____
(4)经过过滤、洗涤、烘干,称量固体质量为1.165mg.
计算:1.165mg硫酸钡中硫元素的质量为 mg.由质量守恒定律可知,2L空气样品中SO2的质量为 mg.
由空气质量标准可得出结论:该厂排放的SO2严重超标.。
【发现新问题】考虑到空气中的各种气体成分,第一组认为第二组同学的SO2的含量偏大,其依据是 ;你提出的实验改进方案是
【反思与应用】为尽快改善该地区的空气质量,请你提出一条合理化建议:
【提出问题】该厂附近所降雨水是否是酸雨?空气里SO2是否超标呢?
【查阅资料】I.我国关于SO2在风景区、居民区、工厂区的空气质量最高标准分别见下表:

Ⅱ.硫酸钡既不溶于水,也不溶于酸(如不与稀盐酸、稀硝酸等反应).
【设计实验1】第一组同学取刚降到地面的雨水水样,用pH计(测pH的仪器)每隔几分钟测一次pH,其数据如下表所示:

所降雨水 (填“是”或“不是”)酸雨。在测定时间内酸雨pH减小的原因可能是__
【设计实验2】第二小组同学设计以下步骤来测定空气中SO2的含量.
(1)用2L的空可乐瓶采集工厂附近的空气样品,采样的具体操作是:
(2)向取回的装有空气样品的可乐瓶中倒入NaOH溶液,盖紧瓶塞后充分振荡,仿照CO2与NaOH溶液的反应,写出SO2与NaOH溶液反应的化学方程式:
(3)加入一定量氧化剂H2O2,使其中Na2SO3完全转化为Na2SO4.向可乐瓶中加入过量的BaCl2溶液.Na2SO4和BaCl2反应的化学方程式为: ____
(4)经过过滤、洗涤、烘干,称量固体质量为1.165mg.
计算:1.165mg硫酸钡中硫元素的质量为 mg.由质量守恒定律可知,2L空气样品中SO2的质量为 mg.
由空气质量标准可得出结论:该厂排放的SO2严重超标.。
【发现新问题】考虑到空气中的各种气体成分,第一组认为第二组同学的SO2的含量偏大,其依据是 ;你提出的实验改进方案是
【反思与应用】为尽快改善该地区的空气质量,请你提出一条合理化建议:


(1)发热剂需接触到空气才会发热,原因是铁要与 、 等物质共同作用才会生锈,铁生锈发生氧化反应,放出热量。
(2)试推测发热剂成分氯化钠的作用是 ,从而更快的放出热量;“暖足贴”的发热还应用了活性炭具有 性。
(3)打开用过的“暖足贴”,兴趣小组的同学们发现原先黑色的铁粉颜色变成了红棕色。他们想到了金属的回收及利用的重要性,考虑能否用学过的知识将之还原成铁粉。于是,他们在实验室找来炭粉及Fe2O3粉末,在做完图乙所示实验后,发现澄清石灰水变浑浊,试管中粉末全部变为黑色。
A组一同学将黑色粉末倒在纸上,发现纸竟然烧起来了,原因是 ;另一同学立即用一块湿抹布进行扑盖,火马上熄灭,试说明灭火原理 。
(4)B组同学在正确操作之后,取少量黑色粉末,加入足量稀硫酸充分振荡,但她惊讶地发现黑色粉末没有溶解,试管中也未产生预期的气泡,这说明该反应并没有生成 。
(5)A、B组同学查阅资料,得到关于铁的氧化物相关信息如下:
根据以上信息,试写出图乙实验中炭粉与Fe2O3发生反应的化学方程式
经分析后,A、B同学试着提高反应温度后,实验出现了预期的现象。
(6)两组同学联想到还原性气体H2,通过继续查阅资料发现酒精灯火焰的温度在600℃左右,而H2还原氧化铜所需温度大约在250℃,他们按图丙所示进行实验,看到了预期现象,写出试管中反应的方程式 。
“暖足贴”利用铁氧化生锈时会放热的原理从而达到给人局部热敷的作用,具有一贴即热,快速热敷的作用,深受大众的喜爱。下图甲是某品牌“暖足贴”的图片。A、B两小组的同学,通过查阅资料发现,其主要成份为:铁粉、活性炭、水、食盐等物质。

[来源:Z.xx.k.Com]
(1)发热剂需接触到空气才会发热,原因是铁要与 、 等物质共同作用才会生锈,铁生锈发生氧化反应,放出热量。
(2)试推测发热剂成分氯化钠的作用是 ,从而更快的放出热量;“暖足贴”的发热还应用了活性炭具有 性。
(3)打开用过的“暖足贴”,兴趣小组的同学们发现原先黑色的铁粉颜色变成了红棕色。他们想到了金属的回收及利用的重要性,考虑能否用学过的知识将之还原成铁粉。于是,他们在实验室找来炭粉及Fe2O3粉末,在做完图乙所示实验后,发现澄清石灰水变浑浊,试管中粉末全部变为黑色。
A组一同学将黑色粉末倒在纸上,发现纸竟然烧起来了,原因是 ;另一同学立即用一块湿抹布进行扑盖,火马上熄灭,试说明灭火原理 。
(4)B组同学在正确操作之后,取少量黑色粉末,加入足量稀硫酸充分振荡,但她惊讶地发现黑色粉末没有溶解,试管中也未产生预期的气泡,这说明该反应并没有生成 。
(5)A、B组同学查阅资料,得到关于铁的氧化物相关信息如下:
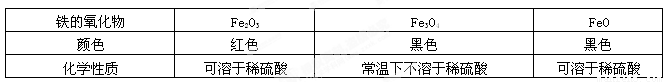 根据以上信息,试写出图乙实验中炭粉与Fe2O3发生反应的化学方程式
根据以上信息,试写出图乙实验中炭粉与Fe2O3发生反应的化学方程式
经分析后,A、B同学试着提高反应温度后,实验出现了预期的现象。
(6)两组同学联想到还原性气体H2,通过继续查阅资料发现酒精灯火焰的温度在600℃左右,而H2还原氧化铜所需温度大约在250℃,他们按图丙所示进行实验,看到了预期现象,写出试管中反应的方程式 。
查看习题详情和答案>>
“暖足贴”利用铁氧化生锈时会放热的原理从而达到给人局部热敷的作用,具有一贴即热,快速热敷的作用,深受大众的喜爱。下图甲是某品牌“暖足贴”的图片。A、B两小组的同学,通过查阅资料发现,其主要成份为:铁粉、活性炭、水、食盐等物质。

(1)发热剂需接触到空气才会发热,原因是铁要与 、 等物质共同作用才会生锈,铁生锈发生氧化反应,放出热量。
(2)试推测发热剂成分氯化钠的作用是 ,从而更快的放出热量;“暖足贴”的发热还应用了活性炭具有 性。
(3)打开用过的“暖足贴”,兴趣小组的同学们发现原先黑色的铁粉颜色变成了红棕色。他们想到了金属的回收及利用的重要性,考虑能否用学过的知识将之还原成铁粉。于是,他们在实验室找来炭粉及Fe2O3粉末,在做完图乙所示实验后,发现澄清石灰水变浑浊,试管中粉末全部变为黑色。
A组一同学将黑色粉末倒在纸上,发现纸竟然烧起来了,原因是 ;另一同学立即用一块湿抹布进行扑盖,火马上熄灭,试说明灭火原理 。
(4)B组同学在正确操作之后,取少量黑色粉末,加入足量稀硫酸充分振荡,但她惊讶地发现黑色粉末没有溶解,试管中也未产生预期的气泡,这说明该反应并没有生成 。
(5)A、B组同学查阅资料,得到关于铁的氧化物相关信息如下:
 根据以上信息,试写出图乙实验中炭粉与Fe2O3发生反应的化学方程式
根据以上信息,试写出图乙实验中炭粉与Fe2O3发生反应的化学方程式
经分析后,A、B同学试着提高反应温度后,实验出现了预期的现象。
(6)两组同学联想到还原性气体H2,通过继续查阅资料发现酒精灯火焰的温度在600℃左右,而H2还原氧化铜所需温度大约在250℃,他们按图丙所示进行实验,看到了预期现象,写出试管中反应的方程式 。
查看习题详情和答案>>