摘要:22.用纯净的锌粒与稀盐酸反应制取氢气气体.请回答: (1)实验过程如下图所示.分析判断 段化学反应速率最快.这段反应速率最快的原因是 . (2)为了减缓上述反应的速率.欲向溶液中加入下列物质.你认为可行的是 A.蒸馏水 B.氯化钠固体 C.氯化钠溶液 D.浓盐酸 (3)除了上述方法外.你认为还可以采取哪些措施来减缓化学反应速率? .
网址:http://m.1010jiajiao.com/timu3_id_145387[举报]
 用纯净的锌粒与稀盐酸反应制取氢气气体,请回答:
用纯净的锌粒与稀盐酸反应制取氢气气体,请回答:(1)实验过程如下图所示,分析判断
EF
EF
段化学反应速率最快,EF
EF
段收集的氢气最多.(2)将锌粒投入盛有稀盐酸的烧杯中,刚开始时产生H2的速率逐渐加快,其影响因素是
该反应是放热反应,温度升高,反应速率加快
该反应是放热反应,温度升高,反应速率加快
,一定时间后反应速率逐渐减慢,其原因是随着反应的进行,盐酸的浓度逐渐减小,反应速率逐渐减小
随着反应的进行,盐酸的浓度逐渐减小,反应速率逐渐减小
.(3)为了减缓上述反应的速率,欲向溶液中加入下列物质,你认为可行的是
ACE
ACE
A.蒸馏水 B.氯化钠固体 C.氯化钠溶液 D.浓盐酸 E.降低温度
(4)EF段产生H2的反应速率为
7.0
7.0
mL?min-1.(5分)用纯净的锌粒与稀盐酸反应制取氢气气体,请回答:
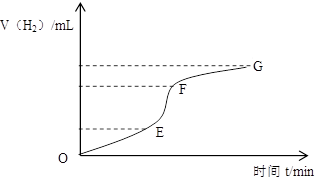
(1)实验过程如下图所示,分析判断________段化学反应速率最快,_______段收集的氢气最多。这段反应速率最快的原因是 。
(2)为了减缓上述反应的速率,欲向溶液中加入下列物质,你认为可行的是( )
A.蒸馏水 B.氯化钠固体 C.氯化钠溶液 D.浓盐酸
(3)除了上述方法外,你认为还可以采取哪些措施来减缓化学反应速率?(至少回答一种) 。
查看习题详情和答案>>
(8分)用纯净的锌粒与稀盐酸反应制取氢气气体,请回答:
(1)实验过程如下图所示,分析判断________段化学反应速率最快,这段反应速率最快的原因是 。
(2)为了减缓上述反应的速率,欲向溶液中加入下列物质,你认为可行的是( )
A.蒸馏水 B.氯化钠固体 C.氯化钠溶液 D.浓盐酸
(3)除了上述方法外,你认为还可以采取哪些措施来减缓化学反应速率?(回答一种即可)
。
查看习题详情和答案>>
